Lysozym
Den lysozym eller muramidase er et protein lang globulært hundre aminosyrer (130) hos mennesker som er involvert i forsvaret mot bakterielle infeksjoner. Den er tilstede i mange dyrearter (virveldyr, insekter, midd og visse bløtdyr). Det finnes spesielt i en rekke sekreter ( tårer , spytt , morsmelk , slim ...) og i eggehvite (129 aminosyrer hos høner).
Det er en sur glykosidhydrolase ( EC 3.2.1.17) utskilt av granulocytter og monocytter . Det ødelegger bakterieveggen til gram-positive bakterier ved å katalysere hydrolysen av peptidoglykanene som utgjør den. Denne egenskapen har fått noen forfattere Til å kvalifisere den som et kroppslig antibiotikum . Mer spesifikt er lysozym en av bestanddelene av medfødt immunitet .
Dette proteinet ble oppdaget av Alexander Fleming i 1922.
Eggehvite lysozym (type C) har en søt smak 200 ganger mer intens enn den for det søtende proteinet thaumatin (ved terskelen for oppfatning ).
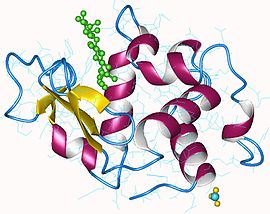
Lysozym Tertiær struktur av lysozym av kyllingegg ( PDB 132l )
Tertiær struktur av lysozym av kyllingegg ( PDB 132l )
| EF nr. | EC |
|---|---|
| CAS-nummer |
| IUBMB | IUBMB-oppføring |
|---|---|
| IntEnz | IntEnz-visning |
| BRENDA | BRENDA inngang |
| KEGG | KEGG-inngang |
| MetaCyc | Metabolisk vei |
| PRIAM | Profil |
| FBD | Strukturer |
| GÅ | AmiGO / EGO |
 Bobwhite vaktel lysozym ( PDB 1DKJ )
Bobwhite vaktel lysozym ( PDB 1DKJ )
| Pfam | PF00062 |
|---|---|
| Klan Pfam | CL0037 |
| InterPro | IPR001916 |
| LØNNHET | PDOC00716 |
| SCOP | 1e0g |
| OVERFAMILIE | 1e0g |
| TCDB | 9.B.41 |
| CAZy | GH22 |
| CDD | cd00119 |
Handlingsmåte
Lysozym kan fungere som et medfødt opsonin , eller som et lytisk enzym som er i stand til å lysere bakterier, spesielt gram-positive bakterier, uavhengig av patogenisitet. I kontrast er gramnegative bakterier generelt resistente mot dette enzymet takket være det ytre laget av lipopolysakkarider (LPS) som karakteriserer dem. Dette LPS-laget dekker murveggen (f.eks. Et lag av peptidoglykaner) og beskytter det mot angrep av lysozym ved å forhindre tilgang til dette enzymet.
Lysozym fungerer som et medfødt uspesifikt opsonin ved å feste seg til bakterieoverflaten, og derved redusere den negative ladningen og lette fagocytose av bakteriene før opsoninene i systemet fikk immunitet . Med andre ord letter lysozym fagocytose av leukocytter .
Når det gjelder bakteriell lysis, angriper enzymet peptidoglykanene som utgjør veggen av bakterier (spesielt grampositive bakterier ). Faktisk, lysozym hydrolyse kovalente bindinger (β1 → 4-glukosidiske ledd) mellom N-acetyl-muramic og 4 th karbonatom i den N-acetyl-glukosamin . Peptidoglycan-molekylet er assosiert med bindingsstedet til enzymet ( Binding Site ) lokalisert i en fordypning mellom de to domenene. Dette tvinger substratmolekylet til å vedta konformasjonen av overgangstilstanden. Den aminosyrene Glu 35 ( glutaminsyre, aminosyre nummer 35), og Asp 52 ( asparaginsyre , aminosyre nummer 52) har vist seg å være avgjørende for enzymatisk aktivitet. Glu 35 fungerer som en protondonor ved den glykosidiske broen, og spalter CO-bindingen av substratet, mens Asp 52 fungerer som en nukleofil som tillater forbigående dannelse av et glykosylert enzym. Denne reagerer så med et vannmolekyl , og gir sluttproduktet av hydrolysen og enzymet i sin opprinnelige form.
Lysozymrelaterte sykdommer
En mutasjon i det lysozym -genet kan føre til opphopning av amyloid-proteiner i visse vev.
Diagnostisk bruk
Et økt nivå av lysozym i blodet er ofte knyttet til sarkoidose . Verdier på 8 mg / L eller mer anses å være høye.
Referanser
- (en) Mr. Muraki, K. Harata, N. Sugita og K. Sato , " røntgenstruktur av humant lysozym merket med 2 ', 3'-epoxypropyl-β-glykosid av Man β1,4-GlcNAc. Structural Change and Recognition Specificity at Subsite B ” , Acta crystallographica Seksjon D - Structural Biology , vol. 54, n o Pt 1, September 1998, s. 834-843 ( PMID 9757098 , DOI 10.1107 / S090744499800122X , les online )
- Verdiene for massen og antall rester som er angitt her er verdiene til proteinforløperen som skyldes oversettelsen av genet , før posttranslasjonelle modifikasjoner , og kan avvike betydelig fra de tilsvarende verdiene For det funksjonelle proteinet .
- Lenka Grunclov, Hélène Fouquier, Václav Hyps og Petr Kopásek, Lysozym fra tarmen til den myke flåtten Ornithodoros moubata: sekvensen, fylogeni og regulering etter fôring ; Developmental & Comparative Immunology Volume 27, Issue 8, September 2003, Pages 651-660 doi: 10.1016 / S0145-305X (03) 00052-1 ( Abstract )
- (en) Masuda, T. & Kitabatake, utvikling i bioteknologisk produksjon av søte proteiner. J. Biosci. Bioeng. 2006, 102, 375–389