Protein
De proteinene ble definert som makromolekyler biologisk finnes i alle levende celler , men nyere studier viser at det finnes også hundrevis om ikke tusenvis av mikro- eller nano proteiner. De er dannet av en eller flere polypeptidkjeder . Hver av disse kjedene er sammensatt av sekvensen av rester av aminosyrer bundet sammen av peptidbindinger .
Proteiner utfører en rekke funksjoner i levende celler og i vev . De er enzymatiske proteiner ( enzymer ) som katalyserer de kjemiske syntese- og nedbrytningsreaksjonene som er nødvendige for metabolismen av cellen. Andre proteiner gir en strukturell rolle i cytoskelettet eller vevet ( aktin , kollagen ), noen er molekylære motorer som tillater mobilitet ( myosin ), andre er involvert i kondisjonering av DNA ( histoner ), regulering av genuttrykk ( transkripsjonsfaktorer ), energi metabolisme ( ATP-syntase ) eller overføring av cellulære signaler ( membranreseptorer ).
Proteinkjedene syntetiseres i cellen av ribosomene , fra informasjonen kodet i genene , som bestemmer i hvilken rekkefølge de 22 aminosyrene, kalt proteinogener , som er innlemmet direkte under genenes biosyntese . Sekvensen av aminosyrer som kalles polypeptidet sekvensen . Av post-translasjonelle modifikasjoner kan deretter gripe inn når det syntetiserte proteinet, som kan ha effekten av å modifisere de fysiske eller kjemiske egenskapene. Det er også vanlig at ikke-proteinmolekyler, kalt protesegrupper , binder stabilt til proteiner og bidrar avgjørende til deres biologiske funksjoner: dette er for eksempel tilfellet med hem i hemoglobin , uten hvilket dette proteinet ikke kunne føre oksygen i blodet .
Proteiner vedtar en tredimensjonal struktur som gjør at de kan utføre sin biologiske funksjon. Denne spesielle strukturen bestemmes fremfor alt av deres aminosyresekvens, hvis forskjellige fysisk-kjemiske egenskaper fører til at proteinkjeden tar en stabil folding.
I laboratoriet kan de skilles fra andre cellulære bestanddeler ved hjelp av forskjellige teknikker som ultrasentrifugering , utfelling , elektroforese og kromatografi . Den genteknologi har innført en rekke metoder for å legge til rette for proteinrensing. Deres struktur kan studeres ved immunhistokjemi , stedrettet mutagenese , røntgenkrystallografi , kjernemagnetisk resonans og massespektrometri .
Protein er en viktig komponent i mat dyret, de nedbrytes i fordøyelseskanalen og frigjøres aminosyrene blir deretter gjenbrukt av kroppen.
vi skiller mellom komplette proteiner og ufullstendige proteiner. Et komplett protein inneholder alle de ni essensielle aminosyrene, mens et ufullstendig protein som finnes i matvarer av vegetabilsk opprinnelse ikke inneholder dem alle.
Etymologi
Proteinene ble oppdaget fra 1835 i Nederland av den organiske kjemikeren Gerardus Johannes Mulder (1802-1880), under navnet wortelstof . Det var hans berømte svenske kollega, Jöns Jacob Berzelius , som foreslo navnet protein til ham i 1838 .
Begrepet protein kommer fra de gamle greske prôtos som betyr først , essensielt . Dette refererer sannsynligvis til det faktum at proteiner er essensielle for livet og ofte utgjør majoriteten (del 60%) av tørrvekten til (dyre) celler . En annen teori er at protein refererer, i likhet med det proteaniske adjektivet, til den greske guden Proteus som kan endre form etter eget ønske. Proteiner har mange former og utfører flere funksjoner. Men dette ble ikke oppdaget før mye senere, i løpet av XX th århundre .
Biokjemi
Proteiner dannes fra en eller flere polypeptidkjeder , som er lineære biopolymerer , kan være ganske lange, sammensatt av en tjue syrer L -a-amino forskjellige. Vi snakker generelt om protein med mer enn femti rester i molekylet, og peptid med opptil noen få titalls rester.
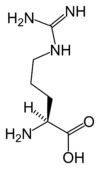
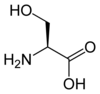
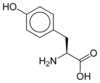
Alle proteinogene aminosyrer - med unntak av prolin - har en felles struktur som består av en funksjon karboksylsyre , et primært amin på α-karbonet og en sidekjede . Sistnevnte har et veldig bredt utvalg av kjemiske strukturer, og det er den kombinerte effekten av alle disse sidekjedene i en polypeptidkjede som bestemmer den tredimensjonale strukturen så vel som de kjemiske egenskapene til sistnevnte. Tavlen nedenfor viser den kjemiske strukturen til de 22 proteinogene aminosyrene:
|
Struktur av 22 proteinogene aminosyrer . Den pyrrolysine og selenocystein (ovenfor grånet) er spesifikke for visse proteiner : - den pyrrolysine bare funnet i noen archaeal metanogener , - den selenocystein er også til stede hos eukaryoter , men a priori i flere titalls av enzymer familie av oksidoreduktaser . De andre 20 aminosyrene, kalt standarder, er derimot universelt distribuert i alle kjente levende vesener. |
Aminosyrer i en polypeptidkjede som er bundet sammen med peptidbindinger som er etablert mellom karboksylgruppen -COOH av en første aminosyre og den primære amin -NH 2 et sekund:
Ryggraden i proteinet består således av en lineær aminosyrekjede som sidekjedene er koblet til og bundet av peptidbindinger. Peptidbindingen har to former av resonans som delvis gir den egenskapene til en dobbeltbinding , som begrenser rotasjon rundt sin akse, slik at de fire atomer i amid- gruppen - (C = O) NH- er alltid omtrent i samme plan . De to andre bindingene som utgjør ryggraden i aminosyren, kan derimot rotere fritt. De to tosvinklede vinklene som tilsvarer disse to indre bindingene bestemmer den lokale geometrien som er vedtatt av proteinkjeden.
Karboksylenden av polypeptidsidekjeden kalles ende C- terminal , mens aminsiden kalles ende N- terminal . Ordene protein, polypeptid og peptid er ganske tvetydige og deres betydning kan overlappe hverandre. Vi snakker generelt om protein i referanse til det komplette biologiske molekylet utstyrt med en stabil konformasjon, mens et peptid generelt betegner et kortere molekyl uten en stabil tredimensjonal struktur. Grensen mellom de to er veldig upresis og ligger rundt noen titalls aminosyrerester.
Størrelser
Proteiner ble alltid antatt å være store (ved biomolekylære skalaer); det var en følelse fra 1980-tallet, og vi visste fra begynnelsen av 1990-tallet at dette ikke var tilfelle, etter oppdagelsen av en, så av noen få andre MicroProteins (noen ganger kalt MiPs ). Siden den gang har forskere demonstrert eksistensen av hundrevis og deretter tusenvis av mikroproteiner og nanoproteiner (noen ganger assosierer bare noen få aminosyrer, kanskje selvmonterte), så små at klassiske genomiske analysesystemer ikke kan oppdage dem. De ser ut til å ha nøkkelroller i celler i proteinkomplekset , ved å samhandle i protein-protein-forhold. Noen kontrollerer altså aktiviteten til større proteiner, og spiller en rolle som regulatorer etter translasjon, uten å samhandle direkte med DNA eller RNA. Andre fremmer muskelutvikling og regulerer muskelsammentrekning . Atter andre bidrar til håndtering av intracellulært avfall (gammelt, nedbrutt eller mangelfullt RNA). I planter kunne de delta i påvisning av lys og i andre tilfeller spille en rolle i fytohormonal signalisering . Hos dyr deltar de i funksjonen til den biologiske klokken .
Det finnes spesielt i gift (fra edderkopper , skorpioner og andre giftige dyr ). Komplekse nanoproteiner kan opprettes in vitro ved selvmontering av aminosyrer ; de kan kanskje brukes til biomolekylær gjenkjenning og katalyse. De har allerede blitt funnet å være av kommersiell interesse: Noen insektmidler bruker det. De er av medisinsk interesse: de brukes til å merke hjernesvulster for å tillate mer presis kirurgi.
Struktur
Proteiners natur bestemmes fremfor alt av deres aminosyresekvens, som utgjør deres primære struktur . Aminosyrer med svært forskjellige kjemiske egenskaper, deres arrangement langs polypeptidkjeden bestemmer deres romlige arrangement. Dette er beskrevet lokalt av deres sekundære struktur , stabilisert av hydrogenbindinger mellom nærliggende aminosyrerester, og globalt av deres tertiære struktur , stabilisert av alle interaksjoner mellom restene - noen ganger veldig fjernt på peptidsekvensen, men brakt i romlig kontakt ved foldingen av proteinet - så vel som mellom selve proteinet og dets miljø. Til slutt er sammensetningen av flere proteinunderenheter for å danne et funksjonelt kompleks beskrevet av den kvartære strukturen til dette settet.
Ytterligere kovalente bindinger kan også dannes, enten innenfor den samme proteinkjeden, eller mellom forskjellige peptidkjeder i et protein, spesielt gjennom dannelsen av disulfidbroer mellom cysteinrester .
De fleste proteiner vedtar en unik tredimensjonal konformasjon. Den naturlige formen til et protein in vivo er dets opprinnelige tilstand , som er den formen det tar for å være biologisk aktiv og funksjonell. Mange proteiner er i seg selv biologisk aktive fra dem under påvirkning av den romlige fordelingen av rester av aminosyrer som utgjør dem, andre trenger å bli hjulpet til å gjøre dette av kaperonproteiner som skal brettes i henhold til deres opprinnelige tilstand.
Organisasjonsnivåer
I biokjemi kan vi derfor skille mellom fire organisasjonsnivåer for å beskrive strukturen til proteiner:
- Den primære strukturen tilsvarer sekvensen av aminosyrer.
- Den sekundære strukturen beskriver arrangementet av aminosyrerester som kan observeres i atomskalaen. Stabilisert av hydrogenbindinger , er disse lokale arrangementene for eksempel α-helikser , β-arkene , fatene β eller albuene. Det er flere varianter, og det er vanlig at et protein har flere typer sekundære strukturer som helhet.
- Den tertiære strukturen tilsvarer den generelle formen til proteinet som kan observeres på skalaen til hele molekylet. Den beskriver samspillet mellom de forskjellige elementene i den sekundære strukturen. Det er stabilisert ved hjelp av en hel rekke interaksjoner som oftest fører til dannelse av en hydrofob kjerne , eventuelt med saltbindinger, hydrogenbindinger, disulfid-broer , eller til og post-translasjonelle modifikasjoner . En tertiær struktur blir ofte referert til som folding av et protein.
- Den kvaternære strukturen beskriver komplekset som følge av montering av flere proteinmolekyler (flere polypeptidkjeder), kalt i dette tilfellet proteinunderenheter for å danne et enkelt proteinkompleks. Alle proteiner består ikke nødvendigvis av flere underenheter og har derfor ikke alltid en kvartær struktur.
Proteiner er ikke helt stive molekyler. De vil sannsynligvis vedta flere relaterte konformasjoner mens de utfører sine biologiske funksjoner. Overgangen fra en av disse konformasjonene til en annen kalles konformasjonsendring . I tilfelle av et enzym kan for eksempel slike konformasjonsendringer induseres av interaksjonen med substratet på nivået av det aktive stedet . I løsning gjennomgår proteiner også mange konformasjonsendringer på grunn av termisk vibrasjon av kollisjonen med andre molekyler.
Biologiske implikasjoner og bestemmelse av tertiære og kvartære strukturer
Det er tre hovedgrupper av proteiner i henhold til deres tertiære eller kvaternære struktur: kuleproteinene , de fibrøse proteinene og membranproteinene . Nesten alle kuleproteiner er oppløselige og er ofte enzymer . Fiberholdige proteiner spiller ofte en strukturell rolle, som kollagen , hovedbestanddelen av bindevev , eller keratin , et protein som består av hår og negler . Membranproteiner er ofte reseptorer eller kanaler som gjør at polære eller elektrisk ladede molekyler kan passere gjennom membranen .
Kunnskap om tertiær eller kvaternær struktur av et protein kan gi viktig informasjon for å forstå hvordan dette proteinet utfører sin biologiske funksjon. Den røntgen-krystallografi , og NMR-spektroskopi er vanlige eksperimentelle metoder for å studere proteinstruktur, som kan ene og den andre gir informasjon med en oppløsning for å skalere atom . NMR-data gir informasjon som det er mulig å estimere en delmengde av avstander mellom visse par atomer, noe som gjør det mulig å utlede mulige konformasjoner av dette molekylet. Den interferometri dobbelt polariserende er en kvantitativ analysemetode for måling av det samlede konformasjonen av proteinet og dets konformasjonsendringer som en funksjon av dets interaksjon med andre stimuli. Den sirkulære dikroismen gir en annen laboratorieteknikk for å løse bestemte elementer i sekundærstrukturen til proteiner ( α helices og ark β spesielt). Den kryo-elektronmikroskopi gir strukturell informasjon med lavere oppløsning på meget store proteiner, inkludert virus . Den elektron krystallografi (i) , teknisk enden av den foregående, gjør det mulig i enkelte tilfeller også produsere data med høy oppløsning, særlig for to-dimensjonale krystaller av membranproteiner . De adskilte proteiner konstruksjoner generelt er deponert i proteindata Bank (PDB), en åpen tilgang database og gir strukturen av tusen proteiner for hvilke de kartesiske koordinater for hvert atom er tilgjengelige.
Antall proteiner hvis struktur er løst er mye lavere enn antall gener hvis sekvens er kjent. I tillegg er delmengden av proteiner hvis struktur er løst, forutinntatt til fordel for proteiner som lett kan fremstilles for analyse ved røntgenkrystallografi, en av hovedmetodene for å bestemme proteinstrukturer. Spesielt er globulære proteiner relativt lettest å krystallisere for krystallografi, mens membranproteiner er vanskeligere å krystallisere og er underrepresentert blant proteinene som er tilgjengelige i PDB. For å avhjelpe denne situasjonen har strukturgenomiske tilnærminger blitt gjennomført for å løse strukturene som er representative for de viktigste proteinfoldingsklassene . Metoder for prediksjon av proteinstruktur har som mål å gi midler til å generere den sannsynlige strukturen til et protein fra strukturer som kan bestemmes eksperimentelt.
Syntese
De sure a-amino- proteinogene er samlet i polypeptider i celler av ribosomene fra den genetiske informasjonen som overføres av messenger-RNA fra DNA som omfatter gener . Det er nukleotidsekvensen av DNA, transkribert identisk i messenger RNA, som bærer informasjonen som er lest av ribosomer for å produsere proteiner i henhold til peptidsekvensen spesifisert av genene. Korrespondansen mellom nukleotidsekvensen til DNA og messenger RNA på den ene siden og peptidsekvensen til proteinene som er syntetisert på den andre siden, bestemmes av den genetiske koden , som i det vesentlige er den samme for alle kjente levende ting bortsett fra et antall ganske begrensede variasjoner.
Genetisk kode
Den genetiske koden etablerer samsvaret mellom en triplett av nukleinbaser , kalt et kodon , på messenger RNA og en proteinogen α-aminosyre . Denne korrespondansen blir utført in vivo av overførings-RNAene , som er RNAer som maksimalt inneholder hundre nukleotider og bærer en aminosyre som forestrer deres 3'-OH-ende. Hver av aminosyrene er knyttet til spesifikke overførings-RNAer, som også bærer spesifikke kodoner, slik at hver av de 64 mulige kodonene bare kan kode en aminosyre. På den annen side kan hver av de 22 proteinogene aminosyrene kodes av flere forskjellige kodoner. Det er enzymene som utfører forestring av messenger-RNA med aminosyrer - aminoacyl-tRNA-syntetaser - som opprettholder den genetiske koden: faktisk binder disse enzymene spesifikt både til et gitt overførings-RNA og til en aminosyre. Gitt, slik at hver type overførings-RNA er bare forestret med en spesifikk aminosyre.
Tilfellet med selenocystein og pyrrolysin er noe annerledes ved at disse spesielle aminosyrene ikke blir kodet direkte av spesifikke kodoner, men ved translasjonell omkoding av stoppkodoner i nærvær av spesielle innsettingssekvenser kalt henholdsvis SECIS- elementet og elementet. PYLIS , som koder UGA (Opal) og UAG (Amber) stopper kodoner i henholdsvis selenocystein og pyrrolysin. I tillegg er selenocystein ikke bundet som sådan til dets overførings-RNA, fordi det er for reaktivt til å eksistere fritt i cellen; det er serinet som er bundet til et selenocystein-overførings-RNA Sec tRNA av serin-tRNA-ligasen . Den seryl - tRNA Sec kan ikke brukes av ribosomene som det ikke blir gjenkjent av forlengelsesfaktorer som er involvert i biosyntesen av proteiner , slik som serin kan bli innlemmet i selenoproteins i stedet for selenocystein. I motsetning til dette, seryl-tRNA Sec er et substrat for visse enzymer som dens omdannelse til sélénocystéinyl - tRNA Sec : direkte omforming av den syntase selenocystein i bakterier , indirekte omdannelse via den U- -phosphoséryl -ARNt Sec suksessivt ved O - phosphoseryl-tRNA Sec kinase og O- fosfoseryl-tRNA: selenocysteinyl-tRNA-syntase i arkea og eukaryoter .
Genene kodet i DNA blir først og fremst transkribert til pre-messenger RNA av enzymer som RNA-polymeraser . De fleste levende ting modifiserer dette pre-messenger RNA gjennom et sett med prosesser som kalles post-transkripsjonelle modifikasjoner som fører til modent messenger RNA. Sistnevnte kan deretter brukes av ribosomer til å tjene som modell under proteinbiosyntese . I prokaryoter kan messenger-RNA brukes så snart det syntetiseres eller blir oversatt til proteiner etter at de har forlatt nukleoid . I motsetning til det, i eukaryoter , produseres messenger-RNA i cellens kjerne mens proteiner syntetiseres i cytoplasmaet , så messenger-RNA må krysse kjernemembranen .
Biosyntese
Biosyntese av et protein fra et messenger RNA er oversettelsen av dette mRNA. Messenger RNA binder seg til ribosomet, som leser det sekvensielt ved tre nukleotider på hvert trinn av syntesen. Hver triplett av nukleotider utgjør et kodon på messenger-RNA, som antikodonet til et overførings-RNA som gir den tilsvarende aminosyren kan binde seg . Den sammenkoblingen mellom det kodonet og antikodonet er basert på komplementariteten av sine respektive sekvenser . Det er denne komplementariteten som sikrer gjenkjennelsen mellom overførings-RNA og kodonen til messenger-RNA. Aminosyren som tilveiebringes av overførings-RNA på ribosomet, etablerer en peptidbinding med den C- terminale enden av den gryende kjeden, som gjør at den kan utvides med en aminosyrerest. Ribosomet beveger deretter tre nukleotider på messenger RNA for å møte et nytt kodon, som nøyaktig følger det forrige kodonet. Denne prosessen gjentas til ribosomet er foran et stoppkodon , i hvilket tilfelle translasjon stopper.
Biosyntesen av et protein blir utført, og resten etter rest, enden N- terminal til enden C- terminal . Når den er syntetisert, kan proteinet gjennomgå forskjellige mod -translasjonelle modifikasjoner som spaltning , fosforylering , acetylering , amidering , metylering , glykosylering , lipidering eller til og med dannelse av disulfidbindinger . Størrelsen på proteinene som således syntetiseres er veldig variabel. Denne størrelsen kan uttrykkes i antall aminosyrerester som utgjør disse proteiner, så vel som i dalton (symbol Da), som i molekylærbiologi , svarer til den atommasseenhet . Ettersom proteiner ofte er ganske store molekyler, blir deres masse ofte uttrykt i kilodalton (symbol kDa). For eksempel har gjærproteiner en gjennomsnittlig lengde på 466 aminosyrerester, for en masse på 53 kDa . De største kjente proteiner er de titins av sarcomers danner myofibrillene av tverrstripet skjelettmuskler : mus titin- inneholder noen 35 213 aminosyrerester består av 551,739 atomer med en masse på over 3900 kDa og en lengde l av størrelsesorden 1 mikrometer .
Kjemisk syntese
De små proteinene kan også syntetiseres in vitro ved en rekke metoder kjent peptidsyntese , som er basert på teknikker for organisk syntese slik som kjemisk ligering (in) for effektivt å produsere peptider. Kjemisk syntese gjør det mulig å introdusere unaturlige aminosyrer i polypeptidkjeden, for eksempel ved å plassere fluorescerende prober på sidekjeden til noen av dem. Disse metodene er nyttige i laboratoriet innen biokjemi og cellebiologi, men brukes vanligvis ikke til kommersielle applikasjoner. Kjemisk syntese er ikke effektiv til å syntetisere peptider av mer enn ca. 300 aminosyrerester , og proteiner som er produsert på denne måten, vil kanskje ikke lett anta sin opprinnelige tertiære struktur . De fleste metoder for kjemisk proteinsyntese går fra enden C- terminal til slutten N- terminal , det vil si i motsatt retning av biosyntese av proteiner med ribosomer .
Funksjoner
Blant alle bestanddelene i cellen er proteiner de mest aktive elementene. Bortsett fra noen RNA , er de fleste andre biologiske molekyler ikke kjemisk reaktive nok, og det er proteinene som virker på dem. Proteiner utgjør omtrent halvparten av tørrstoffet i en E. coli- celle, mens RNA og DNA utgjør henholdsvis en femtedel og 3%. Alle proteinene uttrykt i en celle utgjør proteomet .
Hovedegenskapene til proteiner som lar dem utføre sine biologiske funksjoner, er deres evne til å binde seg til andre molekyler på en veldig spesifikk og veldig stram måte. Regionen til et protein som binder seg til et annet molekyl er dets bindingssted, som ofte danner en depresjon, hulrom eller "lomme" i overflaten av molekylet. Det er proteinets tertiære struktur og den kjemiske naturen til sidekjedene til restene av aminosyrene på bindingsstedet som bestemmer spesifisiteten til denne interaksjonen. Bindingsseter kan føre til meget spesifikke og tette bånd: Således er de ribonuklease-inhibitor bindes til humant angiogenin med en sub-femtomolar dissosiasjonskonstant ( <10 -15 mol L -1 ) men ikke binder seg ikke i det hele tatt til den ranpirnase , homologe av amfibier av dette proteinet (konstant større enn 1 mol L- 1 ). En liten kjemisk modifisering kan radikalt endre et molekyls evne til å samhandle med et gitt protein. Dermed binder aminoacyl-tRNA-syntetasen spesifikk for valin til sistnevnte uten å samhandle med isoleucin , som imidlertid er strukturelt veldig nær den.
Proteiner kan binde seg til andre proteiner eller til små molekyler som substrater . Når de spesifikt binder seg til andre proteiner som er identiske med seg selv, kan de polymerisere for å danne fibriller . Dette er vanlig for strukturelle proteiner, dannet av kuleformede monomerer som selvmonteres for å danne stive fibre. Av protein-protein interaksjoner også regulere deres aktivitet enzym , fremdriften av cellesyklus og sammenstilling av store proteinkomplekser realisere dele nært beslektede reaksjoner en felles biologisk funksjon. Proteiner kan også binde seg til overflaten av cellemembraner og ofte til og med bli en integrert del av dem. Evnen til visse proteiner til å endre konformasjon når de binder seg til spesifikke molekyler tillater konstruksjon av ekstremt komplekse cellesignalnettverk . Generelt er studiet av interaksjoner mellom spesifikke proteiner et sentralt element i vår forståelse av hvordan celler fungerer og deres evne til å utveksle informasjon.
Enzymer
Den mest synlige delen av proteinene i cellen er enzymet , det vil si biomolekyl som katalyserer de kjemiske reaksjonene . Enzymer er generelt veldig spesifikke og akselererer bare en eller få kjemiske reaksjoner. De aller fleste kjemiske reaksjoner i metabolismen utføres av enzymer. I tillegg til metabolisme er sistnevnte også involvert i genuttrykk , DNA-replikasjon , DNA- reparasjon , transkripsjon av DNA til RNA , og oversettelse av messenger-RNA til proteiner. Noen enzymer jobber med andre proteiner for å binde eller spalte visse funksjonelle grupper og rester av andre biomolekyler i dem, i en prosess som kalles posttranslasjonell modifisering . Enzymer katalyserer over 5000 forskjellige kjemiske reaksjoner. Som alle katalysatorer modifiserer de ikke kjemisk likevekt, men akselererer reaksjoner, noen ganger i betydelige proporsjoner; således katalyserer orotidin-5'-fosfat-dekarboksylase i millisekunder en reaksjon som ellers ville tatt flere millioner år.
Molekyler som binder seg til enzymer og som kjemisk endres av dem, kalles substrater . Selv om enzymer noen ganger består av flere hundre aminosyrerester, er det bare noen få av dem som kommer i kontakt med enzymets substrat (er), og et veldig lite antall - vanligvis tre eller fire - er direkte involvert i katalyse. Det aktive stedet er regionen til et enzym som er involvert i den kjemiske reaksjonen katalysert av dette proteinet: det grupperer sammen restene som binder seg til substratet eller bidrar til dets posisjonering, så vel som restene som direkte katalyserer reaksjonen.
Cellesignalering og ligandbinding
Mange proteiner er involvert i mekanismene for cellesignalering og signaltransduksjon . Enkelte proteiner som insulin tilhører det ekstracellulære miljøet og overfører et signal fra cellen hvor de syntetiseres til andre celler som noen ganger ligger i fjerne vev . Andre er membranproteiner som fungerer som reseptorer hvis hovedfunksjon er å binde til molekyler som bærer signaler og indusere en biokjemisk respons i målcellen. Mange membranreseptorer har et bindingssete eksponert til utsiden av cellen, og et felt effektor (en) i kontakt med det intracellulære medium. Dette effektordomenet kan ha en enzymatisk aktivitet eller kan gjennomgå konformasjonsendringer som virker på andre intracellulære proteiner.
De antistoffene er proteinbestanddeler i immunsystemet hvis primære funksjon er å binde seg til antigener eller xenobiotisk å merke dem for eliminering fra kroppen. Antistoffene kan skilles ut i det ekstracellulære mediet eller forankres i plasmamembranen til spesialiserte B-lymfocytter kalt plasmaceller . Der enzymer er veldig spesifikke for substratene for å akselerere veldig presise kjemiske reaksjoner, har ikke antistoffer denne begrensningen; på den annen side er deres tilknytning til målet deres ekstremt høy.
Mange ligandtransportørproteiner binder seg spesifikt til små molekyler og transporterer dem til sine destinasjoner gjennom cellene og vevet i flercellede organismer . Disse proteinene må ha høy affinitet for liganden når konsentrasjonen derav er høy, men må også kunne frigjøre den når konsentrasjonen er lav i målvevet. Det kanoniske eksempelet på det ligandbærende proteinet er hemoglobin , som fører oksygen fra lungene til andre organer og vev i alle virveldyr og har relaterte kolleger i alle levende riker . De lektiner er proteiner som binder reversibelt til visse karbohydrater med meget høy spesifisitet. De spiller en rolle i biologiske gjenkjennelsesfenomener som involverer celler og proteiner.
De transmembranproteiner kan også spille rollen som transportøren ligand protein kan forandre permeabiliteten av cellemembranen til små molekyler polare og ioner . Selve membranen har en hydrofob kjerne som polære eller elektrisk ladede molekyler ikke kan diffundere gjennom. Membranproteinene kan således inneholde en eller flere kanaler gjennom cellemembranen og la disse molekylene og disse ionene krysse den. Mange ionekanaler er veldig spesifikke for ionet de sirkulerer. Dermed er kaliumkanaler og natriumkanaler ofte spesifikke for den ene av de to ionene kalium og natrium, med unntak av den andre.
Strukturelle proteiner
Strukturelle proteiner gir stivhet og stivhet til biologiske bestanddeler som uten dem ville være flytende. De fleste strukturelle proteiner er fibrøse. Dette er for eksempel tilfellet med kollagen og elastin som er essensielle bestanddeler av bindevev slik som brusk og keratin som er tilstede i harde eller trådformede strukturer som hår , negler , fjær , hover og eksoskelettet til noen dyr . Visse kuleproteiner kan også spille en strukturell rolle, for eksempel aktin og tubulin hvis monomerer er kuleformige og oppløselige, men polymeriserer for å danne lange stive filamenter som utgjør cytoskelettet , som gjør at cellen kan opprettholde sin form og størrelse.
Den motor proteiner er spesifikke strukturelle proteiner som er i stand til å generere mekaniske krefter. Dette er for eksempel myosin , kinesin og dynein . Disse proteinene er essensielle for motiliteten til encellede organismer så vel som for sædceller fra flercellede organismer . De hjelper også med å generere kreftene som arbeider i muskelkontraksjon og spiller en viktig rolle i intracellulær transport.
Imidlertid ser mannoproteiner ut til å ha nøkkelroller i celler, spesielt ved å kontrollere porøsiteten til celleveggen.
Sammendrag av funksjoner utført av proteiner
Proteiner utfører dermed et bredt utvalg av funksjoner i cellen og kroppen:
- de strukturelle proteiner som gjør det mulig for cellen for å opprettholde dens organisasjon på plass, og som er bestanddelene i cytoskjelettet ;
- de transportproteiner , som gir overføring av forskjellige molekyler inn i og ut av cellene;
- de regulatoriske proteiner som modulerer aktiviteten til andre proteiner eller som kontroll genekspresjon ;
- de signaliseringsproteiner som fanger opp de eksterne signaler og sikrer deres overføring i cellen eller organismen; det er flere typer, for eksempel hormonelle proteiner , som hjelper med å koordinere aktivitetene til en organisme ved å fungere som signaler mellom celler;
- de reseptorproteinene , som detekterer budbringermolekyler og andre signaler for cellen for å handle i samsvar med:
- de sensoriske proteinene detektere omgivelses signaler: og svarer med å sende signaler i cellen, (f.eks lys).
- de hormonreseptorer detektere hormoner og sende signaler til cellen for å virke tilsvarende (f.eks. insulin er et hormon som, når den mottas, indikerer til cellen for å absorbere og bruk glukose );
- den motor proteiner , slik at celler eller organismer eller visse elementer (cilia) for å bevege eller deformere (f.eks. aktin og myosin tillate at muskelen til kontrakt );
- de forsvars proteiner som beskytter cellen mot smittestoffer (f.eks. antistoff );
- de lagringsproteiner som tillater bestilling av sure amino orden biosyntese andre proteiner (f.eks. ovalbumin , det viktigste protein i eggehvite gir lagring for utvikling av embryo fra kylling );
- de enzymer som endrer frekvensen av nesten alle kjemiske reaksjoner i cellen uten å bli transformert i reaksjonen.
Studiemetoder
Proteinens struktur og funksjoner kan studeres in vivo , in vitro og i silico . In vivo studier gjør det mulig å utforske den fysiologiske rollen til et protein i en levende celle eller til og med i en organisme som helhet. In vitro- studier av rensede proteiner i kontrollerte miljøer er nyttige for å forstå hvordan et protein fungerer in vivo : for eksempel å studere kinetikken til et enzym muliggjør analyse av den kjemiske mekanismen for dets katalytiske aktivitet og dets relative affinitet med hensyn til forskjellige substrater . I silico- studier bruker datamaskinalgoritmer for å modellere proteiner.
Proteinrensing
For å kunne analyseres in vitro , må et protein først ha blitt renset fra de andre kjemiske bestanddelene i cellen. Dette begynner vanligvis med lysering av cellen, der plasmamembranen brytes for å frigjøre innholdet i en løsning for å gi et lysat. Denne blandingen kan renses ved ultrasentrifugering , som gjør det mulig å skille bestanddelene i fraksjoner som inneholder henholdsvis oppløselige proteiner, lipider og membranproteiner , celleorganeller og nukleinsyrer . Den utfelling av proteinene ved frigivelse gjør det mulig å konsentrere dem fra dette lysat. Det er da mulig å bruke flere typer kromatografi for å isolere proteinene som det er ønskelig å studere i henhold til deres fysisk-kjemiske egenskaper som deres molare masse , deres elektriske ladning eller til og med deres bindingsaffinitet. Graden av rensing kan følges ved bruk av flere typer gelelektroforese hvis molekylmassen og det isoelektriske punktet til de studerte proteinene er kjent, ved spektroskopi hvis proteinet har identifiserbare spektroskopiske egenskaper, eller ved enzymatisk analyse (in) hvis proteinet bærer enzymatisk aktivitet . Videre kan proteiner isoleres i henhold til deres elektriske ladning ved isoelektrisk fokusering .
Naturlige proteiner krever etter hvert en rekke rensetrinn før de kan studeres i laboratoriet. For å forenkle denne prosessen brukes genteknologi ofte til å modifisere proteiner ved å gi dem egenskaper som gjør dem lettere å rense uten å endre struktur eller aktivitet. Det tilfører således "merkinger" som er gjenkjennelige på proteinet i form av sekvenser av aminosyrer som er identifisert, ofte et antall rester av histidin - polyhistidin-tag eller His-tag - til enden C- terminal eller i enden N- terminal av den polypeptidkjeden . Derfor, når lysatet plasseres i en kromatografisk kolonne som inneholder nikkel , blir histidinrester kompleksert med nikkel og forblir bundet til kolonnen mens de ikke-merkede bestanddelene passerer gjennom det uten å bli stoppet. Flere typer etiketter er utviklet for å tillate forskere å rense bestemte proteiner fra komplekse blandinger.
Mobil lokalisering
In vivo- studien av proteiner innebærer ofte å vite nøyaktig hvor de syntetiseres og hvor de finnes i celler. Selv om de fleste intracellulære proteiner blir produsert i cytoplasma og mest membran eller utskilte proteiner i den ekstracellulære medium er produsert i den endoplasmatiske retikulum , er det sjelden at vi forstå nøyaktig hvordan proteiner er spesielt rettet mot visse cellestrukturer eller visse cellestrukturer. Organeller . Den genteknologi gir nyttige verktøy for å få et inntrykk av plasseringen av visse proteiner, for eksempel ved å binde proteinet til et protein undersøkt tillater sted, det vil si, ved å utføre et fusjonsprotein mellom proteinet studert og et protein som brukes som en markør, slik som grønt fluorescerende protein . Den intracellulære lokaliseringen av det resulterende fusjonsproteinet kan enkelt og effektivt visualiseres ved mikroskopi .
Andre metoder for intracellulær lokalisering av proteiner involverer bruk av markører som er kjent for visse cellerom som endoplasmatisk retikulum , Golgi-apparat , lysosomer , mitokondrier , kloroplaster , plasmamembran , etc. Det er for eksempel mulig å lokalisere proteiner merket med et fluorescerende merke eller målrettet med antistoffer mot disse markørene. Immunfluorescens teknikker dermed gjøre det mulig å lokalisere spesifikke proteiner. Fluorescerende pigmenter brukes også til å merke celledeler for et lignende formål.
Den immunhistokjemi benytter vanligvis et antistoff som er rettet mot ett eller flere forskjellige proteiner som er konjugert med enzymer som sender ut signaler Lysende eller kromogen kan sammenlignes med forskjellige prøver, noe som gjør det mulig å utlede informasjon om plasseringen av proteinene som ble studert. Det er også mulig å bruke ko-fraksjoneringsteknikker i en sukrose (eller annen substans) gradient ved bruk av isopyknisk sentrifugering.
Immunoelektronmikroskopi kombinerer bruken av konvensjonell elektronmikroskopi med bruk av et antistoff rettet mot det studerte proteinet, og dette antistoffet ble tidligere konjugert til et materiale med høy elektrondensitet som gull . Dette gjør det mulig å finne ultrastrukturelle detaljer så vel som proteinet som studeres.
Proteomikk
Proteinsettet av en celle eller av en celletype utgjør proteomet , og den vitenskapelige disiplinen som studerer den er proteomikk . Disse to begrepene ble laget analogt med genom og genomikk . Hvis proteomet er avledet fra genomet, er det imidlertid ikke mulig å forutsi nøyaktig hva proteomet til en celle vil være fra den enkle kunnskapen om genomet. Faktisk varierer ekspresjonen av et gen fra en celle til en annen i samme organisme som en funksjon av celledifferensiering , eller til og med i den samme cellen som en funksjon av cellesyklusen . Videre kan det samme genet gi flere proteiner (for eksempel virale polyproteiner ), og endringer etter translasjon er ofte nødvendige for å gjøre et protein aktivt.
Blant de eksperimentelle teknikkene som brukes i proteomikk, bemerker vi todimensjonal elektroforese , som tillater separering av et stort antall proteiner, massespektrometri , som muliggjør rask og høy gjennomstrømning av proteinidentifikasjon samt sekvensering av peptider. (Oftest etter gel fordøyelse (en) ), protein chips (en) , som tillater påvisning av relative konsentrasjoner av et stort antall proteiner tilstede i en celle, og den dobbelte hybrid tilnærmingen som også tillater utforsking av protein-protein interaksjoner . Settet med protein-protein-interaksjoner i en celle kalles et interaktom . Tilnærmingen til å bestemme strukturen til proteiner blant alle mulige konformasjoner er strukturell genomikk .
Bioinformatikk
Det er nå en rekke datamaskinmetoder tilgjengelig for å analysere proteinenes struktur, funksjon og evolusjon. Utviklingen av slike verktøy ble gjort nødvendig av den store mengden genomiske og proteomiske data som var tilgjengelig for et veldig stort antall levende vesener, med utgangspunkt i det menneskelige genomet . Det er umulig å studere alle proteiner eksperimentelt, slik at bare et lite antall av dem blir studert i laboratoriet mens beregningsverktøyene gjør det mulig å ekstrapolere resultatene som er oppnådd til andre proteiner som ligner på dem. Slike homologe proteiner identifiseres effektivt ved sekvensjusteringsteknikker . Peptidsekvensen profileringsverktøy gjør det mulig å lokalisere områder som kløyves av restriksjonsenzymer , leserammene i nukleotidsekvenser , og forutsi sekundære strukturer . Det er også mulig å konstruere fylogenetiske trær og utvikle hypoteser om evolusjonen ved hjelp av programvare som ClustalW (in) for å spore forfedrene til moderne organismer og deres gener. Bioinformatikkverktøy har blitt viktig for studiet av gener og proteiner uttrykt av disse genene.
Strukturforutsigelse og simulering
I tillegg til strukturell genomikk, forutsier prediksjon av proteinstruktur å utvikle midler for effektivt å bygge sannsynlige modeller som beskriver strukturen til proteiner som ikke kunne løses eksperimentelt. Den mest effektive måten å forutsi struktur på, kalt homologimodellering , er avhengig av at det eksisterer kjente modellstrukturer hvis sekvens er lik den for proteinet som studeres. Målet med strukturell genomikk er å gi tilstrekkelig data om løste strukturer for å gjøre det mulig å belyse de som gjenstår å løse. Selv om det fortsatt er vanskelig å modellere strukturer nøyaktig når det bare er fjerne strukturelle modeller å referere til, antas det at kjernen i problemet ligger i justeringen av sekvensene fordi veldig nøyaktige modeller kan bli funnet. Etablert når en veldig nøyaktig sekvensjustering er kjent. Mange strukturer forutsigelser var nyttige for det nye feltet for protein engineering (in) , som inkluderte utvikling av nye former for folding . Et mer komplekst problem å løse ved beregning er prediksjon av intermolekylære interaksjoner, slik som prediksjon av forankring av molekyler og protein-protein-interaksjoner .
Bretting og binding av proteiner kan simuleres ved hjelp av teknikker som molekylær mekanikk , molekylær dynamikk og Monte Carlo-metoden , som drar nytte av mer og mer dataarkitekturer parallell og distribuert databehandling , som prosjektet Folding @ home eller molekylær modellering på en grafikkprosessor . Brettingen av små α-heliske proteindomener , som villin cap og tilbehørsproteinet til HIV , er vellykket simulert i silico , og hybridmetoder som kombinerer standard molekylær dynamikk med elementer av kvantemekanikk har gjort det mulig å utforske de elektroniske tilstandene til rhodopsins .
Eiendommer
Fenotype
Planen for å lage proteiner avhenger derfor først og fremst av genet . Sekvensene av gener er imidlertid ikke strengt identiske fra ett individ til et annet. I tillegg, når det gjelder diploide levende ting , er det to kopier av hvert gen. Og disse to eksemplarene er ikke nødvendigvis identiske. Et gen eksisterer derfor i flere versjoner fra ett individ til et annet og noen ganger i det samme individet. Disse forskjellige versjonene kalles alleler . Settet med alleler til et individ danner genotypen .
Siden gener finnes i flere versjoner, vil proteiner også eksistere i forskjellige versjoner. Disse forskjellige versjonene av proteiner vil forårsake forskjeller fra individ til person, slik person har blå øyne, men som andre har svarte øyne osv . Disse egenskapene, synlige eller ikke, spesifikke for hver enkelt kalles fenotypen . I det samme individet sies det at en gruppe proteiner med en lignende sekvens og identisk funksjon er isoform . Isoformer kan være resultatet av den alternative spleisen av det samme genet, ekspresjonen av flere gener av et gen, eller tilstedeværelsen av flere homologe gener i genomet.
Utvikling
Under evolusjonen har akkumuleringer av mutasjoner ført til at gener har spredt seg innenfor og mellom arter . Fra dette kommer mangfoldet av proteiner assosiert med dem. Imidlertid er det mulig å definere familier av proteiner, som selv tilsvarer familier av gener. Således, i en art, kan svært like gener, og derfor proteiner, eksistere sammen og danne en familie. To nært beslektede arter har sannsynligvis representanter for samme familie av proteiner.
Vi snakker om homologi mellom proteiner når forskjellige proteiner har en felles opprinnelse, et felles forfedren.
Sammenligningen av sekvensene av proteiner gjør det mulig å demonstrere graden av "slekt" mellom forskjellige proteiner, man snakker her om sekvenslikhet. Funksjonen til proteiner kan avvike når likheten avtar, og dermed føre til familier av proteiner som har en felles opprinnelse, men som har forskjellige funksjoner.
Analyse av proteinsekvenser og strukturer har vist at mange organiserer seg i domener , det vil si deler som får struktur og utfører en bestemt funksjon. Eksistensen av proteiner med flere domener kan være resultatet av rekombinasjonen til et enkelt gen av flere opprinnelig individuelle gener, og omvendt proteiner sammensatt av et enkelt domene kan være resultatet av separasjonen i flere gener fra et gen opprinnelig. -domene protein.
Menneskelig mat
Under fordøyelsen , fra magen, blir proteiner av plante-, bakterie-, sopp- eller animalsk opprinnelse nedbrutt ( hydrolysert ) av proteaser ; brutt ned i polypeptider og deretter til aminosyrer som er nyttige for kroppen , inkludert essensielle aminosyrer (som kroppen ikke kan syntetisere). Den pepsinogen omdannes til pepsin i kontakt med saltsyre magen. Pepsin er det eneste proteolytiske enzymet som fordøyer kollagen , hovedproteinet i bindevev .
Fordøyelsen av proteiner foregår hovedsakelig i tolvfingertarmen . De absorberes hovedsakelig når de ankommer jejunum, og bare 1% av inntatt proteiner finnes i avføringen . Visse aminosyrer forblir i tarmens epitelceller , brukt til biosyntese av nye proteiner, inkludert tarmproteiner som kontinuerlig fordøyes, resirkuleres og absorberes av tynntarmen .
Fordøyeligheten til proteiner varierer betydelig avhengig av deres natur og tilberedning av maten.
Anbefalte mengder
De Anses anbefaler en anbefalt inntak (RDI) på 0,83 g · kg -1 · d -1 , til et maksimum på 2,2 g · kg -1 · d -1 i voksne i god helse, 62 g per dag til et menneske av 75 kg . Det skal bemerkes at ANC er høyere enn gjennomsnittsbehovet som er 0,66 g · kg -1 · d -1 ifølge den samme rapporten, noe som vil gi 49,5 g per dag for forrige sak.
Det gjennomsnittlige proteinbehovet er definert av FAO, som anbefaler 49 g protein for voksne menn og 41 g for kvinner (47 hvis gravide, 58,5 hvis du ammer).
Dyr, sopp, vegetabilske proteiner
I følge American Heart Association er det ikke nødvendig å konsumere animalsk protein for å ha nok protein i kostholdet ditt: planteprotein kan gi nok essensielle og ikke-essensielle aminosyrer, så lenge kildene til protein i kosten er varierte og at kalori inntak er tilstrekkelig for å dekke energibehov. Det er ikke nødvendig å kombinere dem i samme måltid. The American Dietetic Association minner også om at planteprotein kan møte protein krav dersom anlegget kostholdet er variert og tilfredsstiller energikrav. I tillegg kan “et utvalg av vegetabilske matvarer som forbrukes i løpet av en dag, gi alle essensielle aminosyrer og sikre tilstrekkelig nitrogenretensjon og bruk hos friske voksne, slik at proteinkombinasjonen under samme måltid ikke er nødvendig. "
- Animalske proteiner : de ledsages alltid av mettede lipider , hvis forbruk ofte er overdreven, og noen ganger tilsetningsstoffer (som nitritter fra kjøttpålegg , mistenkt for å være kreftfremkallende). Animaliske proteiner, eller tilknyttede produkter som heterosykliske aminer antas også å være en risikofaktor for visse kreftformer ( tykktarm , blære ). Siden 2015 har WHO og IARC klassifisert rødt kjøtt (svinekjøtt, storfekjøtt, sau, hest og geit) som sannsynlig kreftfremkallende og bearbeidet kjøtt som et bevist kreftfremkallende middel (34.000 dødsfall / år over hele verden, ifølge en studie fra Global Burden of Disease Prosjekt ; ifølge WHO: å spise 50 gram bearbeidet kjøtt per dag øker risikoen for tykktarmskreft med 18% (et kjøtt sies å være bearbeidet hvis det har gjennomgått salting, modning, gjæring, røyking eller andre prosesser som har som mål å forbedre dets På grunn av mangel på data klarte IARC-arbeidsgruppen ikke å klassifisere rått kjøtt med hensyn til kreftrisiko, men det minner om at det utgjør en smittsom risiko . å ha biokonsentrerte forurensninger via næringskjeden.
- Planteproteiner : positive effekter er assosiert med planter som er rike på protein. De pulser er rike på protein, men også i fiber , mineraler og få en følelse av metthet for en lav glykemisk indeks. Forbruk av bønner bidrar til lavere kolesterolnivå og risikoen for kardiovaskulær ulykke og visse kreftformer ( kolorektal , prostata og bukspyttkjertel ). De er åpenbart et alternativ for veganere eller vegetarianere. Nøtter, grønnsaker, bønner, quinoa og korn inneholder store mengder protein, men også energi.
- Soppeprotein : Spiselige sopp inneholder ofte mye protein, og i likhet med planter er de kilder til kostfiber og mineraler. På den annen side, høstet i naturen eller dyrket på forurensede underlag, har de en tendens til å akkumulere mye tungmetaller , metalloider og til og med radionuklider .
Proteinkvalitet
Alle nødvendige aminosyrer må leveres av mat, med smerter for å være mangelfull, noe som innebærer forskjellige proteinkilder.
Anbefalingen om å kombinere animalsk og planteprotein i hvert måltid er ugyldiggjort siden 1994 etter en artikkel av Vernon Young og Peter Pellett som ble en referanse om proteinmetabolisme hos mennesker, og bekreftet at kombinasjonen av proteiner i måltid er helt unødvendig. Mennesker som ikke ønsker å spise animalsk protein, risikerer ikke en aminosyrebalanse i planteproteiner i kostholdet. Mange vegetabilske proteiner inneholder litt mindre enn en eller flere av de essensielle aminosyrene ( spesielt lysin og i mindre grad metionin og treonin ), uten at det eksklusive forbruket av kilder til vegetabilske proteiner hindrer et balansert kosthold i aminosyrer.
Konklusjonene i artikkelen fra Young og Pellet skal bare vurderes i det helt generelle tilfellet der korn ikke er den eksklusive matkilden, som de er nøye med å spesifisere, i tillegg, hvor de forklarer i andre artikler. I noen vanskeligstilte regioner kan matrasjoner bare omfatte frokostblandinger, noe som gir alvorlige helseproblemer for små barn, for eksempel i fattige husholdninger i staten Madhya Pradesh i India (hvete og ris).
I tillegg søker frøbedrifter å skaffe eller allerede ha oppnådd varianter av frokostblandinger med et modifisert aminosyreinnhold ( GMO ), for eksempel mais beriket med lysin.
De franske helsemyndighetene (AFSSA / ANSES ) nekter fortsatt å løse dette spørsmålet.
Kosttilskudd
Den kosttilskudd protein finnes for idrettsutøvere som ønsker å utvikle sin muskelvolum, og for folk i proteinmangel. Proteinene som brukes er ofte proteiner oppnådd fra lucerne ( Alfalfa i form av bladekstrakt (EFL) ) , feltbønner , erter eller myse (under navnet "myse") og forgrenede aminosyrer betegnet under navnet "BCAA" .
Mat rik på proteiner
- De sopper har et proteininnhold det vanskelig å måle nøyaktig (innhold tidligere overvurderes med 70 til 200% til tider), men ofte er forholdsvis høy (15 til 35% av tørrvekten av soppen), mye høyere enn kornsorter som hvete og mais, av matinteresse. Disse nivåene er sammenlignbare med belgfrukter som erter og linser.
De essensielle aminosyrer ofte står for en betydelig andel av disse proteinene ( f.eks. 61,8 og 63,3% av den totale aminosyre nivåer henholdsvis i Tricholoma portentosum og Tricholoma terreum (hvor leucin , den isoleucin og tryptofan er de begrensende aminosyrer) De korrigerte aminosyrescoreene (PDCAAS) av proteinene til disse to soppene er lave sammenlignet med kasein, eggehvite og soyabønner, men høyere enn for mange planteproteiner. Fettinnholdet var lavt (5,7% for Tricholoma porterosum og 6,6 % for Tricholoma terreum ) hos begge arter, med oljesyre og linolsyre som utgjør over 75% av de totale fettsyrene.
Noen som fungus de Paris (3,09 g protein per 100 g ) har lenge blitt dyrket og tørket, men individuelt ( som andre matvarer) kan de ha mangel på visse aminosyrer ( f.eks. svovelholdige aminosyrer, metionin og cystin når det gjelder østerssopp for eksempel), men de er rike på lysin og leucin som mangler for eksempel i frokostblandinger. De blir fremdeles oppdaget dyder ( f.eks.: Et av disse proteinene ser ut til at mus hemmer matallergi ) og defekter ( f.eks. Et annet soppprotein har vist seg å være kardiotoksisk ).
- Matvarer av animalsk opprinnelse er vanligvis mer protein enn de av vegetabilsk opprinnelse, og spesielt egg (rik på albumin) eller ost (kasein osv.), Som for eksempel parmesan, som inneholder 39,4 g / 100 g, mer enn kjøtt og fisk. I tillegg til visse kjøttvarer ( f.eks: kokt kyllingbryst med et gjennomsnittlig innhold på 29,2 g / 100 g), som biff som inneholder 26 g / 100 g, inneholder fisk som albacore tunfisk eller sardiner også omtrent 30 g / 100 g. Egg er også en kilde til protein (24 g / 100 g for fire egg).
- Visse planter eller frø er meget rike på proteiner: olje frø ( mandel , pistasj , lin , etc. ) og belgfrukter ( kikerter , bønner , linser , etc. ). Dermed inneholder 100 g råprodukt en proteindel på: 58 g for spirulina , 38 g for soyabønner , 30 g for gresskarfrø , 25 g for svarte bønner , 24 g for linser , 21 g for seitan (gluten) og nøtter , 20 g til mandler og semulegryn , 15 g til havregryn , 15 g til vill ris , 14 g til quinoa .
- Den gjær , bakterier og cyanobakterier er sjelden vokst til å bli spist direkte, men den gjær eller Spirulina (58 g protein per 100 g Spirulina) er svært rike på proteiner.
Merknader og referanser
- Oppdagelser av proteiner
- Gregory A. Petsko og Dagmar Ringe ( overs. Fra engelsk), Struktur og funksjon av proteiner , Brussel, De Boek UniversityNovember 2008, 190 s. ( ISBN 978-2-8041-5888-0 , les online )
- (i) Alex Gutteridge og Janet M. Thornton , " Understanding nature's catalytic toolkit " , Trends in Biochemical Sciences , vol. 30, n o 11november 2005, s. 622-629 ( PMID 16214343 , DOI 10.1016 / j.tibs.2005.09.006 , les online )
- (i) Harvey Lodish, Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky og James Darnell, Molecular Cell Biology , New York, WH Freeman & Company 5 th edition,august 2003, 973 s. ( ISBN 978-0-7167-4366-8 )
- Garcia Martin S (2015) Dynamic Nanoproteins: Self-Assembly of Peptides on Monolayer Protected Gold Nanoparticles
- Mitch Leslie (2019) Effekt på størrelse ; | Vitenskap 18. okt 2019: Vol. 366, utgave 6463, s. 296-299 | DOI: 10.1126 / science.366.6463.296 ( sammendrag )
- Staudt, AC og Wenkel, S. (2011). Regulering av proteinfunksjon av 'microProteins' . EMBO rapporter, 12 (1), 35-42.
- (Wang et al (2009)
- zhang et al, 2009)
- (in) Zhaohui Xu, Arthur L. Horwich og Paul B. Sigler , " Krystallstrukturen til den asymmetriske GroEL-GroES- (ADP) 7chaperonin complex ” , Nature , vol. 388, n o 6644,21. august 1997, s. 741-750 ( PMID 9285585 , DOI 10.1038 / 41944 , les online )
- (i) Lisa J Harris, Eileen Skaletsky og Alexander McPherson , " Crystallographic structure of an intact IgG1 monoclonal antody " , Journal of Molecular Biology , vol. 275, n o 5,6. februar 1998, s. 861-872 ( PMID 9480774 , DOI 10.1006 / jmbi.1997.1508 , les online )
- (in) W. Bolton og MF Perutz , " Three Dimensional Fourier Synthesis of Horse Deoxyhaemoglobin at 2.8 Å Resolution " , Nature , vol. 228, n o 5271,7. november 1970, s. 551-552 ( PMID 5472471 , DOI 10.1038 / 228551a0 , Bibcode 1970Natur.228..551B , les online )
- (i) Edward N. Baker, Thomas L. Blundell, John F. Cutfield, Susan M. Cutfield, Eleanor J. Dodson, Guy G. Dodson, Dorothy Crowfoot Hodgkin Mr. Roderick E. Hubbard, Neil W. Isaacs, Colin D. Reynolds, Kiwako Sakabe, Norioshi Sakabe og Numminate M. Vijayan , “ The structure of 2Zn grise insulin crystals at 1.5 Å resolution ” , Philosophical Transactions B , vol. 319, n o 11956. juli 1988, s. 369-456 ( PMID 2905485 , DOI 10.1098 / rstb.1988.0058 , Bibcode 1988RSPTB.319..369B , les online )
- (en) Michael B. Berry og George N. Phillips Jr. , " Krystallstrukturer av Bacillus stearothermophilus adenylatkinase med bundet Ap 5 A, Mg 2+ Ap 5 A og Mn 2+ Ap 5 Aavsløre en mellomlokkposisjon og seks koordinat oktaedral geometri for bundet Mg 2+ og Mn 2+ ” , Proteins: Structure, Function, and Bioinformatics , vol. 32, n o 3,15. august 1998, s. 276-288 ( PMID 9715904 , les online )
- (i) Harindarpal S. Gill og David Eisenberg , " krystallstrukturen av Phosphinothricin i det aktive området av glutaminsyntetasegenet belyser Mekanisme enzymatisk Hemming " , biokjemi , vol. 40, n o 7,20. februar 2001, s. 1903-1912 ( PMID 11329256 , DOI 10.1021 / bi002438h , les online )
- (in) Wojciech R. Rypniewski Hazel Holden og Ivan Rayment , " Strukturelle konsekvenser av reduktiv metylering av lysinrester i høneeggehvite lysozym: En røntgenanalyse ved 1,8-Å oppløsning " , Biochemistry , vol. 32, n o 37,21. september 1993, s. 9851-9858 ( PMID 8373783 , DOI 10.1021 / bi00088a041 , les online )
- (in) Tamir Gonen Yifan Cheng, Piotr Sliz, Yoko Hiroaki Yoshinori Fujiyoshi, Stephen C. Harrison og Thomas Walz , " Lipid-protein interactions in double layered two-dimensional crystals AQP0 " , Nature , vol. 438, n o 7068,1 st desember 2005, s. 633-638 ( PMID 16319884 , PMCID 1350984 , DOI 10.1038 / nature04321 , les online )
- (i) Daron M. Standley, Akira R. Kinjo, Kengo Kinoshita og Haruki Nakamura , " Proteinstrukturdatabaser med nye webtjenester for strukturell biologi og biomedisinsk forskning " , Briefings in Bioinformatics , vol. 9, n o 4,juli 2008, s. 276-285 ( PMID 18430752 , DOI 10.1093 / bib / bbn015 , les online )
- (i) Peter Walian, Timothy A Cross K og Bing Jap , " Structural genom av membranproteiner " , Genome Biology , vol. 5, n o 4,2004, s. 215 ( PMID 15059248 , PMCID 395774 , DOI 10.1186 / gb-2004-5-4-215 , les online )
- (in) Roy D. Sleator , " Prediction of Protein Functions " , Methods in Molecular Biology , vol. 815,2012, s. 15-24 ( PMID 22130980 , DOI 10.1007 / 978-1-61779-424-7_2 , les online )
- Forchhammer K, Bock A, “ Selenocysteinsyntase fra Escherichia coli. Analyse av reaksjonssekvensen ”, J. Biol. Chem. , vol. 266, n o 101991, s. 6324–8 ( PMID 2007585 )
- (in) Yuhei Araiso, Sotiria Palioura, Ryuichiro Ishitani, R. Lynn Sherrer, Patrick O'Donoghue, Jing Yuan, Hiroyuki Oshikane, Naoshi Domae Julian DeFranco, Dieter Söll og Osamu Nureki , " Strukturell innsikt i RNA-avhengig og eukaryal selenocysteindannelse ” , Nucleic Acids Research , vol. 36, n o 4,Mars 2008, s. 1187-1199 ( PMID 18158303 , PMCID 2275076 , DOI 10.1093 / nar / gkm1122 , les online )
- (i) Sotiria Palioura R. Lynn Sherrer, Thomas A. Steitz Dieter Söll og Miljan Simonovic , " The Human SepSecS-tRNA Sec Complex Reveals the Mechanism of Selenocysteine Education " , Science , vol. 325, n o 5938,17. juli 2009, s. 321-325 ( PMID 19608919 , PMCID 2857584 , DOI 10.1126 / science.1173755 , Bibcode 2009Sci ... 325..321P , les online )
- (i) Alice B. Fulton og William B. Isaacs , " Titin, et stort, elastisk sarkomert protein med en sannsynlig rolle i morfogenese " , BioEssays , vol. 13, n o 4,April 1991, s. 157-161 ( PMID 1859393 , DOI 10.1002 / bies.950130403 , les online )
- (in) " Titin (EC 2.7.11.1) (Connectin) Mus musculus (Mouse) " på ProtParam på ExPASy (åpnet 9. mai 2015 )
- (in) Thomas Bruckdorfer Oleg Marder og Fernando Albericio , " From Production of Peptides in Milligram Amounts for Research to Multi-Tone Quantities for Drugs of the Future " , Current Pharmaceutical Biotechnology , vol. 5, n o 1,Februar 2004, s. 29-43 ( PMID 14965208 , DOI 10.2174 / 1389201043489620 , les online )
- (i) Dirk Schwarzer og Philip A Cole , " Protein semisynthesis and Expressed Protein Ligation: chasing a protein's tail " , Current Opinion in Chemical Biology , vol. 9, n o 6,desember 2005, s. 561-569 ( PMID 16226484 , DOI 10.1016 / j.cbpa.2005.09.018 , les online )
- (in) Stephen BH Kent , " total kjemisk syntese av proteiner " , Chemical Society Reviews , vol. 38, n o toFebruar 2009, s. 338-351 ( PMID 19169452 , DOI 10.1039 / B700141J , les online )
- (in) R. Sankaranarayanan og D. Moras , " The fidelity of the translation of the genetical code " , Acta Biochimica Polonica , Vol. 48, n o to2001, s. 323-335 ( PMID 11732604 , les online )
- (i) John A. Copland, Melinda Sheffield-Moore, Nina Koldzic-Zivanovic, Sean Gentry, George Lamprou, Fotini Tzortzatou-Stathopoulou Vassilis Zoumpourlis, Randall J. Urban og Spiros A. Vlahopoulos , " Sexsteroidreseptorer i skjelettdifferensiering og epitelial neoplasi: er vevsspesifikk intervensjon mulig? ” , BioEssays , vol. 31, n o 6,Juni 2009, s. 629-641 ( PMID 19382224 , DOI 10.1002 / bies.200800138 , les online )
- (i) Stanislav Samarin og Asma Nusrat , " Regulering av epitel-apikalt krysskompleks av Rho-familiens GTPases " , Frontiers in Bioscience , Vol. 14,januar 2009, s. 1129-1142 ( PMID 19273120 , DOI 10.2741 / 3298 , les online )
- (i) Ida Schomburg Antje Chang, Sandra Placzek Carola Söhngen, Michael Rother, Maren Lang, Cornelia Munaretto Susanne Ulas, Michael Stelzer, Andreas Grote, Maurice Scheer og Dietmar Schomburg , " BRENDA i 2013: integrerte reaksjoner, kinetiske data, enzymfunksjon data, forbedret sykdomsklassifisering: nye alternativer og innhold i BRENDA ” , Nucleic Acids Research , vol. 41, n o D1,Januar 2013, D764-D772 ( PMID 23203881 , DOI 10.1093 / nar / gks1049 , les online )
- (in) A. og R. Radzicka Wolfenden , " A proficient enzym " , Science , vol. 267, n o 5194,6. januar 1995, s. 90-93 ( PMID 7809611 , DOI 10.1126 / science.7809611 , les online )
- (i) Brian P. Callahan og Brian G. Miller , " OMP decarboxylase-An enigma Persists " , Bioorganic Chemistry , vol. 35, n o 6, desember 2007, s. 465-469 ( PMID 17889251 , DOI 10.1016 / j.bioorg.2007.07.004 , les online )
- (in) Harold Rudiger, Hans-Christian Siebert, Dolores Solis, Jesus initial Jimenez-Barbero, Antonio Romero, Claus-Wilhelm von der Lieth, Teresa Diaz-Maurino og Hans-Joachim Gabius , " Medisinsk kjemi basert på sukkerkoden : Fundamentals of Lectinology and Experimental Strategies with Lectins as Targets ” , Current Medicinal Chemistry , vol. 7, n o 4,april 2000, s. 389-416 ( PMID 10702616 , DOI 10.2174 / 0929867003375164 , les online )
- Fra Nobel, JG, Klis, FM, Priem, J., Munnik, T., & Van Den Ende, H. (1990) T glukanaseløselig mannoproteiner begrenser celleveggens porøsitet i Saccharomyces cerevisiae . Gjær, 6 (6), 491-499.
- Zlotnik, HINDA, Fernandez, MP, Bowers, BLAIR, & Cabib, ENRICO (1984). Saccharomyces cerevisiae mannoproteiner danner et ytre cellevegglag som bestemmer veggporøsitet . Journal of Bacteriology, 159 (3), 1018-1026.
- Caridi A (2006) Enologiske funksjoner av parietal gjærmannoproteiner. Antonie Van Leeuwenhoek, 89 (3-4), 417-422 ( sammendrag )
- Harvey Lodish , Arnold Berk , Paul Matsudaira , Chris A. Kaiser , Monty Krieger , Matthew P. Scott , S. Laurence Zipursky og James Darnell ( overs. Pierre L. Masson og Chrystelle Sanlaville), Molecular biology of the cell ["Molecular Cellbiologi ”], Brussel, De Boeck University,2005, 3 e ed. , 1096 s. [ utgave detalj ] ( ISBN 2-8041-4802-5 )
- (i) Julie Hey, Anton Posch, Andrew Cohen, Liu Ning og Adrianna Harbers , " Fraksjonering av komplekse proteinblandinger ved flytende fase isoelektrisk fokusering " , Methods in Molecular Biology , vol. 424,2008, s. 225-239 ( PMID 18369866 , DOI 10.1007 / 978-1-60327-064-9_19 , les online )
- (i) K. Terpe , " Oversikt over taggproteinfusjoner: fra molekylære og biokjemiske grunnleggende til handelssystemer " , Applied Microbiology and Biotechnology , Vol. 60, n o 5,januar 2003, s. 523-533 ( PMID 12536251 , DOI 10.1007 / s00253-002-1158-6 , les online )
- (in) Olesya V. Stepanenko, Vladislav V. Verkhusha Irina Kuznetsova Mr. Vladimir N. Uversky and KK Turoverov , " Fluorescent Proteins as Biomarkers and Biosensors: Throwing Color Lights on Molecular and Cellular Processes " , Current Protein & Peptide Science , vol. . 9, n o 4,August 2008, s. 338-369 ( PMID 18691124 , PMCID 2904242 , DOI 10.2174 / 138920308785132668 , les online )
- (i) Rafael Yuste , " Fluorescensmikroskopi i dag " , Nature Methods , vol. 2, n o 12desember 2005, s. 902-904 ( PMID 16299474 , DOI 10.1038 / nmeth1205-902 , les online )
- (i) William Margolin , " Green Fluorescent Protein as a Reporter for Macromolecular Localization in Bacterial Cells " , Methods , vol. 20, n o 1,januar 2000, s. 62-72 ( PMID 10610805 , DOI 10.1006 / meth.1999.0906 , les online )
- (in) Terry M. Mayhew og John M. Lucocq , " Utvikling i cellebiologi for kvantitativ immunoelektronmikroskopi basert på tynne seksjoner: en gjennomgang " , Histochemistry and Cell Biology , Vol. 130, n o toAugust 2008, s. 299-313 ( PMID 18553098 , PMCID 2491712 , DOI 10.1007 / s00418-008-0451-6 , les online )
- (in) Angelika Görg, Walter Weiss og Michael J Dunn , " Current two-dimensional electrophoresis technology for proteomics " , Proteomics , vol. 4, n o 12desember 2004, s. 3665-3685 ( PMID 15543535 , DOI 10.1002 / pmic.200401031 , les online )
- (in) P. og S. Conrotto Souchelnytskyi , " Proteomiske tilnærminger i biologisk og medisinsk vitenskap: prinsipper og anvendelser " , Experimental Oncology , vol. 30, n o 3,september 2008, s. 171-180 ( PMID 18806738 )
- (in) T. J. Joos og Bachmann , " Protein microarrays: potentials and limitations " , Frontiers in Bioscience , Vol. 14,januar 2009, s. 4376-4385 ( PMID 19273356 , DOI 10.2741 / 3534 )
- (in) Manfred Koegl og Peter Uetz , " Improving yeast two-hybrid screening systems " , Briefings in Functional Genomics , vol. 6, n o 4,desember 2007( PMID 18218650 , DOI 10.1093 / bfgp / elm035 , bfg.oxfordjournals.org/content/6/4/302.full.pdf+html)
- (in) Dariusz og Krzysztof Ginalski Plewczyński , " The interactome: Predicting the protein-protein interactions in cells " , Cellular and Molecular Biology Letters , vol. 14, n o 1,Mars 2009, s. 1-22 ( PMID 18839074 , DOI 10.2478 / s11658-008-0024-7 , les online )
- (in) Chao Zhang og Sung-Hou Kim , " Oversikt over strukturell genomikk: fra struktur til funksjon " , Current Opinion in Chemical Biology , vol. 7, n o 1, Februar 2003, s. 28-32 ( PMID 12547423 , DOI 10.1016 / S1367-5931 (02) 00015-7 , les online )
- (in) Yang Zhang , " Progress and utfordringer in protein structure prediction " , Current Opinion in Structural Biology , Vol. 18 n o 3, juni 2008, s. 342-348 ( PMID 18436442 , PMCID 2680823 , DOI 10.1016 / j.sbi.2008.02.004 , les online )
- (in) Zhexin Xiang , " Fremskritt innen proteinstrukturmodell homologi " , Current Protein & Peptide Science , vol. 7, n o 3, juni 2006, s. 217-227 ( PMID 16787261 , PMCID 1839925 , DOI 10.2174 / 138920306777452312 # sthash.hup2vFsH.dpuf , les online )
- (in) Yang Zhang og Jeffrey Skolnick , " Prognosen for proteinstrukturforutsigelse kan løses ved hjelp av det nåværende PDB-biblioteket " , Proceedings of the National Academy of Sciences i De forente stater , vol. 102, n o 4, 25. januar 2005, s. 1029-1034 ( PMID 15653774 , PMCID 545829 , DOI 10.1073 / pnas.0407152101 , les online )
- (i) Brian Kuhlman, Gautam Dantas, Gregory C. Ireton, Gabriele Varani, Barry L. Stoddard og David Baker , " Design of a Novel Globular Protein Fold with Atomic-Level Accuracy " , Science , vol. 302, n o 5649, 21. november 2003, s. 1364-1368 ( PMID 14631033 , DOI 10.1126 / science.1089427 , les online )
- (in) David W. Ritchie , " Nylige fremskritt og fremtidige retninger i protein-proteindokking " , Current Protein & Peptide Science , vol. 9, n o 1, Februar 2008, s. 1-15 ( PMID 18336319 , DOI 10.2174 / 138920308783565741 , les online )
- (in) T. Herges og W. Wenzel , " In Silico Folding of a Three Helix Protein and Characterization of Its Free-Energy Landscape in an All-Atom Force Field " , Physical dreamed Letters , vol. 94, n o 1, 14. januar 2005, s. 018101 ( PMID 15698135 , DOI 10.1103 / PhysRevLett.94.018101 , Bibcode 2005PhRvL..94a8101H , les online )
- (i) Michael Hoffmann, Marius Wanko Paul Strodel, Peter H. König, Thomas Frauenheim Klaus Schulten, Walter Thiel, Emad Tajkhorshid og Marcus Elstner , " Color Tuning i rhodopsins: The Mechanism for Spectral Shift entre Bakteriorodopsin og Sensory Rhodopsin II ” , Journal of the American Chemical Society , vol. 128, n o 33, 23. august 2006, s. 10808-10818 ( PMID 16910676 , DOI 10.1021 / ja062082i , les online )
- Proteiner
- " Family Nutrition Guide " (åpnet 26. november 2014 )
- (en-US) American Heart Association , “ Vegetarian, Vegan Diet & Heart Health ” , Go Red For Women® ,26. mars 2014( les online , konsultert 29. juli 2017 )
- (in) " Position of the American Dietetic Association: Vegetarian Diets " , Journal of the American Dietetic Association ,juli 2009, s. 1267–1268 ( les online )
- Adventist Health Study-1 - Cancer Findings: Some Highlights
- WHOs pressemelding Kreftfremkallende ved forbruk av rødt kjøtt og bearbeidet kjøtt oktober 2015]
- Dry Bean-skjema på nettstedet Health Passport
- Ikke-soya belgfrukter reduserer kolesterolnivået: en metaanalyse av randomiserte kontrollerte studier
- Legume-forbruk og risiko for koronar hjertesykdom hos amerikanske menn og kvinner: NHANES I Epidemiologic Follow-up Study
- V. R. Young og PL Pellett , “ Planteproteiner i forhold til ernæring av humant protein og aminosyrer ”, The American Journal of Clinical Nutrition , vol. 59, n o 5 Suppl,Mai 1994, s. 1203S - 1212S ( ISSN 0002-9165 , PMID 8172124 , lest online , åpnet 29. juli 2017 )
- (i) VR Young og PL Pellett , " hveteproteiner i forhold til proteinbehovet og tilgjengelighet av aminosyrer " , The American Journal of Clinical Nutrition , vol. 41, n o 5,1 st mai 1985, s. 1077–1090 ( ISSN 0002-9165 og 1938-3207 , DOI 10.1093 / ajcn / 41.5.1077 , lest online , åpnet 4. februar 2020 )
- Sophie Landrin, " I India inviterer religion seg inn i tallerkenen til skolebarn " , på Le Monde ,4. februar 2020(åpnet 4. februar 2020 )
- " Feltet for anvendelse av transgenese " , om gnis-pedagogikk (åpnet 5. februar 2020 )
- " USA - Et mais beriket med lysin " , på inf'OGM ,november 2005(åpnet 5. februar 2020 )
- AFSSA / ANSES-rapport, side 232 og 233
- Proteininnholdet av sopp er vanskelig å måle nøyaktig, fordi deres kitin og andre nitrogenforbindelser innvirke på analysen av total nitrogen (f.eks Kjeldahls metode ) tidligere brukt. Kilde: Danell E. og Eaker D. (1992), aminosyre og total proteininnhold i den spiselige soppen Cantharellus cibarius (Fries) , Journal of the Science of Food and Agriculture , 60 (3), 333-337.
- Dıez VA og Alvarez A. (2001), Sammensetnings- og ernæringsstudier på to ville spiselige sopp fra Nord-Spania , Food Chemistry , 75 (4), 417-422 ( abstrakt )
- Chang ST og Buswell JA (1996), Mushroom nutriceuticals , World Journal of Microbiology and biotechnology , 12 (5), 473-476 ( abstract ).
- Peter CK Cheung (2009), Ernæringsverdi og helsemessige fordeler av sopp, sopp som funksjonell mat , (71-109).
- (en) VA Dıeez og A. Alvarez, Sammensetnings- og ernæringsstudier på to ville spiselige sopp fra Nord-Spania . I matkjemi . Bånd 75, nr . 4, desember 2001, S. 417-422, DOI : 10.1016 / S0308-8146 (01) 00229-1
- Chang ST og Miles PG (1991), Nylige trender innen verdensproduksjon av spiselige sopp , The Mushroom Journal , 503, 15–18.
- Shah H., Khalil IA og Jabeen S. (1997), Ernæringsmessig sammensetning og proteinkvalitet av Pleurotus sopp , Sarhad Journal of Agriculture (Pakistan) ( Agris / FAO sammendrag ).
- Hsieh, KY, Hsu, CI, Lin, JY, Tsai, CC og Lin, RH (2003), Oral administrering av et spiselig sopp-avledet protein hemmer utviklingen av matallergiske reaksjoner hos mus , Klinisk og eksperimentell allergi , 33 (11), 1595-1602 ( sammendrag )
- Lin, JY, Lin, YJ, Chen, CC, Wu, HL, Shi, GY og Jeng, TW (1974), kardiotoksisk protein fra spiselige sopp , Nature , 252 (5480), 235 ( abstrakt ).
- " Ciqual Table of nutritional composition of foods " , på ciqual.anses.fr (åpnet 10. september 2018 )
- Albert-François Creff og Daniel Layani, Manual of dietetics in current medical practice , Paris, Masson,2004, 301 s. ( ISBN 978-2-294-01346-1 , leses online ) , s. 4
Se også
Bibliografi
- Gregory Petsko, Dagmar Ringe (overs. Chrystelle Sanlaville, Dominique Charmot-Bensimon), Proteins struktur og funksjon , De Boeck, Brussel, 2009. ( ISBN 978-2-8041-5888-0 ) .
- Lubert Stryer, Jeremy Mark Berg, John L. Tymoczko (trad. Serge Weinman), biokjemi , Flammarion, "medisin-Sciences", Paris, 2008, 6 th ed. ( ISBN 978-2-257-00003-3 ) .
- Carl-Ivar Brändén, John Tooze (overs. Bernard Lubochinsky, pref. Joël Janin), Introduksjon til proteinstrukturen , De Boeck University, Brussel, 1996. ( ISBN 978-2-8041-2109-9 ) .
Relaterte artikler
- Kombinasjon av proteiner (mat - eksempel: ris / linser)
- Rekombinante proteiner
- Underfamilie av proteiner
- Proteinaggregering
- Aquaporin
- Rieske protein
- Lysosomal aminosyretransportør
- Fiberholdig protein
- Globulært protein
- Viciline
- transkripsjonsfaktorer
- Cdx proteiner
- Stillasprotein
- Tau-protein
- Thioprotein
- Selenoprotein
- Mannoprotein
- Mikroprotein
Eksterne linker
- ( fr ) Predictor Project En delt dataprogramvare som bruker BOINC-plattformen til å studere proteinfolding.
- (no) MRS- server En biologisk databank-server, der identifiseringen av en oppføring i PDB-banken gjør det mulig å visualisere strukturen på skjermen, i dynamisk modus (se for eksempel hva et søk i banken produserer PDB av oppføringer tilsvarende til trypsin).
- ( fr ) Proteins @ home Et omfattende prosjekt for å studere proteinfolding, som du kan delta i med datamaskinen din.