Etan
| Etan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
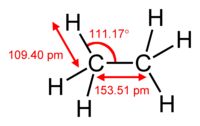
| Etanmolekyl | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-navn | etan | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
dimetyl |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.741 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-814-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6324 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
CC , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C2H6 / c1-2 / h1-2H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | flytende komprimert gass, fargeløs, luktfri i ren tilstand. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C 2 H 6 [Isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 30,069 ± 0,002 g / mol C 79,89%, H 20,11%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −183,3 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | −88,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet |
60,2 mg · l -1 ( vann , 25 ° C ) 460 ml · l -1 ( etanol , 4 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighetsparameter δ | 12,3 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumisk masse |
1.3551 kg · m -3 ( 0 ° C , 1 013 mbar , gass) 0.5441 kg · l -1 ( -88,6 ° C , 1 013 mbar , væske) ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selvantennelsestemperatur | 515 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | -135 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosjonsgrenser i luft |
2,4 - 14,3 volum% 31 - 182 g · m -3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mettende damptrykk |
37,8 bar ved 20 ° C 46,9 bar ved 30 ° C ligning:
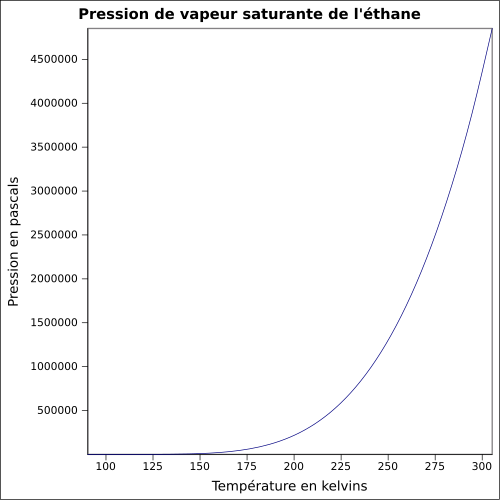
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamisk viskositet | 63,4 mPo ved -78,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt |
32,15 ° C 49 bar 0,147 l · mol -1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trippel punkt |
−182,15 ° C 0,011 bar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighet |
1326 m · s -1 (væske, -88,6 ° C ) 312 m · s -1 (gass, 27 ° C , 1 atm ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 væske, 1 bar | 126,7 J · mol -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gass | -84,0 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,583 kJ · mol -1 til -182,81 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
9,76 kJ · mol -1 til 25- ° C 14,703 kJ · mol -1 til -89,05 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
52,49 J · mol -1 · K -1 ( 25 ° C , gass) 68,68 J · mol -1 · K -1 ( -173,15 ° C , væske) ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1560,7 kJ · mol -1 ( 25 ° C , gass) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 1 437,11 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 11,56 ± 0,02 eV (gass) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallografi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallklasse eller romgruppe | P21 / n | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh-parametere |
a = 4,226 Å b = 5,623 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volum | 190.10 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H220, H220 : Ekstremt brannfarlig gass |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Kritisk komprimert gass temperatur = 32,27 ° C B1 : Brannfarlig gass nedre brennbarhetsgrense = 3,0% Offentliggjøring ved 1,0% i henhold til klassifiseringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 1 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : brannfarlig gass FN-nummer : 1035 : ETHANE Klasse: 2.1 Etikett: 2.1 : Brennbare gasser (tilsvarer gruppene betegnet med hovedstad F); Emballasje: - 
223 : nedkjølt flytende gass, brannfarlig FN-nummer : 1961 : ETHANE KJØLESVÆSKE Klasse: 2.1 Etikett: 2.1 : Brennbare gasser (tilsvarer grupper betegnet med store bokstaver F); Emballasje: -  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1,81 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den etan er et hydrokarbon av familien av alkaner med empirisk formel C- 2 H- 6. Det er en brennbar , fargeløs og luktfri gass som kan finnes i naturgass og også i petroleumsgasser .
bruk
Etan er det basiske reagenset for syntese av etylen via dampkraking , monoklor- , 1,1-diklor- og 1,1,1-trikloretan ved klorering . Ved å kombinere klorering med oksyklorering kan vinylklorid syntetiseres, og reaksjonen av etan med salpetersyre i gassfasen tillater dannelse av nitrometan og nitroetan .
Etan er en bestanddel av flytende petroleumsgass som er et drivstoff som brukes som erstatning for naturgass for bestemte bruksområder.
Fysisk-kjemiske egenskaper
Den etan blir dekomponert fra en temperatur på 500 ° C . Dets oppløselighet i vann og i alkohol er bedre enn den for metan siden, ved 20 ° C , er dette 4,7 cm 3 pr 100 cm 3 av vann og 150 cm 3 pr 100 cm 3 av alkohol .
Produksjon og syntese
Etan kommer hovedsakelig fra rensing av naturgass eller ekstrahert fra flytende petroleumsgass , en brøkdel av petroleum.
Transportere
Den transporteres for tiden flytende, men kan en dag også være i form av etanhydrat ( klatrat ).
Økologi
Etan er et atmosfærisk forurensende stoff klassifisert blant VOC ( Volatile Organic Compound ).
Det er en av forløperne for fotokjemisk forurensning , noe som særlig fører til forurensning av troposfærisk ozon .
Det anses også å være et interessant sporstoff fordi det er assosiert med geologiske metanutslipp (skifergass, naturgass, petroleumsdamp), men ikke med biogene metanutslipp (det er grunnen til at det har vært gjenstand for de siste årene. inkludert fra verdensrommet) og modellering).
Naturlige og menneskeskapte utslipp
På jorden måler vi utslipp av størrelsen femten megaton av denne gassen i atmosfæren per år:
- to til fire megaton frigjøres av gjørmevulkaner , geotermiske kilder , oljekasser og gasslekkasjer på havbunnen;
- rundt ti megaton kommer fra skogbranner , biologisk aktivitet i havene, dyreliv og mennesker.
- en umålt mengde til dags dato kommer fra lekkasjer fra borehull, gassrørledninger og olje- og gassinstallasjoner, og spesielt skifergass basert på hydraulisk brudd .
Etan og skifergass
En studie publisert i mai 2015 i tidsskriftet Atmospheric Environment viser at etan er et godt spor etter gasslekkasjer knyttet til utnyttelse av skifergass. Disse lekkasjene kan oppdages hundrevis av miles nedovervind av utvinningsområder, inkludert i USA i stater som forbyder eller strengt kontrollerer fracking .
Denne studien fulgte anomalier oppdaget i luftinnholdet i etan i USA fra 2010, hvor det ble oppdaget i betydelige mengder i stater der det ikke skulle slippes ut: Mens det hadde vært en total reduksjon i ikke-metan VOC-utslipp og en forbedring av luftkvaliteten siden 1996, har etannivået i luften , fra 2010 til 2013, økt kraftig fra 7 til 15% av det totale organiske karbonet som ikke er metan i luften, en økning på “ca 30 prosent fra 2010 til 2013 ” . På det tidspunktet ble ikke metanutslippene overvåket tilstrekkelig i landet til å kunne knyttes til disse uregelmessighetene i nivået av etan i luften. Selv om ingenting i Maryland kunne forklare økningen i etannivået, ble det raskt funnet at timeverdiene målt av fotokjemiske overvåkingsstasjoner i Baltimore og Washington DC var sterkt korrelert med vindretningen og utviklingen av fracking-aktiviteter i Marcellus-bassenget ( hvor skifergass har blitt utnyttet i massiv skala i noen år), i stor avstand oppstrøms (i forhold til vinden) fra målepunktet. Værmodeller (basert på kompassrosen og vindhastigheten) bekreftet at Maryland ble utsatt for fjærhaler av fjerne utslipp fra Pennsylvania , West Virginia og Ohio . I Maryland kommer de rådende vindene fra Marcellus-bassenget 2/3 av tiden.
Forfatterne av studien var i stand til å utelukke alle kilder som kan forklare utseendet til disse etantoppene i luften (inkludert kjøretøyer, lekkasjer fra gassrørledninger eller naturgasslagring i Garrett County , Md. studie område). De fant videre at den samme analysen ikke avslørte disse etantoppene for Atlanta , Ga. Som ligger i et område som ikke er berørt av utbredt naturgassutvikling og uten nye olje- og gassoperasjoner. Denne studien bekrefter det forrige arbeidet som viser at vi undervurderte metanforurensningen som ble forårsaket av utnyttelse av skifergass, og det viser at denne forurensningen kan ha fjerne effekter (vel vitende om at etan her blir ansett som et sporstoff for annet skadeligere ( kvikksølv ) eller mer reaktive gasser fra brønner, men også fra boring, ferdigstillelse, reaktivering og utrangerte sikkerhetsinstallasjoner og arbeider ( nitrogenoksider , partikelforurensning, svoveldioksid og hydrokarbondampe også kilder til luftforurensning).
For R. Subramanian (forsker ved Carnegie Mellon , som spesialiserer seg i studiet av atmosfæriske partikler, hvis arbeid har vist at etan er en utmerket markør for metanutslipp fra utnyttelse og transport av naturgass), viser denne studien det potensielle bidraget til skifergass utvinning i Pennsylvania til luftkvalitet i Leeward stater, og behovet for å vurdere interstate transport av forurensning i å utforme miljøbestemmelser om partikkelforurensning og bakkenær ozon kontroll .
For Ehrman er disse resultatene også sterke ledetråder om at vi ikke lenger kan snakke om lokal forurensning, men at det er et "regionalt problem" . Han legger til at forfatterne av denne publikasjonen ønsket å "bringe dette temaet under offentligheten, og fortaler for langsiktig overvåking av metan, og fremme regionalt samarbeid om overvåking og reduksjon av utslipp fra produksjon av naturgass" .
Biologisk nedbrytbarhet i naturen
Metanotrofe mikrober har vært kjent i flere tiår , spesielt funnet i visse marine sedimenter. Selv om den nødvendige biokjemiske reaksjonen er kompleks og termodynamisk usannsynlig, trodde forskere derfor at det også kan være mikrober som er i stand til å konsumere etan (slippes ut i ca. 10% av naturgassplommene som finnes lokalt i dypvannet). Marine og som etter å ha steget til overflaten utgjør ca 5% av atmosfærisk metan).
En første mikroorganisme som er i stand til å konsumere etan i anaerob tilstand ble oppdaget i havbunnen (publikasjon 2019): archaea Argoarcheum ethanivorans ; den oksyderer etan takket være en symbiose med en annen mikroorganisme som forsyner den med oksygen, i en gjensidig handling ( syntrofi ), ved å redusere sulfatet til sulfid .
Merknader og referanser
- ETHANE , sikkerhetsark (er) til det internasjonale programmet for sikkerhet for kjemiske stoffer , konsultert 9. mai 2009
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Oppføring "Etan" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 19. april 2009 (JavaScript kreves)
- “ ETHANE ” , om databank for farlige stoffer (åpnet 29. november 2009 )
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , leses online ) , s. 294
- (no) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- (en) "Ethane" , på NIST / WebBook , åpnet 11. februar 2010
- (in) William M. Haynes , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor og Francis,1 st juli 2010, 91 th ed. , 2610 s. ( ISBN 9781439820773 , online presentasjon ) , s. 14-40
- (i) Carl L. yaws, Handbook of Thermodynamic diagrammer: Organic Compounds C8 til C28 , vol. 1, Huston, Texas, Gulf Pub. Co.,1996, 396 s. ( ISBN 0-88415-857-8 )
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online presentasjon ) , s. 5-89
- (i) David R. Lide, håndbok for kjemi og fysikk , Boca Raton, CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- “ Ethane ” , på www.reciprocalnet.org (åpnet 12. desember 2009 )
- Indeksnummer i tabell 3.1 i vedlegg VI til EF-forskrift nr. 1272/2008 (16. desember 2008)
- " Etan " i databasen over kjemikalier Reptox fra CSST (Quebec-organisasjonen med ansvar for arbeidsmiljø og helse), åpnet 25. april 2009
- "etan" , på ESIS , åpnes den 15 februar 2009
- Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Ullmann's Encyclopedia of Industrial Chemistry , Hydrocarbons , Wiley-VCH Verlag GmbH & Co,2000
- R. Kumar, P. Linga, I. Moudrakovski, JA Ripmeester, og P. Englezos, struktur og kinetikken for gasshydratene fra metan / etan / propan-blandinger som er relevante for utforming av naturgasshydrat lagring og transport. AlChE J. 2008; 54 (8), 2132–2144.
- Ser ut i rommet for å kvantifisere naturgasslekkasjer på jorden ; Phys.org 2015, Science X-nettverk, publisert 24. mars 2015, åpnet 2. mai 2015
- Science & Vie, Vi vet hva jorden avgasser med hydrokarboner , nº 1098, mars 2009, s. 34.
- Vinciguerra, T & al. (2015) " Regional air quality impact of hydraulisk frakturering og skifer naturgassaktivitet: Bevis fra omgivende VOC-observasjoner ," Atmospheric Environment, Volume 110, June 2015, Pages 144-150, ISSN 1352-2310, dx.doi.org/10.1016 /j.atmosenv.2015.03.056 ( sammendrag )
- News ( 1 st mai 2015) Utslipp fra naturgassbrønner kan reise langt medvinds , Phys.org, Science X Network
- Timothy Vinciguerra, Simon Yao, Joseph Dadzie, Alexa Chittams, Thomas Deskins, Sheryl Ehrman, Russell R. Dickerson (2015), Regionale luftkvalitetseffekter av hydraulisk brudd og skifer naturgassaktivitet: Bevis fra VOC-observasjoner i omgivelsene; Atmosfærisk miljø Volum 110, juni 2015, side 144–150
- (2019) Gripende mikrobe som bruker etan funnet under sjøen; En mikroorganisme som bruker etan i fravær av miljømessig oksygen, er blitt oppdaget. I havets dyp samarbeider denne mikroben, som oksyderer etan, med en annen som reduserer sulfat til sulfid , publisert 27. mars av tidsskriftet Nature
- Chen SC et al. , Anaerob oksidasjon av etan av arkea fra et marint hydrokarbon-sipp. , 2019 DOI : 10.1038 / s41586-019-1063-0






