Tinndioksid
| Tinndioksid | |
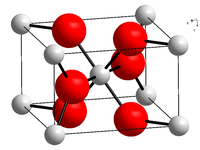 __ Sn 4+ __ O 2- Krystallgitter av tinndioksid |
|
| Identifikasjon | |
|---|---|
| IUPAC-navn | dioksotin |
| Synonymer |
tinn (IV) |
| N o CAS | |
| N o ECHA | 100.038.311 |
| N o EC | 242-159-0 |
| N o RTECS | XQ4000000 |
| PubChem | 29011 |
| ChEBI | 52991 |
| SMIL |
O = [Sn] = O , |
| InChI |
Std. InChI: InChI = 1S / 2O.Sn Std. InChIKey: XOLBLPGZBRYERU-UHFFFAOYSA-N |
| Utseende | hvitt pulver |
| Kjemiske egenskaper | |
| Brute formel |
O 2 Sn |
| Molarmasse | 150,709 ± 0,008 g / mol O 21,23%, Sn 78,77%, |
| Fysiske egenskaper | |
| T ° fusjon | 1.630 ° C |
| Volumisk masse | 6,95 g · cm -3 til 20 ° C |
| Enheter av SI og STP med mindre annet er oppgitt. | |
Den tinn-dioksyd eller tinn (IV) oksyd , er en kjemisk forbindelse med formel SnO 2. Dens mineralform er kassiteritt , som er hovedmalmen av tinn .
Fysiske egenskaper
Tinndioksid er en sterk diamagnetisk fargeløs, halvleder og amfoter , og ser ut som et pulver krystallisert hvitt. Det er den vanligste formen for tinnkjemi.
Det krystalliserer med den maske av rutil , hvor atomene av tinn har et koordinasjonstall lik 6 og atomer av oksygen har et koordinasjonstall lik 3. SnO 2blir generelt sett på som en halvleder av typen n til oksygenunderskudd.
Kjemiske reaksjoner
Tinndioksidet renses ved reduksjon til tinn og deretter forbrenning av sistnevnte i friluft.
Tinnoksider oppløses i syrer . De hydrohalogensyrer angriper SnO 2å gi heksahalostannater som [SnI 6 ] 2-. Reaksjonen til en prøve angrepet med HI- hydriodinsyre i flere timer er beskrevet:
SnO 2+ 6 HI → H 2 SnI 6+ 2 H 2 O.Likeledes SnO 2oppløses i svovelsyre H 2 SO 4for å gi tinn (IV) sulfat Sn (SO 4 ) 2 :
SnO 2+ 2 H 2 SO 4→ Sn (SO 4 ) 2+ 2 H 2 O.SnO 2oppløses i sterke baser for å gi stannater, for eksempel med natriumhydroksyd NaOHFor å gi natriumstannat Na 2 SnO 3. Å oppløse den smeltede SnO 2 / NaOH -blanding i vanngir de kjemiske forbindelsene Na- 2 [Sn (OH) 6 ] 2.
bruk
- Blandet med indium (III) oksid (In 2 O 3 ), danner det indium tinnoksid (ITO) som er det ideelle materialet for å lage de tynne gjennomsiktige elektrodene som dekker LCD-skjermer .
-
SnO 2 pulver.
-
Rutile- typen krystallinsk mesh .
Merknader og referanser
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Oppføring "Tin (IV) oxide" i den kjemiske databasen GESTIS fra IFA (tysk instans ansvarlig for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 13. november 2011 (JavaScript kreves)
- (in) ER Caley , " The actions of Hydriodic Acid is Stannic Oxide " , J. Am. Chem. Soc. , vol. 54, n o 8,August 1934, s. 3240–3243 ( ISSN 0002-7863 og 1520-5126 , DOI 10.1021 / ja01347a028 )
Se også
Relaterte artikler
Bibliografi
- Sergent N (2003) [ https://hal.inria.fr/file/index/docid/45309/filename/tel-00002302.pdf Tinndioksid: Syntese, karakterisering og studie av interaksjoner med forskjellige forurensende gasser - Anvendelse på katalysen av NOx] ; Katalyse. Jean Monnet University - Saint-Étienne <tel-00002302v2> PDF, 248 s