Flåttbåren encefalitt
Flåttbåren encefalitt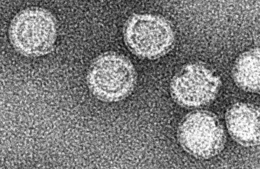 Tick-borne encefalittvirus, under et elektronmikroskop.
Tick-borne encefalittvirus, under et elektronmikroskop.
| Spesialitet | Infeksjonssykdom og nevrologi |
|---|
| ICD - 10 | A84 |
|---|---|
| CIM - 9 | 063 |
| Sykdommer DB | 29274 |
| MeSH | D004675 |
| Inkubasjon min | 7 dager |
| Maks inkubasjon | 14 dager |
| Symptomer | Hodepine , myalgi , feber , tretthet , fotofobi , meningeal syndrom ( d ) , søvnighet ( in ) , koma , oppkast , kvalme , undersøkelse for hjernehinnetegn ( d ) , lammelse og forvirring ( in ) |
| Overført sykdom | Kryssoverføring ( d ) |
| UK pasient | Flåttbåren encefalitt-pro |
Den tick-borne encephalitis eller meningoencefalitt tick eller meningoencefalitt tick vår-sommer (TBE) er en viral encefalitt forårsaket av en arbovirus av familien Flaviviridae , den TBEV som virker nesten utelukkende Vector og nesten alltid overføres av flått harde og særlig i Europa av Ixodes ricinus . Det påvirker mennesker så vel som de fleste pattedyr.
Viruset er nevrotropisk for sentralnervesystemet , det kan infisere membranene ( hjernehinnebetennelse ) som omgir hjernen og ryggmargen , og infisere dem i sin tur ( encefalitt , myelitt ), derav begrepene meningoencefalitt, encefalomyelitt, etc.
Sykdommen er fortsatt dårlig forstått. Den er fordelt over Nord-Eurasia (fra Øst-Frankrike til Japan). Den kommer i former av varierende alvorlighetsgrad, knyttet til geografisk distribusjon, kryssvektorarter og tre virusundertyper (europeisk, sibirisk og fjernøstlig).
Antall tilfeller øker i de fleste europeiske land unntatt Østerrike.
Fire vaksiner som ble ansett som trygge og effektive, ble godkjent av WHO i 2010. To er tilgjengelige i Europa og Canada. De to andre er russiske. Som hovedregel anbefales de i henhold til risikosituasjoner, spesielt for arbeidere eller reisende i endemiske skogsområder.
Historie
Oppdagelse
Sykdommen ble først beskrevet i 1931 av H. Schneider som en sesongpidemi (vår-sommer) av hjernehinnebetennelse i distriktet Neunkirchen ( Nedre Østerrike ). Det ble funnet i Sovjetunionen under epidemier i 1934 på ryddesteder i Sibir , og i 1939 ble det rapportert i den europeiske delen av Russland .
Viruset ble isolert i 1937 i Russland av Zilber og Soloviev, som også viser overføring av flåtten Ixodes persulcatus , men denne informasjonen vil ikke bli publisert før ti år senere, etter krigen. Utenfor Russland ble et europeisk virus isolert i 1949, overført av flåtten Ixodes ricinus, og i årene som fulgte er flåttbåren encefalitt identifiserbar i de fleste europeiske land.
I Nord-Kina, nær den sovjetiske grensen, ble sykdommen rapportert i 1943. Det første tilfellet i Japan ble diagnostisert i 1993. I Sør-Korea er viruset tilstede i flått, men ingen menneskelige tilfeller er oppdaget per 2017.
Den første franske saken ble beskrevet i 1968, i en gamekeeper i skogen i Illkirch , sør for Strasbourg .
Synonymer
Sykdommen har blitt kalt: Central European Encefalitis (CEE); Russisk vårsommer encefalitt (RSSE); Taiga vårsommer encefalitt ; Früh Sommer Meningo-encefalitt (FSME); Zentraleuropäische enzephalitt ; Zecken encefalitt ; Sentral-europeisk encefalitt; Russisk vår-sommer encefalitt; tofase meningoencefalitt; to-fase melk feber; biondulant meningoencefalitt; Kumlinge sykdom (oppkalt etter en finsk øy ( Kumlinge ), hvor mange tilfeller har blitt studert); Schneiders sykdom (oppkalt etter den første beskrivelsen).
Den mest vanlige navnet i XXI th århundre Tick Borne Encefalitt (TBE) på engelsk eller "TBE" på fransk. Ved bruk eller konvensjon brukes uspesifisert "flåttbåren encefalitt" og forstås som "viral encefalitt av TBE arbovirus, overført av flått", som ekskluderer bakteriell encefalitt overført av flått (slik som encefalitt ved borreliose ), og annen viral encefalitt ved andre arbovirus, ikke overført av flått (som japansk encefalitt , overført av mygg).
Klassifisering
Fram til 1970-tallet var det to sykdommer som ble tilskrevet to forskjellige virus:
- Sentral-europeisk (flåttbåren) encefalitt;
- Russisk vårsommer (flåttbåren) encefalitt.
Siden da er det ansett at disse to sykdommene, med ulik klinisk presentasjon, skyldes mer eller mindre virulente varianter av samme virus, TBEV Tick Borne Encefalitis Virus .
I XXI th århundre, basert på sekvense genom tre undertyper av TBEV virus er fremstående ledere av hjernebetennelse som ved økende alvorlighetsgrad:
- TBEV-Eu ( Europa ): Europeisk eller vestlig undertype (Øst-Frankrike til Sentral-Europa), hvis hovedvektor er flåtten Ixodes ricinus , som gir den mindre alvorlige formen av de tre;
- TBEV-Sib ( Sibir ): Sibirisk undertype (Øst-Europa og Vest-Sibir), hovedvektor Ixodes persulcatus ;
- TBEV-FE ( Fjernøsten ): fjernøstlig undertype (Øst-Sibir, Nord-Kina og Japan), hovedvektor Ixodes persulcatus , som gir den mest alvorlige formen.
Alle tre undertyper kan sirkulere samtidig i Østersjøen , den europeiske delen av Russland og i Sibir .
Fra og med 2018 tilbys to nye undertyper for diskusjon: Lake Baikal- undertypen TBEV-Bkl og Himalaya- undertypen (TBEV-Him).
Virologi
Encefalittvirus i flått av slekten Flavivirus av familien Flaviviridae , som inkluderer rundt 70 virus inkludert denguevirus , gult febervirus , virus, japansk encefalitt og West Nile-virus .
Virionen består av et enkeltstrenget RNA- molekyl assosiert med et strukturelt protein "C", og innesluttet i en sentral membran og et kappeprotein. Den har en sfærisk form, dens diameter er 50 nm , eller 1/20 th av en mikron. Den ytre konvolutten bærer to proteiner; "M" og "E", den andre er involvert i identifikasjonen av viruset og dets immunogenisitet (antigene determinanter og induksjon av beskyttende immunitet i verten).
RNA, sekvensert siden 1989, oversettes og dupliseres på de ekstracellulære membranene i det endoplasmatiske retikulumet og Golgi-apparatet .
De tre undertypene (vestlige, sibiriske og fjernøstlige) er nært beslektet genetisk og antigenisk. Disse undertypene viser ikke signifikant antigen variasjon, vaksinene som er tilgjengelige mot den vestlige undertypen vil derfor være beskyttende mot de to andre.
Viruset er varmefølsomt, ødelagt eller inaktivert ved pasteurisering , men det kan overleve i lengre perioder i rå melk og upasteuriserte meieriprodukter, og motstå det sure miljøet under mulig passasje gjennom viruset. 'Mage.
Vektorer og reservoarer
Harde flått av slekten Ixodes er de viktigste vektorer og reservoarer av TBE-viruset. I Eurasia er mer enn 8 arter identifisert som i stand til å overføre viruset. De viktigste er Ixodes ricinus og I. hexagonus i Europa, I. persulcatus i Sibir og Haemaphysalis concinna i Asia.
Kryss av livssyklus
Flåtten utvikler seg i 3 stadier (larve, nymfe, voksen) som varer i gjennomsnitt 1 år (fra 6 måneder til flere år, avhengig av klimatiske forhold). Viruset kan overføres på alle stadier.
Den midd fortrinnsvis i hi i kratt våt, i nærheten av vannveier. Hunnen legger hundrevis av egg som allerede kan være smittet.
Larver seks poter fra egg, er aktivert, og gjør sitt første blodmåltid når utetemperaturen overskrider 5 ° C . Klimatiske forhold bestemmer flåttaktivitet som kan bli forsinket (hard vinter og sen vår) eller avansert (mild vinter og tidlig vår).
De venter på offeret sitt på et gressklipp for å henge dem på vei. Under måltidet kan de overføre viruset til verten (et lite dyr: mus, ekorn osv.) Eller tvert imot bli smittet hvis offeret er bærer av viruset.
Det er et fenomen med " co-fôring " når larver eller nymfer (infiserte og ikke-infiserte) mates samtidig på samme vertsimmunkompetent mot TBE. Infiserte prøver overfører viruset til uinfiserte dyr mens det parasittiserte dyret ikke har viremi (se avsnittet patofysiologi om lokal multiplikasjon av viruset i dermis).
Etter måltidet, som kan vare i flere dager, lar larven falle og etter metamorfose blir en 8-legged nymfe . Etter et nytt blodmåltid, 1 til 2 år senere når flåtten voksenstadiet. Den måler så noen millimeter i lengden og kan klatre i buskene opptil 80 cm i høyden for å nå et større dyr (rev, storvilt). Etter dette nye blodmåltidet pares flisen, legger egg, og syklusen gjenopptas.
Viruset multipliserer og diffunderer i det generelle hulrommet, deretter i alle organene i flåtten, inkludert i spyttkjertlene (overføring ved flåttbitt) og i eggstokkene (transovarian overføring fra hunnen til hennes avkom), noe som gjør flått både vektorer og magasiner.
Viruset forblir inaktivt i flått (som ikke utvikler sykdom), men infiserte flått forblir det til slutten av livet.
Andre reservoararter
Mer enn hundre forskjellige dyrearter (pattedyr, reptiler og fugler) kan smittes med viruset, men ikke alle utgjør et reservoar.
Hovedreservoaret (annet enn selve flåttene) er små gnagere. I dem er viremia langvarig på høye nivåer. De hyppigst siterte gnagerarter er collared mus skogmus flavicollis , tre Vole Myodes glareolus , og andre som tilhører gliridae familien .
Store pattedyr og fugler har en lavere og kortvarig viremi. For store pattedyr er reservoarartene hovedsakelig vill hjort (som rådyr Capreolus capreolus ) og for fugler, skogspasserines .
Disse store pattedyrene og fuglene spiller en mindre viktig rolle som et reservoar for virus enn små pattedyr, men de spiller en nøkkelrolle i flokkenes økologi (parrings- og leggefase, vedlikehold av flåttpopulasjonen), samtidig som det sikres fjernformidling. Svært lang avstand spredt av trekkfugler virker usannsynlig, fordi flått løsner fra verten etter 5 til 9 dager.
Viruset er ikke veldig patogent hos dyr. Sjeldne tilfeller av alvorlig sykdom er beskrevet hos hunder, hester, aper, sauer, geiter og muffler.
Under viremi (multiplikasjon av virus som går gjennom blodet), kan passasjen gjøres i melken til infiserte kyr, geiter eller sauer.
I motsetning til andre flavivirus overført av mygg, er ikke mennesker involvert i overføring av TBE-viruset (naturlig syklus). Mennesker er sporadiske verter som utgjør en blindvei for syklusen, siden flåtten i dette tilfellet ikke vanligvis kommer tilbake til naturen etter blodmåltidet.
Overføring
De to periodene med maksimal overføring av TBE-viruset er slutten av våren (mai-juni) og slutten av sommeren (september-oktober), den varme og tørre sommeren er mindre gunstig for flått. Encefalitt tilfeller er funnet i den eksponerte menneskelige befolkningen en måned senere.
Hos mennesker beveger flåtten seg vanligvis opp bena for å nå et tynt, fuktig område av huden som er lettere å bite der den nestler seg, navlen, armhulen eller hårfestet i nakken. Etter en periode på 2 til 3 dager begynner flåtten sitt blodmåltid som varer 1 dag, deretter, mettet med blod, faller det til bakken.
Viruset overføres som oftest ved injeksjon av spytt fra bitt av infiserte flått. Dette spyttet har også en bedøvelseseffekt, bittet er smertefritt, og går vanligvis ubemerket. I endemiske områder i fare vil overføring av viruset være i størrelsesorden 1 av 200 bitt.
Kostholdsoverføring er mulig gjennom melk og upasteuriserte melkeprodukter fra infiserte dyr (noen få menneskelige tilfeller beskrevet i Polen , Slovakia og Estland ). Dette skjedde våren 2020 i Frankrike: rundt førti tilfeller ble identifisert i Ain, alt knyttet til inntak av rå melkgeitost fra samme produsent.
Overføring mellom mennesker, inkludert seksuell overføring, har aldri blitt dokumentert. Det er fortsatt teoretisk mulig (ved blodoverføring, ved amming, etc.), men har aldri blitt observert. Overføringer etter forurensede organtransplantasjoner er dokumentert.
Forekomsten av viruset i flått varierer fra sted til sted og fra tid til annen. I Østerrike og Sør-Tyskland bærer 1-3% av flått viruset, og i hardt berørte lokale områder i Litauen, Russland eller Sveits, opptil 10-30% av flått.
Risiko etter flåttbitt
I Sveits er risikoen for å utvikle flåttbåren encefalitt etter bitt mindre enn 1 av 1000. Etter flåttbitt i et endemisk område vil mellom en av 1000 og en av 5000 mennesker utvikle EVD med nevrologiske symptomer. Hos halvparten av voksne og 75% av barna vil denne nevrologiske svikt være forbigående meningitt.
Risikoen for å bli hardt rammet etter flåttbitt er derfor 1 av 10.000 voksne og 1 av 20.000 barn etter flåttbitt i en endemisk region. Risikoen for alvorlig EVD etter flåttbitt eksisterer, men er sjelden.
På grunn av sjeldenheten i alvorlige tilfeller er PCR-analyse av et laboratorium av flått fjernet fra en pasient for å demonstrere MEVE-viruset eller borrelia, ufortolkbar og ubrukelig.
Epidemiologi
TBE-viruset finnes bare i Eurasia , i ikke-tropiske skogsområder, fra Alsace-Lorraine til øya Hokkaidō i Japan. Denne fordelingen er ujevn, den forekommer i spredte foci som tilsvarer optimale levekår for flått og deres verter (små gnagere og stort vilt ). Dette er risikoområder og lommer med høy forekomst, hovedsakelig i og rundt skoger.
Det er ingen internasjonal definisjon av disse risikoområdene, hvis eksakte determinanter ikke er kjent. Disse utbruddene kan være regionale ( i det minste flere km 2 ) eller reduseres til lokale områder (opptil 500 m 2 ).
Antall tilfeller øker i de fleste land i europeiske land unntatt Østerrike.
innvirkning
Flåttbåren encefalitt er den viktigste europeiske arbovirussykdommen. Russland og Europa rapporterer rundt 10 000 saker årlig ( fra 5 000 til 13 000, avhengig av år). De høyeste forekomstene er funnet i det tidligere Sovjetunionen og de baltiske landene ( spesielt Latvia ), og står for mer enn halvparten av tilfellene. Så kommer de fra Sentral-Europa ( Polen , Tsjekkia , Slovakia , Ungarn , tidligere Jugoslavia ), Tyskland ( Bayern , Baden-Württemberg fremfor alt), Østerrike og Sveits. 10.000 tilfeller blir innlagt på verdensbasis hvert år, og dette tallet øker
Sammenlignet med befolkningen generelt, indikerer disse tallene for Den russiske føderasjonen i 2006, en landsgjennomsnittlig forekomst på 2,44 tilfeller per 100 000 innbyggere i gjennomsnitt, men 5 ganger mer i Sibir, og opptil 10 ganger avhengig av områdene i Sibir. I 2009 var forekomsten 6,89 i Litauen; 7,50 i Latvia; 9,90 i Slovenia; og 10.40 i Estland.
I Kina var dataene lite kjent, men nylige publikasjoner indikerer at i Nord-Kina ( Heilongjiang- provinsen ) er gjennomsnittlig forekomst av TBE 0,33 tilfeller per 100 000 innbyggere per år (periode 1980-1998), men med et hyperendemisk område ( Daxing'anling prefektur ) på 88,6 tilfeller per 100 000 innbyggere per år (periode 1990-1998).
I Frankrike, fra 1990 til 2005, ble det rapportert rundt førti tilfeller i avdelingene Alsace-Lorraine. Siden 2010-tallet har 7 til 20 tilfeller blitt diagnostisert hvert år. Det er en særlig høy forekomst i 2020 (mer enn førti tilfeller i Ain alene og i månedene april-mai), knyttet til grupperte tilfeller av flåttbåren encefalitt etter inntak av ost eller forurenset rå geitemelk.
Sykdommen rammet først godt identifiserte risikogrupper, profesjonelle eller semi-profesjonelle: landbruks- og skogbruksarbeidere, jegere, bærplukkere og undervekstsopp. Med økende turisme i skogsområder (turgåere, sport og utendørsaktiviteter, etc.), oppstår de fleste infeksjoner i fritiden, noe som gjør flåttbåren encefalitt til "en reisendes sykdom".
Det amerikanske og australske kontinentet er blottet for TBE- virus . Noen tilfeller kan oppstå når du kommer tilbake fra en tur. I USA ble det diagnostisert åtte tilfeller av TBE fra 2000 til 2017 ved retur fra Europa eller Kina.
Seroprevalens
Seroprevalensdata studier indikerer at i Tyskland og Østerrike, 4 til 8% av ikke-vaksinerte mennesker (i den generelle befolkning) som er tilstede spesifikke antistoffer, og har vært i kontakt med viruset (naturlig immunisering).
I Frankrike, blant fagfolk innen skogbruk (uvaksinert) i Grand Est-regionen , var denne prevalensen 3,4%, og blant loggere 17,5%.
Patofysiologi
Etter en flåttbitt og inokulering ved injeksjon av infisert spytt, multipliserer viruset lokalt for første gang i hudcellene, på bittstedet, og diffunderer deretter inn i blod og lymfesirkulasjon. Immunforsvar kan blokkere infeksjon på dette stadiet.
Ellers invaderer viruset flere organer og vev, spesielt retikuloendotel-systemet . Der multipliserer den igjen på en massiv måte, til virusbelastningen er tilstrekkelig til å krysse blod-meningealbarrieren . Etter invasjon av endotelcellene som utgjør denne barrieren, kan viruset nå sentralnervesystemet, spesielt gråstoffet . Det forårsaker en inflammatorisk reaksjon med spredning av gliaceller og vevsnekrose.
Under laboratorieforhold kan viruset reise gjennom nervenett for å nå sentralnervesystemet. For eksempel i laboratorieinfeksjoner av aerosoler, via neseslimhinnen og luktenerven .
I tilfeller av fordøyelsesspredning (ved inntak av forurenset rå melk) er inkubasjonen mye kortere (1 til 2 dager) enn ved flåttbitt.
Kliniske manifestasjoner
Det kliniske bildet av TBE avhenger av virusets virulens og pasientens status (alder, immunitet, genetikk, etc.). Alvorlighetsgraden av sykdommen varierer avhengig av subtypen som viruset tilhører. Fjerntypen er mer virulent enn den europeiske undertypen. Alvorlighetsgraden øker med alderen: barnet har mindre alvorlige former (hjernehinnebetennelse) enn pasienten over 40 år (encefalitt).
I endemiske regioner er det asymptomatiske (symptomløse) former som indikert av seroprevalensstudier .
I halvparten av tilfellene ble ikke begrepet flåttbitt funnet, det ble ikke engang lagt merke til av offeret.
Inkubasjon varer ofte 7 til 14 dager (rekkevidde 2 og 28 dager) etter flåttbitt. Det er en stille fase der viruset multipliserer lokalt.
Europeisk TBE
Den typiske sykdomsforløpet forårsaket av den europeiske undertypen er bifasisk. Etter en inkubasjonsperiode på omtrent en uke begynner den viremiske fasen, som varer en til ti dager, etterfulgt av en asymptomatisk fase på syv til ti dager, og til slutt, hos omtrent en tredjedel av pasientene, vises de første tegn på angrep.
Viremisk faseDen første kliniske fasen er viremisk , svarende til passasjen av viruset i den generelle sirkulasjonen. Anslagsvis 10 til 30% av de smittede manifesterer infeksjonen seg ved ikke-spesifikke tegn på influensasyndromstypen (tretthet, hodepine, kroppssmerter, utilpashed, feber ved 38 ° C og over) og fordøyelsessykdommer. Det varer fra 1 til 10 dager.
Dette er det eneste stadiet når viruset kan påvises i blodet. I omtrent to tredjedeler av tilfellene ender infeksjonen der, undertrykt av immunsystemet
Gratis intervallI nesten 35% av tilfellene blir ikke pasienten kurert spontant. Viruset går inn i en ny fase av duplisering i de forskjellige vev og organer som det har vært i stand til å nå. Denne fasen varer i gjennomsnitt en uke, det er også en fase med asymptomatisk remisjon, der pasienten ikke lenger har symptomer.
Nevrologisk faseDet er preget av passasjen av viruset i sentralnervesystemet. Det resulterer i en mer intens febergjenoppretting enn i den viremiske fasen.
Den hyppigste formen (50% av tilfellene som er rammet av den nevrologiske fasen) manifesterer seg som en klar flytende viral hjernehinnebetennelse (spesielt hos barn). I 40% av tilfellene som er rammet av den nevrologiske fasen, som meningo- encefalitt, inkludert lidelser som piriformis syndrom , cerebellar syndrom , forstyrrelser i hjernenerver . Halvparten av voksne pasienter utvikler encefalitt. Generelt, i europeisk TBE, er utviklingen av disse to formene gunstig.
Mer sjelden, i rundt 10% av tilfellene som er berørt av den nevrologiske fasen, dvs. 3% av den totale, manifesterer sykdommen seg også som myelitt (meningoencefalomyelitt), som også inkluderer slapp lammelse av øvre lem, spesielt av skuldermuskulaturen. ( skulderbelte ) med høy risiko for følgevirkninger.
Sykdommen varer fra noen dager til flere uker.
Kuren er uten oppfølger i 90% av tilfellene. Omtrent 1–2% av pasientene dør på dette stadiet, og 10–20% av ofrene har permanente nevrologiske følgevirkninger. En tredjedel av pasientene har resterende lidelser flere år etter sykdommen ( hodepine , sensoriske eller autonome lidelser, etc. som resulterer i post-encefalitt syndrom).
Dødsfall fra nevrologiske komplikasjoner er observert hos pasienter over 60 år.
Ikke-europeisk TBE
Fjernøsten undertype er preget av en fase i ett stykke (stille viremisk fase) som raskt utvikler seg til nevrologisk involvering, noen ganger med hemorragisk feber . Dødsfallet i saken er 20%, og opptil 60% av de overlevende har gjenværende nevrologiske følgevirkninger.
Den sibiriske undertypen er mellomliggende i alvorlighetsgrad mellom europeisk og fjernøstlig, med en dødsrate på 6% til 8%. Det er preget av hyppigere kroniske former.
Årsakene til disse forskjellene er dårlig kjent og diskutert: relatert til virusundertypen og dens virulens, genetisk mottakelighet hos pasienter, men også forskjeller i kriterier for valg av studerte pasienter (ingen internasjonal konsensus), tilgang til medisinske tjenester., Forskjeller i eksponering etter alder.
Langsiktig konsekvens
Tre kliniske evolusjoner kan identifiseres. Hos omtrent en fjerdedel av pasientene observeres fullstendig utvinning innen 2 måneder. Hos de resterende pasientene observeres enten langvarig, hovedsakelig kognitiv dysfunksjon eller vedvarende spinal nerveparese med eller uten andre postencefaliske symptomer. Opptil 46% av pasientene har permanente følgetilstand. De hyppigst rapporterte følgetilstandene er forskjellige kognitive eller nevropsykiatriske lidelser , balanseforstyrrelser , hodepine , dysfasi , hørselsforstyrrelser og spinal lammelse.
I Sveits har de under 16 år mindre alvorlige symptomer enn hos voksne og sjeldnere følgevirkninger (0,5% mot 5% av pasientene).
Diagnostisk
Siden de kliniske tegnene ikke er spesifikke, er diagnosen flåttbåren encefalitt en laboratoriediagnose.
I den første viraemiske fasen av sykdommen kan viruset påvises i blodkulturen . I løpet av den nevrologiske fasen kan viruset isoleres fra cerebrospinalvæske (CSL)
Kultur er vanskelig og forbeholdt spesialiserte laboratorier. Det har en tendens til å bli erstattet av polymerasekjedereaksjonen (PCR).
Anti- TBEV- antistoffer kan påvises tidlig i den nevrologiske fasen. Søket etter anti-TBE IgM, utført etter Elisa-metoden , utføres i serum og LCS; det gjør det mulig å skille mellom en pågående infeksjon og det serologiske sporet av en tidligere infeksjon som har gått ubemerket hen (IgG).
Behandling
Det er ingen spesifikk antiviral behandling, behandlingen er symptomatisk. Som regel blir pasienter innlagt på sykehus uten å bli isolert (fravær av menneske-til-menneskeoverføring). Støttende behandling så vel som intensivbehandling og assistert ventilasjon i alvorlige tilfeller kan være nødvendig.
Pasienter får gjenopplivingsbehandling basert på alvorlighetsgraden av manifestasjonene: smertestillende midler , febernedsettende midler (aspirin og NSAIDs anbefales ikke), vitaminer, hydrering og elektrolytter ; om nødvendig, antiemetika , krampestillende midler .
I alvorlige former med lammelse av luftveismusklene, eller i tilfelle hjerneødem , brukes behandlingen som tilsvarer komplikasjonen. For eksempel intubasjon og assistert ventilasjon for åndedrettslammelse.
Behandlinger etter eksponering med spesifikke immunglobuliner ble forlatt på begynnelsen av 2000-tallet på grunn av bivirkninger, men de fortsetter i Russland, som rapporterer om en viss beskyttende effekt.
I noen endemiske regioner, som Litauen, får pasienter som er rammet høye doser kortikosteroider. Denne behandlingen er basert på kliniske erfaringer med raske forbedringer i pasientenes tilstand. Imidlertid har eksisterende retrospektive studier ikke vist gunstige effekter av kortikosteroider i forhold til symptomatisk behandling.
Pasienter med revmatiske sykdommer behandlet med rituximab vil være i fare og vaksinen vil være ineffektiv.
Forebygging
I endemiske regioner er forebygging basert på pasteurisering av melken og, avhengig av risikonivå, på vaksinasjon.
For å unngå flåttbitt og infeksjon anbefaler eksperter følgende forholdsregler:
- unngå områder som er infisert av flått, spesielt i de varmeste månedene;
- ha på deg lyse klær slik at flått blir lettere sett. Bruk en lang skjorte, hatt, lange bukser og trekk sokkene opp over buksebenene;
- gå midt i stiene for å unngå gress og busker;
- sjekk kroppen din regelmessig for flått etter noen timer når du tilbringer mye tid utendørs i flåttinfiserte områder. Flått finnes oftest på lår, armer, armhuler og ben. Flått kan være veldig lite (ikke større enn et nålhode). Undersøk nøye eventuelle nye "fregner";
- bruke insekt avstøtende som inneholder DEET på huden eller permetrin på klær;
- umiddelbart trekke ut flått festet til huden.
Flått bør fjernes raskt og forsiktig med en pinsett og bruke jevn, mild trekkraft. flåttens kropp bør ikke knuses under ekstraksjonen, og pinsetten skal plasseres så nær huden som mulig for å unngå å etterlate biter av flåttens talerstol i huden. Flått skal ikke trekkes ut med bare hender. Hender skal beskyttes med hansker og / eller klut og vaskes grundig med såpe og vann og etter operasjonen. Denne manøveren skal utføres med stor forsiktighet.
Det er også spesifikke kroker ( flåttdragere ) tilgjengelig på apotek, slik at flått lett kan fjernes uten å forlate talerstolen.
Undersøkelser
En studie fra 2017 viste at hos mus infisert med kryssbåren encefalittvirus, kunne 90% beskyttelse oppnås ved injeksjon av en høy dose intravenøst immunglobulin som inneholder høyere titere. Virusspesifikke antistoffer, men ingen immunterapeutisk effekt ble observert hos mus behandlet med en dose immunglobulin uten virusspesifikke antistoffer. Denne studien antyder at injeksjon av en høy dose intravenøst immunglobulin som inneholder høye titre av spesifikke antistoffer mot viruset, kan representere profylakse etter eksponering eller en effektiv førstelinjebehandling av pasienter med en alvorlig form for viruset. Flåttbåren encefalitt.
Injeksjonen av monoklonale antistoffer rettet mot flåttbåren encefalittvirus hos mus har vist seg å være effektiv spesielt som en profylaktisk injeksjon, men også med en injeksjon en dag etter infeksjon.
Vaksinasjon
Historiske vaksiner
Allerede i 1937, noen måneder etter identifiseringen av " Vår-sommer encefalitt " -virus (verno-sommer encefalitt) i Sibir , ble det umiddelbart utviklet en militær vaksine for den røde armé . Det er den første vaksinen (i massebruk) mot et flavivirus, og den tredje vaksinen mot en virussykdom.
Denne vaksinen ble oppnådd fra en virussuspensjon (kultur på musens hjerne) inaktivert av formaldehyd . Denne vaksinen er effektiv, men med en høy grad av allergiske komplikasjoner på grunn av tilstedeværelsen av myelin i preparatet. Med fremkomsten av cellekulturer produserte sovjeterne andre vaksiner fra virus dyrket i kyllingembryoceller. Problemet med bivirkninger er redusert, men ikke løst.
Den første kinesiske vaksinen, som den sovjetiske, var tilgjengelig i 1953 for skogarbeidere nordøst i Kina.
Den første vaksineforskningen mot den europeiske undertypen begynte på 1960-tallet i Tsjekkoslovakia .
På 1970-tallet gjorde samarbeid mellom østerrikske og britiske institutter det mulig å utvikle en inaktivert vaksine som var ment å produseres kommersielt i store mengder. Denne vaksinen er også laget av cellekulturer av kyllingembryoer, men høyt renset i henhold til metoder introdusert i 1979.
Siden 1981 har Østerrike tilbudt massevaksinering mot flåttbåren encefalitt (ikke obligatorisk, men anbefales hver vår for barn over to år).
I 1999-2001 gjennomgikk denne østerrikske vaksinen flere modifikasjoner, blant annet for å oppfylle de nye europeiske anbefalingene knyttet til uttak av tiomersal fra vaksiner.
Nåværende vaksiner
På 2010-tallet ble fire vaksiner anerkjent som kvalitet og godkjent av WHO . De har det til felles at de er produsert på celler eller fibroblaster av kyllinger, inaktivert med formaldehyd, og at de bruker aluminiumhydroksyd som et hjelpestoff .
To er europeiske: den østerrikske vaksinen markedsført under navnet FSME-Immun (opprinnelig lisensiert i 1976 under navnet Ticovac) og den tyske vaksinen under navnet Encepur (lisensiert i 1994). Disse vaksinene har en pediatrisk formulering (barn over 1 år) og er tilberedt av europeiske virusstammer.
De to andre er russiske: TBE-Moskva-vaksinen og EnceVir-vaksinen, tilberedt fra stammer fra Østen.
I følge WHO er disse fire vaksinene trygge og effektive, russiske vaksiner har mindre data og er kontraindisert for barn under 3 år. De er utskiftbare da de tilsynelatende gir kryssbeskyttelse mot alle virale undertyper i omløp.
Det er også en andre generasjon kinesisk vaksine (utviklet i 2004, ved hjelp av hamsternyrecellekultur ) brukt i grenseområder i Nord-Kina.
Anbefalinger
WHOs anbefalinger er basert på nødvendig forkunnskap om sykdommen (overvåking, risikovurdering, kostnadseffektivitetsforhold, etc.). Basert på disse dataene, i svært endemiske land (pre-vaksinasjonsperiode), med minst 5 tilfeller per 100 000 innbyggere per år, anbefales generalisert vaksinasjon. I land med moderat eller lav risiko anbefales vaksinering for risikogrupper, eller fra sak til sak.
I alle tilfeller, i endemiske områder, må informasjon om sykdommen, vektorene og smitteformene, forebygging osv. Være lett tilgjengelig for publikum.
I 2008 hadde nesten 80 millioner vaksinedoser blitt brukt i Europa siden 1980. I Amerika er de to europeiske vaksinene bare tilgjengelige i Canada (som tilbyr dem som reisende vaksiner). Østerrike er det eneste landet som systematisk vaksinerer mot flåttbåren encefalitt siden 1981, med en vaksinasjonsgrad på 88% av befolkningen generelt i 2005.
For andre europeiske land varierer anbefalingene i henhold til den epidemiologiske situasjonen og risikovurderingen på regionalt / nasjonalt nivå. De vil sannsynligvis utvikle seg i henhold til endringer i situasjonen.
I Sveits anbefales vaksinasjon mot TBE i risikofylte situasjoner, fra fylte 6 år, i alle kantoner, unntatt de i Genève og Ticino .
I Frankrike, gitt den relativt sjeldne sykdommen, anbefales ikke generalisert vaksinasjon (i de avdelingene som er mest utsatt). Vaksinen er indikert fra sak til sak, hos mennesker i fare (landbruks- og skogbruksarbeidere, jegere, turgåere osv.). For reisende anbefales det turister i skogsområder, opp til 1500 m høyde, Sentral- og Øst-Europa, Skandinavia, Nord-Kina, Sør-Korea, Japan, Kirgisistan, Mongolia, Øst-Russland, i krysssesongen (februar til november).
I sterkt endemiske regioner, i skogsområder og i løpet av høysmissesesongen, anslås risikoen for at uvaksinerte reisende får sykdommen til 1 av ti tusen per måned. Risikoen blir ubetydelig hvis vi bor i et urbane eller ikke-skogsområde og uten å konsumere rå meieriprodukter.
Fremvekstfaktorer
Antall tilfeller øker i de fleste land i europeiske land unntatt Østerrike. Fra 1974 til 2003 økte forekomsten ti ganger i Tyskland, og fem ganger i Litauen. Ulike faktorer (biotisk og abiotisk) kan forklare fremveksten og / eller nylig spredning av flåttbåren encefalitt over hele Europa.
Forlengelsen synes å være mot nord og i høyde, avhengig av de skiftende temperatur- og fuktighetsforhold som er gunstige for huke populasjoner . Disse utvikler seg i beste fall ved en temperatur på over 7 ° C med en relativ luftfuktighet på over 80%. Disse forholdene finnes hovedsakelig i mikroboliger i skog og enger i regnperioder.
Den raske økningen i registrert siden slutten av XX th tallet tilsvarer delvis til bedre overvåking og bedre diagnostikk, men også, tilsynelatende på grunn av miljøendringer ( global oppvarming og écopaysager : landskapet fragmentering , introduserte arter eller krenkende , spredning av parasitter ved å øke bevegelse av mennesker og arter, etc.).
Global oppvarming
En svensk studie, publisert i 2001, viste en sammenheng mellom et mildere klima og en økning i tilfeller av TBE. Over 30 år, jo mildere klima, jo flere flått hadde vært og jo mer encefalitt hadde også vært. I Stockholms fylke har forekomsten av denne sykdommen økt dramatisk (tredobling) siden midten av 1980-tallet, med en topp i 1994 (tredobling av antall menneskelige tilfeller). Forskerne integrerte andre påvirkningsfaktorer (inkludert økningen i befolkningen som bor (i sommerhus ) i regioner der flått og sykdommen er endemisk i dag, og økning i dyrepopulasjoner som er vektorer for flått. Og / eller mikroben (faktor delvis knyttet sammen) Tilgang til vaksinasjon mot flåttbåren encefalitt i Sverige (siden 1986) og økt bevissthet om risikoen ved flått kan til og med ha ført til ytterligere undervurdering av årsak og virkning.
Sosiale og atferdsmessige faktorer
Global oppvarming alene kan imidlertid ikke forklare økningen i TBE-tilfeller, ifølge en studie fra de baltiske landene . Sosioøkonomiske parametere (økonomiske og atferdsmessige endringer etter Sovjetunionens fall) kan også være involvert.
Generelt er de nevnte sosiale faktorene fortrengning av populasjoner for forstadshabitater (i utkanten av skog), nye former for rekreasjon i skog, modifisering av landbrukspraksis, skogplanting .
Landskap og befolkningsøkologi
En studie utført i de italienske Alpene ( provinsen Trento ) så på mulige sammenhenger mellom økningen i menneskelige tilfeller av TBE, variasjoner i klima og skogstruktur, overflaten av flått og deres verter. Den beste forklaringsmodellen for økningen i forekomsten av sykdommen hos mennesker er den som integrerer endringer i skogstrukturen og spesielt forholdet mellom coppice / skoghøyde og tetthetsendringer i hjortebestanden (Capreolus capreolus ).
Forvaltningspraksis for jaktbar fauna ( agrainering av vilt, fangst eller jakt på rovdyr og store naturlige rovdyr) har sterkt favorisert virusets reservoararter (gnagere og hjort).
Ifølge en svensk studie ser økningen i menneskelige tilfeller ut til å korrelere med overfloden av Ixodes ricinus- flåtten i larvestadiet, som blir smittet hos gnagere før de får mat på hjort, for eksempel hjort. Antall hjort stoppet ikke med å vokse i flere tiår i Sverige før det gradvis gikk ned fra årene 1990 til 2010, noe som sannsynligvis tvang flått til å mate på gnagere som er de beste reservoarene for viruset. TBEV encefalitt, som sannsynligvis økte antallet infiserte voksne flått. og vektorer av sykdommen.
De to vintrene 2009 og 2011 var veldig kalde, noe som førte til at antallet hjortedyr falt og sannsynligvis ble videresendt flått på jakt etter måltider til russebukkene ( Myodes glareolus ) som plutselig hadde spredt seg på den tiden, snarere enn på hjort. 2011 var et veldig varmt år, som oppmuntret folk til å være oftere og lenger i de angrepne områdene, noe som kan forklare minst 284 menneskelige tilfeller av encefalitt i landet, et fenomen som kan vare på grunn av et uvanlig tidlig og varmt 2012-kryss årstid.
Tilpasning av flått til biocider
I tillegg, som mange andre organismer som står overfor biocider , har flått vist motstand mot akaricider , noe som tvinger oppdrettere og skadedyrprodusenter til å lete etter nye plantevernmidler , noe som er dyrt. Alternative strategier søkes. Den massive bruken av insektmidler eller akaricider på husdyr og husdyr kan også bidra til å styrke flåttenes evne til å overvinne denne barrieren.
Bibliografi
- Xavier Haller, flåttbåren meningoencefalitt (doktoravhandling), Strasbourg, University Louis Pasteur,1992( les online ).
- (i) Stanley A. Plotkin ( red. ) og P. Noel Barrett, Vaccines , Philadelphia, Saunders Elsevier,2008, 1725 s. ( ISBN 978-1-4160-3611-1 , leses online ) , kap. 32 (“Tick-borne encefalittvirusvaksiner”) , s. 841-856.
- WHO, “ Briefing Note: WHO Position on Tick-borne Encefalitis Vaccines ,” Weekly Epidemiological Record , Vol. 86, n o 2410. juni 2011, s. 241-256. ( les online ).
- Philibert Mougel, flåttbåren meningoencefalitt (doktoravhandling i farmasi), Nancy, Université Henri Poincaré Nancy 1,2011( les online ).
Merknader og referanser
- (no) Denne artikkelen er delvis eller helt hentet fra Wikipedia-artikkelen på engelsk med tittelen " Tick-borne encefalitt " ( se listen over forfattere ) .
- (no) Kaiser R, " Tick-borne encefalitt " , Infect. Si. Clin. North Am. , Vol. 22, n o 3,september 2008, s. 561–75, x ( PMID 18755391 , DOI 10.1016 / j.idc.2008.03.013 , les online )
- Stanley A. Plotkin 2008 , s. 841-842.
- Xavier Haller 1992 , s. 15-17.
- Kentaro Yoshii , Joon Young Song , Seong-Beom Park og Junfeng Yang , “ Tick-borne encefalitt i Japan, Republikken Korea og Kina ”, Emerging Microbes & Infections , vol. 6, n o 9,september 2017, e82 ( ISSN 2222-1751 , PMID 28928417 , PMCID 5625319 , DOI 10.1038 / emi.2017.69 , les online , åpnet 10. september 2019 )
- Eric Menot, " Central European tick encephalitis ", La Revue du Praticien - Médecine générale , vol. 9, n o 319,27. november 1995, s. 42-46.
- Jean-Louis Camicas, “ Tiques et arbovirus ”, Cahiers ORSTOM Medical entomology and parasitology , vol. 16, n o to1978, s. 166-167 ( les online )
- Charrel, RN; Attoui, H; Butenko, AM; Clegg, JC; Deubel, V, et al. Flåttbårne virussykdommer av menneskelig interesse i Europa . Klinisk mikrobiologi og infeksjon. 2004; 10: 1040–1055. [PubMed]
- Gritsun, TS; Nuttall, PA; Gould, E. Flåttbårne flåttvirus . Fremskritt innen virusforskning. 2003; 61: 317–371. PubMed
- Gérard Duvallet, medisinsk og veterinær entomologi , Quae - IRD,2017( ISBN 978-2-7099-2376-7 ) , s. 580-582.
- WHO 2011 , s. 242-243.
- (en) Anna Michelitsch , Kerstin Wernike , Christine Klaus and Gerhard Dobler , “ Exploring the Reservoir Hosts of Tick-Borne Encefalitis Virus ” , Viruses , vol. 11, n o 7,juli 2019( PMID 31336624 , DOI 10.3390 / v11070669 , lest online , åpnet 6. september 2019 )
- WHO 2011 , s. 244-245.
- WHO 2011 , s. 253.
- (i) Jarmo Oksi , Derrick Crook og Uga Dumpis , " Tick-Borne Encefalitis " , Clinical Infectious Diseases , vol. 28, n o 4,1 st april 1999, s. 882–890 ( ISSN 1058-4838 , DOI 10.1086 / 515195 , lest online , åpnet 7. september 2019 )
- Stanley A. Plotkin 2008 , s. 843-844.
- Patrice Bourée, " Tick-borne encephalitis ", La Revue du Praticien - Médecine générale , vol. 21 n o 790,4. desember 2007, s. 1152-1153.
- Thomas Krech, “ Verno-summer meningoencephalitis ”, Swiss Medical Forum , nr . 6,2006, s. 268-274 ( les online )
- “ Fokus på flåttbårne encefalitttilfeller knyttet til inntak av rå melkgeitost i Ain. Oppdater 19. juni 2020. ” , på www.santepubliquefrance.fr (åpnet 23. juni 2020 )
- (i) Dariusz Lipowski Marta Popiel , Karol Perlejewski og Shota Nakamura , " A Cluster of Fatal Tick-borne Encefalitis Virus Infection in Organ Transplant Setting " , The Journal of Infectious Diseases , vol. 215, n o 6,15. mars 2017, s. 896–901 ( ISSN 0022-1899 , DOI 10.1093 / infdis / jix040 , leses online , åpnes 27. mai 2020 )
- (in) Suss J, " Tick-borne encefalitt i Europa og utover - den epidemiologiske statusen fra 2007 " , Euro Surveill. , vol. 13, n o 26juni 2008( PMID 18761916 , les online )
- (in) Kunze U, " Tick-borne encefalitt: fra epidemiologi til vaksinasjonsanbefalinger i 2007. Nye problemer - beste praksis " , Wien Med Wochenschr , vol. 157 n bein 9-10,2007, s. 228–32 ( PMID 17564770 , DOI 10.1007 / s10354-007-0424-8 , les online )
- “ Tickborne Encefalitt - Kapittel 4 - 2020 Gul bok | Reisendes helse | CDC ” , på wwwnc.cdc.gov (åpnet 5. september 2019 )
- J. Gaudelus , " Flåttbåren meningoencefalitt hos barn ", Pediatrics Archives , pediatriske zoonoser: Hva er nytt i 2008? 24th Annual Days of the Pediatric Infectious Pathology Group, vol. 16,1 st oktober 2009, S108 - S114 ( ISSN 0929-693X , DOI 10.1016 / S0929-693X (09) 75312-6 , les online , åpnet 28. mai 2020 )
- (in) " TBE " , på www.santepubliquefrance.fr (åpnet 5. september 2019 )
- " Tick-borne sykdommer i Frankrike " , på has-sante.fr ,juni 2018
- " Seroprevalens av borreliose og flåttbåren encefalitt i profesjonelle presentasjoner i det store øst " på santepubliquefrance.fr (åpnet 9. september 2019 )
- Netgen , " Tick-borne encefalitt: første urbefolkning og epidemiologisk overvåking i kantonen Valais " , på Revue Médicale Suisse (åpnet 28. mai 2020 )
- (i) Gritsun Ts og Lashkevich Go , " Tick-borne encephalitis " på Antiviral forskning , januar 2003 ( PMID 12615309 , vist 28 mai 2020 )
- (en) Lindquist L og Vapalahti O , " Tick-borne Encefalitis " , på Lancet (London, England) ,31. mai 2008( PMID 18514730 , åpnet 28. mai 2020 )
- (in) Kaiser R , " The Clinical and Epidemiological Profile of Tick-Borne Encefalitis in Southern Germany from 1994 to 1998: A Prospective Study of 656 pasients " on Brain: a Journal of Neurology 1999 November ( PMID 10545392 , åpnet 28. mai 2020 )
- WHO 2011 , s. 244-245.
- (in) Haglund M og Günther G , " Tick-borne Encefalitis - Pathogenesis, Clinical Course and Long-Term Follow-Up " on Vaccine ,1 st april 2003( PMID 12628810 , åpnet 28. mai 2020 )
- (i) Niccolò Riccardi Roberta Maria Antonello Roberto Luzzati og Joanna Zajkowska , " Tick-borne encefalitt i Europa: en kort oppdatering om epidemiologi, diagnose, forebygging og behandling " , European Journal of Internal Medicine , vol. 62,1 st april 2019, s. 1–6 ( ISSN 0953-6205 , DOI 10.1016 / j.ejim.2019.01.004 , les online , konsultert 27. mai 2020 )
- CMIT, E. Pilly smittsomme og tropiske sykdommer 2018 , Paris, Alinéa Plus,2017, 720 s. ( ISBN 978-2-916641-66-9 ) , kap. 100 ("Arbovirus"), s. 493.
- Petra Bogovic og Franc Strle , “ Tick-borne encefalitt: En gjennomgang av epidemiologi, kliniske egenskaper og ledelse ”, World Journal of Clinical Cases: WJCC , vol. 3, n o 5,16. mai 2015, s. 430–441 ( ISSN 2307-8960 , PMID 25984517 , PMCID 4419106 , DOI 10.12998 / wjcc.v3.i5.430 , les online , åpnet 7. september 2019 )
- (in) JF Valarcher, " Tick borne encefalitt " , Scientific and Technical Review of the Office International des Epizooties , vol. 34, n o to2015, s. 453-466. ( les online )
- WHO 2011 , s. 254 og 256.
- (en) Wengse C og Ericsson J , " [Rapid Improving of Tick-Borne Encefalitis After Treatment With Corticosteroids] " , på Lakartidningen ,16. juni 2017( PMID 28632298 , åpnet 27. mai 2020 )
- (i) Ann Knight , Karlis Pauksens , Gunnel Nordmark og Eva Kumlien , " Dødelig utfall av flåttbåren encefalitt hos to pasienter med revmatisk sykdom behandlet med Rituximab " , Rheumatology , Vol. 56, n o 5,1 st mai 2017, s. 855–856 ( ISSN 1462-0324 , DOI 10.1093 / reumatology / kew495 , lest online , åpnet 27. mai 2020 )
- (i) Jana Elsterova Martin Palus , Jana Sirmarova og Jan Kopecky , " Tick-borne encephalitis virus neutralization by high dose intravenous immunoglobulin " , Flått og flåttbårne sykdommer , vol. 8, n o to1 st februar 2017, s. 253–258 ( ISSN 1877-959X , DOI 10.1016 / j.ttbdis.2016.11.007 , les online , åpnet 27. mai 2020 )
- (in) Andrey Matveev Leonid Matveev Oleg Stronin og Ivan Baykov , " Karakterisering av nøytraliserende monoklonalt antistoff kontre flåttbåren encefalittvirus in vivo " , Vaccine , Vol. 38, n o 272. juni 2020, s. 4309–4315 ( ISSN 0264-410X , DOI 10.1016 / j.vaccine.2020.04.051 , les online , åpnet 27. mai 2020 )
- Stanley A. Plotkin 2008 , s. 845-846.
- " Tick-borne encefalitt uttalelse " , på Public Health Agency of Canada , Canada Communicable Disease Report ,1 st april 2006(åpnet 7. september 2019 )
- Stanley A. Plotkin 2008 , s. 852.
- WHO 2011 , s. 246 og 250.
- WHO 2011 , s. 254-255.
- " Vaksinasjon mot flåttbåren encefalitt " , på health.belgium.be ,februar 2019(åpnet 10. september 2019 )
- Federal Office of Public Health FOPH , " meningoencefalitt i flått (TBE) " på www.bag.admin.ch (åpnet 10. september 2019 )
- " Tick-borne encefalitt " , på vaccination-info-service.fr (åpnet 9. september 2019 )
- Frankrike-informasjon - Flått er (allerede) tilbake: hva som fungerer for å forhindre bitt
- (in) Suss J, " Tick-borne encefalitt i Europa og utover - den epidemiologiske statusen fra 2007 " , Euro Surveill. , vol. 13, n o 26juni 2008( PMID 18761916 , les online )
- (in) Kunze U, " Tick-borne encefalitt: fra epidemiologi til vaksinasjonsanbefalinger i 2007. Nye problemer - beste praksis " , Wien Med Wochenschr , vol. 157 n bein 9-10,2007, s. 228–32 ( PMID 17564770 , DOI 10.1007 / s10354-007-0424-8 , les online )
- Stanley A. Plotkin 2008 , s. 843-844.
- E. Lindgren og R. Gustafson , “ Tick-borne encefalitt i Sverige og klimaendringer ”, Lancet (London, England) , vol. 358, n o 9275,7. juli 2001, s. 16–18 ( ISSN 0140-6736 , PMID 11454371 , DOI 10.1016 / S0140-6736 (00) 05250-8 , leses online , åpnet 8. september 2019 )
- Dana Sumilo , Loreta Asokliene , Antra Bormane og Veera Vasilenko , “ Climate Change Cannot Explain the Upsurge of Tick-Borne Encefalitis in the Baltics ”, PLoS ONE , vol. 2, n o 6,6. juni 2007( ISSN 1932-6203 , PMID 17551580 , PMCID 1876807 , DOI 10.1371 / journal.pone.0000500 , lest online , åpnet 8. september 2019 )
- G. CARPI , F. CAGNACCI , M. NETELER og A. RIZZOLI , “ Tick infestation on roe hjort i forhold til geografiske og eksternt oppdagede klimatiske variabler i et flåttbåren encefalitt endemisk område ”, Epidemiology and Infection , vol. 136, n o 10,oktober 2008, s. 1416–1424 ( ISSN 0950-2688 , PMID 18081949 , PMCID 2870723 , DOI 10.1017 / S0950268807000039 , lest online , åpnet 8. september 2019 )
- Thomas GT Jaenson , Marika Hjertqvist , Tomas Bergström og Åke Lundkvist , “ Hvorfor er tick-borne encephalitis økende? En gjennomgang av nøkkelfaktorene som forårsaker den økende forekomsten av menneskelig TBE i Swedena ”, Parasites & Vectors , vol. 5,31. august 2012, s. 184 ( ISSN 1756-3305 , PMID 22937961 , PMCID 3439267 , DOI 10.1186 / 1756-3305-5-184 , lest online , åpnet 8. september 2019 )
- Jones KE, Patel NG, Levy MA, Storeygard A., Balk D., Gittleman JL & Daszak P. 2008. Globale trender innen nye smittsomme sykdommer . Nature, 451, 990-U4
- Frisch JE. 1999. Mot en permanent løsning for bekjempelse av storfe . Int. J. Parasitol. 29: 57-71.
- Chevillon C. et al. 2007. Akkumulering av akaricidresistensmekanismer i Rhipicephalus microplus ( Acari : Ixodidae ) populasjoner fra Ny-Caledonia- øya . Veterinær. Parasitol. 147: 276-288
- Ghosh S., Azhahianambi P. & Yadav MP 2007. Kommende og fremtidige strategier for flåttkontroll : en gjennomgang. Journal of Vector Borne Diseases , 44, 79-89
- Pegram, RG, Tatchell RJ, de Castro JJ, Chizyuka HGB, Creek MJ, McCosker PJ, Moran MC & Nigarura G. 1993. Tick control: nye konsepter . Verdens animasjon. Rev. 74/75: 2-11.
Se også
Relaterte artikler
Eksterne linker
- France Lyme, Association for the fight against tick vector sykdommer .
- “ Studie av de 3 patologiene overført av flått i Alsace ” , på santepubliquefrance.fr (konsultert 9. september 2019 ) .
- " Hjelp til diagnostisering av feber etter flåttbitt " , på infectiologie.com ,april 2018.