Salpetersyre
| Salpetersyre | |
 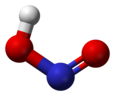  Struktur av cis og trans salpetersyre . |
|
| Identifikasjon | |
|---|---|
| IUPAC-navn |
salpetersyre hydrogen nitritt |
| N o CAS | |
| N o ECHA | 100.029.057 |
| N o EC | 231-963-7 |
| PubChem | 24529 |
| ChEBI | 25567 |
| SMIL |
N (= O) O , |
| InChI |
InChI: InChI = 1S / HNO2 / c2-1-3 / h (H, 2,3) InChIKey: IOVCWXUNBOPUCH-UHFFFAOYSA-N |
| Utseende | blekblå løsning |
| Kjemiske egenskaper | |
| Formel |
H N O 2 [Isomerer] |
| Molarmasse | 47,0134 ± 0,0009 g / mol H 2,14%, N 29,79%, O 68,06%, |
| pKa | 3,35 ved 25 ° C |
| Dipolar øyeblikk |
1,423 ± 0,005 D ( cis ) 1,855 ± 0,016 D ( trans ) |
| Elektroniske egenskaper | |
| 1 re ioniseringsenergi | ≤ 11,3 eV (gass) |
| Enheter av SI og STP med mindre annet er oppgitt. | |
Den salpetersyrling er en kjemisk forbindelse med formel HNO 2. Det er en svak mono syre som bare er kjent i en løsning som ikke er altfor surt (det dismutes ved lav pH-verdi), og i gassfasen. Dens salter ( nitritter ) er stabile i vandig løsning. Salpetersyre er en av de essensielle reagensene ved fremstilling av azofargestoffer. Den blir deretter fremstilt in situ ved forsuring av natriumnitritt ved lav temperatur (ca. 5 ° C).
Den HNO 2 molekylble oppdaget i det interstellare mediet i B-komponenten i det binære systemet IRAS 16293−2422 (en) .
Beskrivelse
Det systematiske navnet er: dioksonitronsyre (III) eller salpetersyre III . Saltene kalles nitritter .
Det er spesielt ustabilt og oppløses ved romtemperatur i nitrogenmonoksid NO og nitration [NO 3 ] -Og viser Frost-diagrammet over nitrogen gitt nedenfor:

Nitrogen, som er i + III oksidasjonstilstand , blir funnet, etter disproporsjonering , i + V og + II tilstandene.
Salpetersyre brukes til å fremstille azoderivater ( azobensen C 6 H 5 –N = N - C 6 H 5) Fra aromatiske aminer , via diazoniumsalter C 6 H 5 -N + ≡N · X -.
Hans pK a er 3,3.
Den tilberedes samtidig fordi den er for ustabil til å lagres ved å tilsette saltsyre til natriumnitritt i oppløsningen:
NO 2 - (aq)+ H 3 O +→ HNO 2 (aq)+ H 2 O (væske).Se også
Merknader og referanser
- (in) David R. Lide, håndbok for kjemi og fysikk , CRC,16. juni 2008, 89 th ed. , 2736 s. ( ISBN 142006679X og 978-1420066791 ) , s. 9-50
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- (in) David R. Lide, håndbok for kjemi og fysikk , CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- (i) A. Coutens, NFW Ligterink, BC Loison, V. Wakelam, H. Calcutt, MN Drozdovskaya JK Jørgensen, HSP Müller, EF van Dishoeck og SF Wampfler , " ALMA PILS-undersøkelsen: Første påvisning av salpetersyre (HONO ) in the interstellar medium ” , Astronomy & Astrophysics , vol. 623, mars 2019, Artikkel n o L13 ( DOI 10,1051 / 0004-6361 / 201935040 , bibcode 2019A og A ... 623L..13C , arxiv 1903,03378 , lese online )