Nitrogenperoksid
| Nitrogenperoksid | |||
 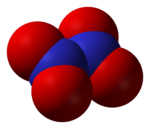 Struktur av nitrogenperoksid. |
|||
| Identifikasjon | |||
|---|---|---|---|
| IUPAC-navn | Nitrogen tetraoxide | ||
| N o CAS | |||
| N o ECHA | 100.031.012 | ||
| N o EC | 234-126-4 | ||
| N o RTECS | QW9800000 | ||
| PubChem | 25352 | ||
| ChEBI | 29803 | ||
| SMIL |
[N +] (= O) ([N +] (= O) [O -]) [O-] , |
||
| InChI |
InChI: InChI = 1S / N2O4 / c3-1 (4) 2 (5) 6 InChIKey: WFPZPJSADLPSON-UHFFFAOYSA-N |
||
| Utseende | fargeløs væske | ||
| Kjemiske egenskaper | |||
| Brute formel |
N 2 O 4 [Isomerer] |
||
| Molarmasse | 92,011 ± 0,0016 g / mol N 30,45%, O 69,55%, |
||
| Fysiske egenskaper | |||
| T ° fusjon | −9,3 ° C | ||
| T ° kokende | 21,15 ° C | ||
| Løselighet | reagerer med vann | ||
| Volumisk masse | 1,45 g · cm -3 til 20 ° C | ||
| Kritisk punkt | 431 K ; 10,1 MPa ; 167 cm 3 · mol -1 | ||
| Termokjemi | |||
| Δ vap H ° | 38,12 kJ · mol -1 ( 1 atm , 21,15 ° C ) | ||
| Forholdsregler | |||
| SGH | |||
    Fare H270, H280, H314, H330, P220, P260, P280, P284, P310, P305 + P351 + P338, H270 : Kan forårsake eller forsterke brann; oksidasjonsmiddel H280 : Inneholder gass under trykk; kan eksplodere ved oppvarming H314 : Gir alvorlig etseskader på huden og øyeskader H330 : Dødelig ved innånding P220 : Oppbevares / oppbevares vekk fra klær / ... / brennbare materialer P260 : Ikke pust støv / røyk / gasser / tåke / damp / aerosoler. P280 : Bruk vernehansker / verneklær / øyevern / ansiktsbeskyttelse. P284 : Bruk åndedrettsvern. P310 : Kontakt et GIFTINFORMASJONSSENTER eller lege. P305 + P351 + P338 : Ved øyne: Skyll forsiktig med vann i flere minutter. Fjern kontaktlinser hvis offeret bruker dem og de lett kan fjernes. Fortsett å skylle. |
|||
| WHMIS | |||
|
Uklassifisert produktKlassifiseringen av dette produktet har ennå ikke blitt validert av Toxicological Directory Service Disclosure på 1,0 % i henhold til listen over ingredienser |
|||
| Transportere | |||
265 : giftig og oksiderende gass (fremmer brann) FN-nummer : 1067 : NITROGEN DIOXIDE; eller DIAZOTE TETROXIDE Klasse: 2.3 Etiketter: 2.3 : Giftige gasser (tilsvarer grupper betegnet med store bokstaver T, dvs. T, TF, TC, TO, TFC og TOC). 5.1 : Oksiderende stoffer 8 : Etsende stoffer    |
|||
| Enheter av SI og STP med mindre annet er oppgitt. | |||
Den nitrogendioksid eller dinitrogentetroksyd , er en kjemisk forbindelse med formel N- 2 O 4. Det er en fargeløs til gulbrun væske avhengig av konsentrasjonen av nitrogendioksid NO 2den inneholder: N 2 O 4er i likevekt med NO 2, hvorav det faktisk er en dimer . Det er en veldig kraftig, etsende og giftig oksidant . Også kalt NTO (fra engelsk Nitrogen TetrOxide) i astronautikk , er nitrogenperoksid en oksidasjonsmiddel som er mye brukt, spesielt med hydrazin og dets derivater for å danne lagringsbare hypergoliske flytende drivmidler .
Egenskaper og struktur
Strukturen til dette molekylet ble mye diskutert til slutten av 1940-tallet, da vi begynte å forstå det, akkurat som den for nitrogentrioksid . N 2 O 4- molekyleter plan, med en NN-binding på 178 µm og en NO-binding på 119 µm . I motsetning til NO 2- molekylet, N 2 O 4 dimerer diamagnetisk .
På 1940-tallet ble det også vist at i flytende form, i motsetning til ammoniakk NH 3eller svoveldioksid SO 2, dette mediet var ikke befordrende for de uorganiske reaksjonene som i utgangspunktet skulle være mulig ved ionisering av mediet. Oppløselige mineralsalter i denne væske ble ikke funnet på tiden, og gitt den høye oppløseligheten av mange organiske forbindelser, kjemikere så konkludert med at denne væske hadde en ikke-ioniserende karakter og en oppførsel som minner om den for oppløsningsmidler. Organisk, slik som benzen C 6 H 6.
Under normale temperatur- og trykkforhold , og under likevekt mellom nitrogenperoksyd N 2 O 4og nitrogendioksid NO 2, er de to artene alltid til stede samtidig, økningen i temperatur forskyver likevekten til denne endotermiske reaksjonen mot dioksidet ved dissosiasjon av dimeren:
N 2 O 4 2 NO 2 : Ah = 57,23 kJ · mol -1 .Forberedelse
Nitrogen peroksyd fremstilles ved katalysert oksydasjon av ammoniakk NH 3i vanndamp H 2 Ofor å begrense temperaturen, noe som gjør det mulig å oksidere nitrogenmonoksid N20 til nitrogendioksid NO 2mens vannet slippes ut i form av salpetersyre HNO 3 ; restgassen er i det vesentlige sammensatt av nitrogenperoksyd, som deretter er tilstrekkelig til å avkjøles.
Astronautisk bruk
Nitrogenperoksid er et av de viktigste drivstoffene som brukes i dag i romfremdrift . Den erstattet den første salpetersyren som ble brukt som forbrenning av drivmidler fra rakettmotorer , med drivstoff som RP-1 , UDMH eller MMH . Motorene ble beskyttet mot surheten i oksidasjonsmidlet ved tilsetning av 0,6% hydrogenfluorid HF, ganske kostbart, veldig giftig og farlig håndtering. Salpetersyre ble erstattet av andre oksidasjonsmidler, særlig nitrogenperoksid, så tidlig som på 1990-tallet. Romskyttere og ballistiske missiler begynte å bruke det på slutten av 1950 - tallet , da USAs stater og Sovjetunionen valgte det som oksidantdannende med hydrazin og dets derivater. - hydrazinhydrat , MMH , UDMH , aerozin 50 og UH 25 hovedsakelig - av flytende drivmidler som kan lagres hypergolisk .
Kalt NTO (for dinitrogentetraoksid ) i sammenheng med plass fremdrift , er nitrogen peroksyd det mest brukte oksydasjonsmiddel hypergolic motorer . Som sådan, er det brukt på et stort antall lavere trinn utformet i 1960 som den russiske Proton bærerakett , den Fregat stadium av russiske Soyuz og Zenit bæreraketter, og den kinesiske Long March raketter . Det ble erstattet på disse trinnene med flytende oksygen på bæreraketter designet senere. Det brukes veldig ofte i de øverste etasjene som opprettholder til tross for deres toksisitet hypergoliske drivmidler, fordi de er enkle å lagre i tankskyttere og tillater flere antennelser som orbitale manøvreringsmotorer (OMS) i romfergen til NASA , Ariane 5, lagringsbart drivstoffstadium ( EPS) , eller den indiske GSLV- bæreraketten , motorene som lar romtaster bli satt inn i bane osv.
Når det brukes som drivmiddeloksidant (oksidant), blandes nitrogenperoksyd vanligvis med en liten prosentandel nitrogenmonoksid N20 for å begrense korroderende effekter på legeringer av titan som er involvert i fremdriftssystemet til romfartøy : dette kalles MON (for blandede oksider av Nitrogen ); HVEM av romfergen bruker for eksempel MON-3, ved 3 % N≡O (vektfraksjon).
Syntese
Ved brenning av kobbernitrat + bly (II) nitrat , nitrogendioksid og nitrogen peroksyd vises.
Toksisitet, økotoksisitet
Den toksisitet av inhalerte nitrogen peroksyd er kjent og har vært studert i laboratoriedyr.
Det oppstår fra sin oksiderende natur , som har direkte effekter på celler, men også effekter av hormonforstyrrelse . Kinesiske militærforskere har vist at nitrogenperoksid spesielt påvirker visse faktorer produsert av høyre atrium i hjertet (hormonelle faktorer som regulerer blodtrykket ). Disse samme forskerne har vist at andre regulatoriske faktorer (kalt natriuretika ), polypeptider ( Atrialt natriuretisk polypeptid eller ANP) produsert av lungene , og som er tilstede i lungeslim , også ble forstyrret.
Merknader og referanser
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- "Nitrogen Tetroxide" i databanken for farlige stoffer , åpnet 11. juni 2010
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Innbundet ( ISBN 978-1-4200-9084-0 )
- Indeksnummer i tabell 3.1 i vedlegg VI til EF-forskrift nr. 1272/2008 (16. desember 2008)
- SIGMA-ALDRICH
- " Nitrogen tetroxide " i databasen over kjemikalier Reptox fra CSST (Quebec-organisasjonen som er ansvarlig for arbeidsmiljø og helse), åpnet 25. april 2009
- "Dinitrogen tetraoxide" , på ESIS , åpnet 11. juni 2010
- JS BROADLEY & J. MONTEATH ROBERTSON Structure of Dinitrogen Tetroxide nature 164, 915-915 1949/11/26; doi: 10.1038 / 164915a0
- CK INGOLD & E. HILDA INGOLD [Konstitusjoner av dinitrogentetroksid og trioksid] Nature 159, 743-744; Dato 1947/05/31; doi: 10.1038 / 159743b0
- Holleman, AF; Wiberg, E. "Inorganic Chemistry" Academic Press, 2001, San Diego. ( ISBN 978-0-12-352651-9 ) .
- W. ROGIE ANGUS, RICHARD W. JONES & GLYN O. PHILLIPS Eksistens av nitrosylioner (NO +) i dinitrogentetroksid og av nitroniumioner (NO2 +) i flytende dinitrogenpentoksid- natur 164, 433-434 (1949/11/10 ); doi: 10.1038 / 164433aZ
- CC ADDISON & R. THOMPSON Ioniske reaksjoner i flytende dinitrogen tetroksid ; natur 162, 369-370 (1948/11/04); doi: 10.1038 / 162369a0
- YE Ming Liang, XIA Ya Dong, WEN Si Zhen, GUO Xu Yi; [Endring i atrielt natriuretisk faktorinnhold hos rotter som led av akutt lungeødem indusert av dinitrogentetroksid]; (Institute of Pharmacology and Toxicology, Academy f Military Medical Sciences, Beijing 100850) ( Tilgang til artikkelen , på kinesisk)
- [Effekt av dinitrogentetroksid på atrielt natriuretisk polypeptid og lungesurfaktivt middel i rotter Ye Mingliang], Wu Haihuan, Peng Liyi et al. ; Institutt for farmakologi og toksikologi, Academy of Military Medical Sciences, Beijing 100850 ( lenke til originalartikkel (kinesisk), abstrakt .
