Perklorsyre
| Perklorsyre | |||
 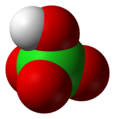 Struktur av perklorsyre. |
|||
| Identifikasjon | |||
|---|---|---|---|
| IUPAC-navn |
Perklorsyre hydrogenperklorat |
||
| N o CAS | |||
| N o ECHA | 100.028.648 | ||
| N o EC | 231-512-4 | ||
| Utseende | fargeløs væske med en skarp lukt | ||
| Kjemiske egenskaper | |||
| Brute formel |
H Cl O 4 [Isomerer] |
||
| Molarmasse | 100.459 ± 0,003 g / mol H 1%, Cl 35,29%, O 63,71%, |
||
| pKa | ≈ −8 | ||
| Fysiske egenskaper | |||
| T ° fusjon | −112 ° C | ||
| T ° kokende | (spaltning): 19 ° C | ||
| Løselighet | i vann: blandbar | ||
| Volumisk masse | 1,76 g · cm -3 til 22 ° C | ||
| Forholdsregler | |||
| SGH | |||
   Fare H271, H319, H373, P260, P305 + P351 + P338, P370 + P378, P371 + P380 + P375, H271 : Kan forårsake brann eller eksplosjon; sterk oksidasjonsmiddel H319 : Forårsaker alvorlig øyeirritasjon H373 : Kan forårsake organskader (liste opp alle berørte organer, hvis kjent) etter gjentatt eller langvarig eksponering (angi eksponeringsvei hvis det er endelig bevist at ingen annen eksponeringsvei gir samme fare) P260 : Unngå innånding av støv / røyk / gass / tåke / damp / spray. P305 + P351 + P338 : Ved øyne: Skyll forsiktig med vann i flere minutter. Fjern kontaktlinser hvis offeret bruker dem og de lett kan fjernes. Fortsett å skylle. P370 + P378 : I tilfelle brann: Bruk ... til utryddelse. P371 + P380 + P375 : I tilfelle større brann og store mengder: evakuer området. Bekjemp ild på avstand på grunn av eksplosjonsfare. |
|||
| WHMIS | |||
   C, E, F, C : Oksiderende materiale forårsaker eller fremmer forbrenningen av et annet materiale ved å frigjøre oksygen E : Etsende materiale Transport av farlig gods: klasse 8 F : Farlig reaktivt materiale blir selvreaktivt under påvirkning av et støt. Avsløring ved 1, 0% i henhold til liste over ingredienser |
|||
| NFPA 704 | |||
| 0 3 3 OKSE | |||
| Transportere | |||
1873 : PERKLORSYRE som inneholder mer enn 50 prosent (masse), men ikke mer enn 72 prosent syre |
|||
| Enheter av SI og STP med mindre annet er oppgitt. | |||
Den perklorsyre er en kjemisk forbindelse med formel HClO 4Der atom av klor er på oksidasjonstilstanden + VII. Det er en oksosyre som kan sammenlignes i styrke med sterke syrer som salpetersyre og svovelsyre , samt et oksidasjonsmiddel . Den brukes spesielt til å produsere perklorater , hovedsakelig ammoniumperklorat , som brukes i sammensetningen av faste drivmidler som er mye brukt i astronautikk , spesielt PCPA . Perklorsyre er veldig etsende og danner lett eksplosive blandinger.
Beskrivelse
Det er en fargeløs væske, en sterk syre og en sterk oksidasjonsmiddel. Saltene kalles perklorater. Det er den eneste formen for klor som er stabil med hensyn til disproporsjonering i et basisk medium med kloridionet . Det kan være dehydrert til en meget ustabil Cl 2 O 7 perklorsyre anhydrid .
Syntese
Perklorat ioner syntetiseres ved elektrokjemisk oksydasjon av klorat- ioner og syren erholdt ved innvirkning av svovelsyre på dens salter.
Bruker
Perklorater er viktige forbindelser i pyroteknikken som oksygenbærer i blandinger. Perklorsyre kan brukes som motioner i oppløsning fordi flertallet av saltene er løselige i vann, noe som begrenser nedbørproblemene.
Se også
Relaterte artikler
Eksterne linker
- (fr) INRS-ark
- (en) Internasjonalt sikkerhetsdatablad
- ( fr ) Perklorater i amerikansk mat , miljøvitenskap og teknologi, 2008-02-13. (En annen FDA-studie gir gjennomsnitt, men inkluderer ikke populasjoner med høy risiko)
Bibliografi
- (en) Schilt, AA, 1979. Perklorsyre og perklorater . GFS Chemicals, Inc, Columbus.
- (en) Kirk-Othmer - Encyclopedia of chemical technology, 5. utg. Flygning. 18. Hoboken: John Wiley og sønner; 2006: 274-284.
- (en) Budavari S (red) - The Merck Index, 13. utg. NJ: Merck og Co. Inc; 2001.
- (no) Perklorsyre. I: HSDB-database. Canadian Center for Health and Safety, revisjon 14.02.2003. Tilgjengelig på http://www.tox-net.nlm.nih.gov .
- (no) Perklorsyre. Ark nr. 14. I: Cheminfo Data Base. Canadian Center for Health and Safety, revisjon 24.03.2003.
- (no) Brannbeskyttelsesguide for farlige materialer. NFPA (National Fire Protection Agency), 13 th ed.
- (no) Perklorsyreoppløsning. BGIA GESTIS-database om farlige stoffer. Tilgjengelig på http://www.hvbg.de/e/bia/gestis/stoffdb/index . html.
- (en) York RG et al. - Raffinering av effektene som er observert i en utviklingsmessig neurobehavioral studie av ammoniumperklorat administrert oralt i drikkevann til rotter. I. Skjoldbruskkjertel og reproduktive effekter. International Journal of toxicology, 2005; 24 (6): 403-418.
- (en) York RG et al. - Oral (drikkevann) utviklingstoksisitetsstudie av ammoniumperklorat hos New Zealand hvite kaniner. International Journal of Toxicology, 2001; 20 (4): 199-205.
- (en) Thuett KA et al. - Effekter av eksponering av ammoniumperklorat i livmoren og laktasjonen på skjoldbruskkjertelhistologi og skjoldbruskkjertel- og kjønnshormoner ved utvikling av hjortmus (peromyscus maniculatus) gjennom fødselsdagen 21. Journal of Toxicology and Environmental Health A, 2002; 65 (24): 2119-2130.
- (en) Forsberg K, Mansdorf SZ - Hurtigvalg guide til kjemiske beskyttelsesklær. New York: John Wiley and sons, 4. utg. ; 2002.
- (fr) Fartøy og reservoarer - Anbefaling CNAM R 435. Paris: INRS; 2008.
- (en) Leleu J, Triolet J - Farlige kjemiske reaksjoner. Paris: INRS ED 697; 2003: 15-18.
Referanser
- PERKLORSYRE (72% LØSNING) , sikkerhetsdatablad (er) fra det internasjonale programmet for kjemisk sikkerhet , konsultert 9. mai 2009
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Sikkerhetsdatablad utarbeidet av Sigma-Aldrich, konsultert 2. februar 2020 https://www.sigmaaldrich.com/MSDS/MSDS/DisplayMSDSPage.do?country=FR&language=fr&productNumber=208507&brand=SIAL&PageToGoToURL=https%2Fwww%2. sigmaaldrich.com% 2Fcatalog% 2Fproduct% 2Fsial% 2F208507% 3Flang% 3Dfr
- " Perklorsyre " i databasen over kjemikalier Reptox fra CSST (Quebec-organisasjonen som er ansvarlig for arbeidsmiljø og helse), åpnet 25. april 2009
