Luft
| Luft | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 28,965 g / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −216,2 ° C ( 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | −194,3 ° C ( 1 atm , 874,0 kg / m 3 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet | 0,0292 vol / vol (vann, 0 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
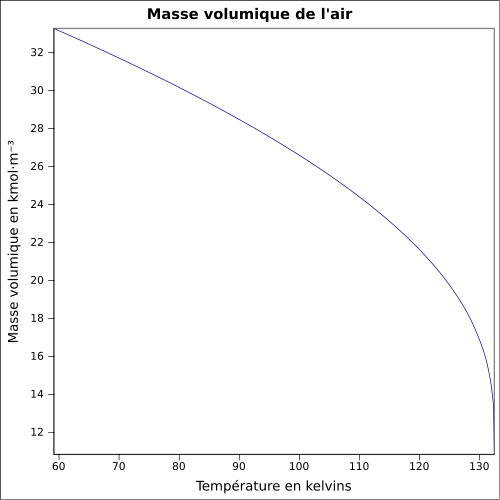
| Volumisk masse |
1,2 kg / m 3 ( 21,1 ° C , 1 atm )
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
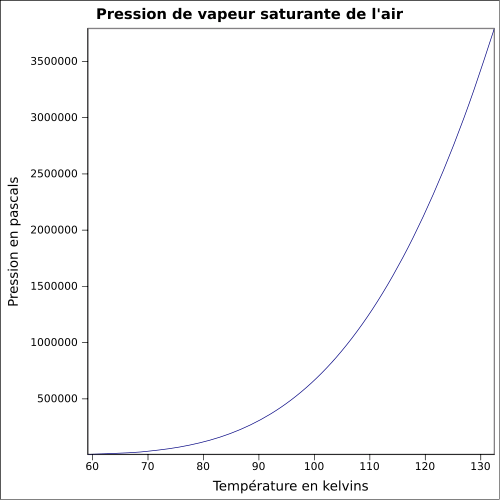
| Mettende damptrykk |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | -140,6 ° C , 3,771 kPa , 351 kg / m 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termisk ledningsevne | 0,023 4 W m −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
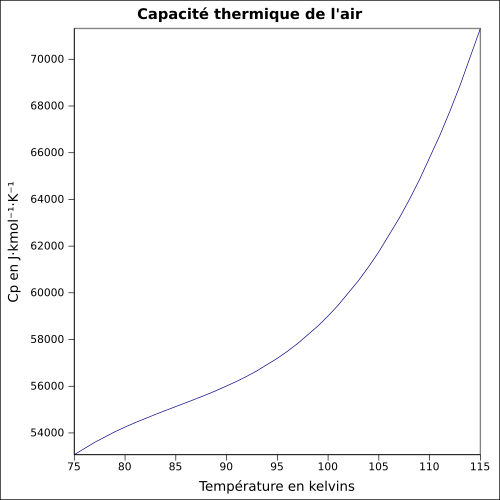
| C s |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brytningsindeks | 1.00026825 ( 100 kPa , tørr luft med 450 ppm CO 2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den luft er en blanding av gasser som utgjør atmosfæren på jorden . Det er normalt fargeløst, usynlig og luktfritt.
Sammensetning
Tørr luft nær bakken er en homogen gassblanding. Den består omtrent av molfraksjon eller volum av:
- 78,08% nitrogen ;
- 20,95% oksygen ;
- mindre enn 1% av andre gasser inkludert:
- edelgasser , hovedsakelig:
- av karbondioksid (CO 2) ~ 0,04% (415 ppmv inApril 2021),
- av metan 0,000187% (1,87 ppmv i 2019).
Den inneholder også spor av 0,000072% dihydrogen (0,72 ppmv ), men også ozon , samt en minimal tilstedeværelse av radon . Det kan også inneholde svoveldioksid , nitrogenoksider , fine suspenderte stoffer i aerosolform , støv og mikroorganismer.
Mesteparten av tiden er luften i jordens miljø fuktig fordi den inneholder vanndamp . Nær bakken er mengden vanndamp veldig variabel. Det avhenger av klimatiske forhold, og spesielt av temperatur. Den partielle trykket av vanndamp i luften er begrenset av dens mettede damptrykk som varierer med temperatur:
| Lufttemperatur | −10 ° C | 0 ° C | 10 ° C | 20 ° C | 30 ° C | 40 ° C |
| % vanndamp
for et lufttrykk på 1013 hPa |
0 til 0,2% | 0 til 0,6% | 0 til 1,2% | 0 til 2,4% | 0 til 4,2% | 0 til 7,6% |
Prosentandelen av vanndamp som er tilstede i luften måles av fuktighetsgraden , det er et viktig element for værmeldinger. Det er flere mengder for å beskrive hydrometri: absolutt fuktighet , som tilsvarer massen av vanndamp per volum luft; og relativ fuktighet , som er prosentandelen av vanndampens delvise trykk i forhold til det mettede damptrykket .
Nivået av karbondioksid varierer over tid. På den ene siden gjennomgår den en årlig endring på amplituden på ca. 6,5 ppmv ( p ection p ar m illion in v olume). På den annen side øker den gjennomsnittlige årlige hastigheten med 1,2 til 1,4 ppmv per år. I størrelsesorden 384 ppmv (0,0384%) i midten av 2008 var det 278 ppmv før den industrielle revolusjonen , 315 ppmv i 1958, 330 ppmv i 1974 og 353 ppmv i 1990. Dette drivhusgassdrivhuset spiller en viktig rolle i global oppvarming av planeten.
Den metan er en annen gass største drivhus hvis hastighet øker med tiden: 800 mm 3 / m 3 (0,8 ppmv ) i pre-industriell era, 1585 mm 3 / m 3 1 985, 1663 mm 3 / m 3 i 1992 og 1676 mm 3 / m 3 i 1996.
Opptil 80 km høyde er sammensetningen av tørr luft veldig homogen, den eneste signifikante variasjonen i sammensetningen av luften er den for vanndampinnholdet.
Luftsammensetning
|
|
||||||||||||||||||||||||||||||||||||||||||||
Masseforholdene kan evalueres ved å multiplisere volumforholdene med forholdet mellom molær masse av gassen som er vurdert delt på molær masse av luft, dvs. 28,976 g mol -1 , for eksempel når det gjelder CO 2. Dette forholdet er ikke ubetydelig, siden det er lik 44 / 28,976 = 1,5185, derav masseinnholdet av CO 2i luft lik 415 × 1,5185 = 630 ppmm .
Volumisk masse
Siden luft er en komprimerbar gass, er densiteten (i kg / m 3 ) en funksjon av trykk, temperatur og fuktighet.
For tørr luft ved normalt atmosfærisk trykk ( 1013,25 hPa ):
Vanligvis tar 1,293 kg / m 3- for å 0- ° C og 1,204 kg / m 3- for å 20 ° C .
Dette er generalisert ( ideell gassformel ) i: (med T i kelvin og P i pascal i henhold til SI-konvensjonene). For en temperatur θ i grader Celsius oppnås temperaturen T i kelvin ved å legge 273,15 til θ : T (K) = θ (° C) + 273,15 .
Globalt oppvarmingspotensial
Det globale oppvarmingspotensialet (GWP på engelsk : GWP: Global Warming Potential ) eller tilsvarende CO 2gjør det mulig å måle ”skadeligheten” til hver klimagass .
Følgende tabell gir verdien av GWP for de viktigste klimagassene som er tilstede i luften:
| PRG | 1 (referanse) | 8 | 23 | 310 | fra 1300 til 1400 | fra 6 200 til 7 100 | 6500 | 22 800 |
| gass | karbondioksid | Vann damp | metan | lystgass (N 2 O) | klordifluormetan (HCFC) | diklordifluormetan (CFC) | karbontetrafluorid (CF 4 ) | svovelheksafluorid (SF 6 ). |
Brytningsindeks
Uttrykket for brytningsindeks for luft "ved standardforhold" er:
med hvor er bølgelengden uttrykt i nanometer (nm), hvor er den gjensidige bølgelengden i mikrometer.Det er for tørr luft med 0,03% karbondioksid , ved et trykk på 101,325 Pa (760 millimeter kvikksølv) og en temperatur på 288,15 Kelvin ( 15 ° C ).
Vi kan få n for en annen temperatur eller et annet trykk ved å bruke ett av følgende to uttrykk:
med:
- T , temperatur uttrykt i kelvin ;
- p , trykk i skritt;
- T s , 288,15 K ;
- p s , 101,325 Pa ;
- n s , brytningsindeks for luft gitt ovenfor,
eller:
med:
- T , temperatur i grader Celsius ;
- T s , 15 ° C ;
- p , trykk i mmHg ;
- p s , 760 mmHg ;
- , 0,00366 K −1 ;
- , (1,049 - 0,015 T ) × 10-6 mmHg -1 ;
- , 8,13 × 10-7 mmHg −1 ;
- n s , brytningsindeks for luft gitt ovenfor.
Termofysiske egenskaper
Fra tabeller publisert av Frank M. White, Heat and Mass transfer , Addison-Wesley, 1988.
med:
- T , temperatur i Kelvin ;
- ρ , tetthet ;
- μ , dynamisk viskositet ;
- v , kinematisk viskositet ;
- C p , spesifikk varme ved konstant trykk ;
- λ , varmeledningsevne ;
- a , termisk diffusivitet ;
- Pr , Prandtl-nummer .
| T | ρ | μ | ν | C s | λ | på | Pr |
|---|---|---|---|---|---|---|---|
| K | kg m −3 | kg m −1 s −1 | m 2 s −1 | J kg −1 K −1 | W m −1 K −1 | m 2 s −1 | - |
| 250 | 1.413 | 1,60 × 10 −5 | 0,949 × 10 −5 | 1.005 | 0,0223 | 1,32 × 10 −5 | 0,722 |
| 300 | 1.177 | 1,85 × 10 −5 | 1,57 × 10 −5 | 1.006 | 0,0262 | 2.22 × 10 −5 | 0,708 |
| 350 | 0,998 | 2,08 × 10 −5 | 2,08 × 10 −5 | 1.009 | 0,0300 | 2,98 × 10 −5 | 0,697 |
| 400 | 0,883 | 2.29 × 10 −5 | 2,59 × 10 −5 | 1.014 | 0,0337 | 3,76 × 10 −5 | 0,689 |
| 450 | 0,783 | 2,48 × 10 −5 | 2,89 × 10 −5 | 1.021 | 0,0371 | 4,22 × 10 −5 | 0,683 |
| 500 | 0,705 | 2,67 × 10 −5 | 3,69 × 10 −5 | 1.030 | 0,0404 | 5,57 × 10 −5 | 0,680 |
| 550 | 0,642 | 2,85 × 10 −5 | 4,43 × 10 −5 | 1.039 | 0,0436 | 6,53 × 10 −5 | 0,680 |
| 600 | 0,588 | 3,02 × 10 −5 | 5,13 × 10 −5 | 1.055 | 0,0466 | 7,51 × 10 −5 | 0,680 |
| 650 | 0,543 | 3,18 × 10 −5 | 5,85 × 10 −5 | 1.063 | 0,0495 | 8,58 × 10 −5 | 0,682 |
| 700 | 0,503 | 3,33 × 10 −5 | 6,63 × 10 −5 | 1.075 | 0,0523 | 9,67 × 10 −5 | 0,684 |
| 750 | 0,471 | 3,48 × 10 −5 | 7,39 × 10 −5 | 1.086 | 0,0551 | 10,8 × 10 −5 | 0,686 |
| 800 | 0,441 | 3,63 × 10 −5 | 8,23 × 10 −5 | 1.098 | 0,0578 | 12,0 × 10 −5 | 0,689 |
| 850 | 0,415 | 3,77 × 10 −5 | 9,07 × 10 −5 | 1110 | 0,0603 | 13,1 × 10 −5 | 0,692 |
| 900 | 0,392 | 3,90 × 10 −5 | 9,93 × 10 −5 | 1.121 | 0,0628 | 14,3 × 10 −5 | 0,696 |
| 950 | 0,372 | 4,02 × 10 −5 | 10,8 × 10 −5 | 1.132 | 0,0653 | 15,5 × 10 −5 | 0,699 |
| 1000 | 0,352 | 4,15 × 10 −5 | 11,8 × 10 −5 | 1.142 | 0,0675 | 16,8 × 10 −5 | 0,702 |
| 1.100 | 0,320 | 4,40 × 10 −5 | 13,7 × 10 −5 | 1.161 | 0,0723 | 19,5 × 10 −5 | 0,706 |
| 1200 | 0,295 | 4,63 × 10 −5 | 15,7 × 10 −5 | 1.179 | 0,0763 | 22,0 × 10 −5 | 0,714 |
| 1.300 | 0,271 | 4,85 × 10 −5 | 17,9 × 10 −5 | 1.197 | 0,0803 | 24,8 × 10 −5 | 0,722 |
Forholdet mellom temperatur og varmeledningsevne for luft, som gjelder for en temperatur mellom 100 K og 1600 K, er som følger:
eller:
- : temperatur uttrykt i K
- : varmeledningsevne i W m −1 K −1
Forholdet mellom dynamisk viskositet av luft og temperatur er:
eller:
- : temperatur i K
- : dynamisk viskositet i kg m −1 s −1
Forholdet mellom kinematisk viskositet av luft og temperatur er:
eller:
- : temperatur i K
- : kinematisk viskositet i m 2 / s
I følge informasjonen WPI (en) er forholdet mellom spesifikk varme i luften og temperaturen:
eller:
- : temperatur i K
- : spesifikk varme i J kg −1 K −1
Press
På grunn av reduksjonen i lufttrykket med høyden , er det nødvendig å sette hytter på fly og andre fly under trykk . I praksis er trykket på hyttene større enn det ytre trykket, men mindre enn trykket på bakkenivå.
Den komprimerte luft blir også brukt i dykking .
Flytende
Luft består av forskjellige gasser som, hvis de avkjøles tilstrekkelig, til slutt endres til flytende tilstand og deretter til fast tilstand . For eksempel oksygen blir fast ved en temperatur på -218 ° C , den nitrogen blir flytende ved -195 ° C . Ved en temperatur på -270 ° C (ca. 3 K ) er alle gasser unntatt helium faste og vi får "frossen luft".
Luften kunne ikke flytes før det kritiske trykket og temperaturene som markerer de teoretiske grensene utover som en forbindelse bare kan eksistere i gassform, er kjent. Siden luft er en blanding, har ikke disse verdiene en streng betydning, men faktisk, ved en temperatur over -140 ° C , er ikke luften lenger flytbar.
Koketemperatur på luftkomponenter
| Etternavn | Formel | Temperatur |
|---|---|---|
| Dinitrogen | Nr. 2 | −195,79 ° C , flytende nitrogen |
| Dioksygen | O 2 | −183 ° C , flytende oksygen |
| Argon | Ar | −185,85 ° C |
| Karbondioksid | CO 2 | −56,6 ° C ved 5,12 atm |
| Neon | Født | −246,053 ° C |
| Helium | Hei | −268,93 ° C , flytende helium |
| Nitrogenmonoksid | NEI | −151,8 ° C |
| Krypton | Kr | −154,34 ° C |
| Metan | CH 4 | −161,52 ° C |
| Dihydrogen | H 2 | −252,76 ° C , flytende hydrogen |
| Nitrogenoksid | N 2 O | −88,5 ° C |
| Xenon | Xe | −108,09 ° C |
| Nitrogendioksid | NO 2 | 21,2 ° C |
| Ozon | O 3 | −111,9 ° C |
| Radon | Rn | −61,7 ° C |
De første dråpene med flytende luft ble oppnådd nesten samtidig av Louis Paul Cailletet og Raoul-Pierre Pictet i 1877 , ved plutselig utvidelse mellom 300 og 1 atmosfære.
I 1894 utviklet den nederlandske fysikeren Heike Kamerlingh Onnes den første flytende luftinstallasjonen. I løpet av de neste 40 årene har forskere i Frankrike, Storbritannia, Tyskland og Russland gjort mange forbedringer i prosessen.
Sir James Dewar flytte først hydrogen i 1898 og Heike Kamerlingh Onnes helium, den vanskeligste gassen å flyte, i 1908 .
Uavhengig av Carl von Linde , Georges Claude utviklet i 1902 en industriell prosess for kondensering av luft.
Symbolsk
- I et uvitenskapelig domene er luft et av de fire elementene (sammen med ild , vann og jord ) som en gang ble ansett (og fremdeles betraktet i noen kulturer) som stoffene på. Som ville være basert gjennom hele livet. Han er Åndens symbol.
- Luft er også ofte assosiert med forskjellige andre konsepter som sverdfamilien i tarotdekk .
Merknader og referanser
Merknader
- Dette er den molare massen av tørr luft.
Referanser
- " Air " , på olivier.fournet.free.fr (åpnet 4. mars 2010 )
- (en) Komprimert gassforening, Håndbok for komprimerte gasser , Springer,1999, 4 th ed. , 702 s. ( ISBN 0-412-78230-8 , leses online ) , s. 234
- (no) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- (in) Philip E. Ciddor, " Refractive index of air: new equations for the visible and near infrared " , Applied Optics , Vol. 35, n o 9,1996, s. 1566-1573 ( DOI 10.1364 / AO.35.001566 )
- (in) Nylig global CO2 på noaa.gov, åpnet 21. april 2021.
- (in) The Keeling Curve , nettstedet keelingcurve.ucsd.edu, åpnet 23. april 2015
- CO 2 -konsentrasjon i jordens atmosfære
- CO 2 -konsentrasjon målt ved Mauna Loa (Hawaii), NOAA.
- Konsentrasjon av metan målt ved Mauna Loa (Hawaii), NOAA.
- I praksis inneholder sterkt tørket luft fortsatt spor av vanndamp.
- Datakilde: Karbondioksid: (en) NASA - Earth Fact Sheet , januar 2007. Metan: IPCC TAR; tabell 6.1, 1998 (en) IPCC Third Assessment Report "Climate Change 2001" av GRID-Arendal i 2003. Totalt var NASA 17 ppmv av 100%, og CO 2økte her med 15 ppmv . For å normalisere, N 2 må reduseres med 25 ppmv og O 2 ved 7 ppmv .
- " Luftbrytningsindeks " , på olivier.fournet.free.fr (åpnet 4. mars 2010 )
- Kjemiske fagpersoner
- Chemical Professionals , ikke funnet 11. august 2013
- Dette dokumentet fra WPI-nettstedet , på wpi.edu-nettstedet
Se også
Relaterte artikler
- Lufttetthet
- Luftmasse
- Psykrometri
- Fuktig luft
- Luftforurensning og artikler fra Kategori: Luftforurensning
- Luftkvalitet