Dihydrogen
| Dihydrogen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-navn | hydrogen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
hydrogen |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.014.187 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 215-605-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E949 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
[HH] , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | luktfri, fargeløs, komprimert gass | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
H 2 [isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 2.01588 ± 0.00014 g / mol H 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −259,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | −252,76 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet |
21,4 ml i 1 l vann (dvs. 1,92 mg / l ) ( 0 ° C ) 8,5 ml i 1 l vann ( dvs. 0,76 mg / l ) ( 80 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighetsparameter δ | 6,9 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumisk masse |
0,089 88 g / l (gass, CNTP ), 0,070 8 kg / l (væske, −253 ° C ), ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selvantennelsestemperatur | 500 til 571 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | brannfarlig gass | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosjonsgrenser i luft | 4 - 76 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mettende damptrykk |
ligning:
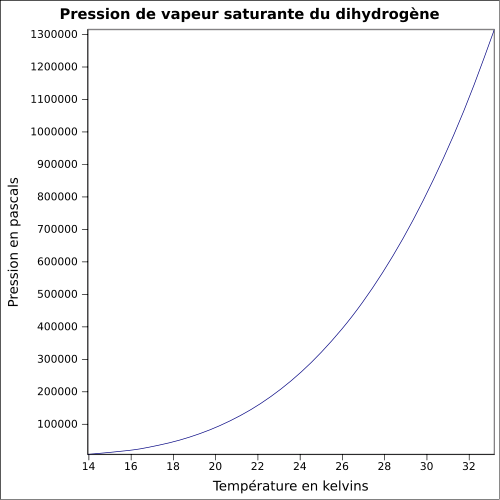
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 13,0 bar, −239,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trippel punkt |
−259,3467 ° C ; 7,205 kPa abs |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termisk ledningsevne | 42,5 × 10 −5 kal cm −1 s −1 K −1 til 16,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighet | 1310 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gass, 1 bar | 130,68 J K −1 mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,058 68 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 0,90 kJ mol −1 ( 1 atm , −252,76 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s | 14 266 J kg −1 K −1 til 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 285,8 kJ / mol ( 25 ° C , gass) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 242,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H220 H220 : Ekstremt brannfarlig gass |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Kritisk komprimert gass temperatur = −239,9 ° C B1 : Brannfarlig gass nedre brennbarhetsgrense = 4,0% Opplysning ved 1,0% i henhold til klassifiseringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gass:
4
0
0
nedkjølt væske: 4 3 0 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : brannfarlig gass UN-nummer : 1049 : KOMPRIMERT VÆSKE Klasse: 2.1 Klassifiseringskode: 1F : Komprimert gass, brannfarlig; Merkelapp: 2.1 : Brennbare gasser (tilsvarer gruppene betegnet med store bokstaver F); 
223 : kjølt flytende gass, brannfarlig FN-nummer : 1966 : HYDROGEN KJØLESKYDD VÆSKE Klasse: 2.1 Klassifiseringskode: 3F : Kjølt flytende gass, brannfarlig; Merkelapp: 2.1 : Brennbare gasser (tilsvarer gruppene betegnet med store bokstaver F);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Innånding | kvelning | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den dihydrat er form molekylære av elementet hydrogen som eksisterer som gass til standardbetingelser for temperatur og trykk . Molekyler har to hydrogenatomer; dets kjemiske formel er H to . Det kalles også "molekylært hydrogen" eller, i gassform, "hydrogengass". I det daglige språket, når det ikke er tvetydighet med det kjemiske elementet med samme navn, blir det veldig ofte referert til det som "hydrogen", og vi snakker noen ganger bare om "hydrogenmolekyl" for hydrogenmolekylet.
Den ble brukt i Zeppelin typen luftskip , ved hjelp av egenskapene til Arkimedes skyvekraft , før de blir erstattet av helium , som er mindre farlig fordi det ikke er brennbart. I dag er det globale forbruk av hydrogen rundt 50 millioner tonn per år. Det meste av produksjonen av hydrogen forbrukes på stedet, hovedsakelig i den kjemiske og petrokjemiske industrien: syntese av ammoniakk (50%), raffinering og avsvovling av hydrokarboner (37%), syntese av metanol (12%). Den er laget 96% av hydrokarboner (metan, petroleum, kull) og 4% ved elektrolyse av vann . Denne produksjonen ledsages i 2020 av produksjon av 830 millioner tonn CO 2per år, eller omtrent 2% av de globale utslippene .
Det er en lett gass som jordens tyngdekraft ikke kan holde tilbake. Den brenner i luften og produserer vann , derav navnet sammensatt av prefikset "hydro", fra gresk ὕδωρ (hudôr) som betyr "vann", og av suffikset "gen", fra gresk γεννᾰν (gennen), "Beget" . Det har blitt brukt spesielt til konservering av kjøtt . Dihydrogen har en fordampningstemperatur på 20,27 K og en smeltetemperatur på 14,02 K . Under veldig høyt trykk , som de som finnes i sentrum av gassgiganter , dissosierer disse molekylene og hydrogen blir et flytende metall . I rommet, skyer av H- 2 er grunnlaget for den stjernedannelse prosessen .
Historisk
Den første kjente forskeren som har beskrevet produksjonen av dihydrogen var sveitsiske Paracelsus (1493-1541). Han gjorde dette funnet ved å helle Sulfat løpet jernpulver , men forsto ikke det nøyaktige innholdet i gassen avgitt under forsøket .
Den engelske kjemikeren Henry Cavendish (1731-1810), som gjentok eksperimentene med Paracelsus med flere forskjellige metaller , oppdager at gassen som dermed produseres er forskjellig fra luft, er brannfarlig og har lav tetthet. Han kalte denne gassen "brennbar luft" (på engelsk: brennbar luft ) og finner ut at den er forbrenningsprodukt av vannet . Den dioxygen blir han kalt "vital luft".
Den franske kjemikeren Antoine Lavoisier etter å ha bekreftet forsøkene med Cavendish, foreslår ordet "hydrogen" for å erstatte uttrykket "brannfarlig luft". Dette ord er utformet med prefikset hydro (fra gresk ὕδωρ (hudôr), “vann”) og suffikset genet (fra gresk γεννᾰν (gennen), “for å generere”). Ordet hydrogen betyr derfor at det genererer vann .
Deretter, i fagfeltet, ordet "hydrogen" vil bli brukt for å navngi kjemisk element H og ordet "hydrogen" bli brukt for den molekylet H- 2 .
Kjemiske egenskaper
Anerkjennelsestest
For å teste for tilstedeværelse av dihydrogen, nærmer man seg en flammende logg til et reagensrør som inneholder dihydrogen. Den kjemiske reaksjonen ved forbrenning av hydrogen med oksygen i luften, initiert av varmekilden, gir en karakteristisk støy som kalles "bjeffing" eller "bjeffing".
Forbrenning
Den forbrenning av hydrogen i dioksygen , som produserer vann , er 2 H 2 (g) + O 2(g) → 2 H20(de). Den er spesielt voldelig (se gjenkjenningstest) og veldig eksoterm : dens brennverdi er 141,86 MJ / kg [eller 141,79 MJ / kg ] (ved 25 ° C [eller 15 ° C ] under 1 atm ), eller en standard forbrenningstentpi , ved 25 ° C , av -285,84 kJ / mol , ved 100 ° C , av -283,45 kJ / mo l (H 2 gass, O 2 gass, men H 2 O væske , som høyere varmeverdi eller PCS), men av 120,1 MJ / kg [eller 119,93 MJ / kg ], det vil si en entalpi på forbrenning, ved 100 ° C , av -242,8 kJ / mol (H 2 gass, Gassformig O 2 H 2 O damp , som lavere brennverdi eller NCV , teller 40,660 kJ / mol for fordampning av vann ved 100 ° C ), mot for eksempel bare 49,51 MJ / kg for butan . Denne egenskapen gjør den til et drivstoff for valg av romfartøyer, men gjør lagringen farlig.
Den samme oksidasjonen saktere brukes til å produsere strøm i brenselcellen .
Ortho og para former
Hydrogengass er en blanding av to typer isomere molekyler som skiller seg fra hverandre i spinnet til atomkjernene . Disse to formene kalles orto- og para-hydrogen , og ortoformen (parallelle spinn, triplettilstand) tilsvarer en opphisset tilstand som ikke eksisterer i sin rene tilstand. Under normale temperatur- og trykkforhold , ved termisk eksitasjon, består hydrogen av 75% av ortoformen og 25% av paraformen. Ved 77 K er blandingen i likevekt (nådd spontant på flere dager, men i løpet av få timer med katalysatorer) 50%. Men ved veldig lav temperatur forvandles ortoformen fullstendig til paratilstanden (antiparallelle spinn, singlet -tilstand) over tid. De to formene har litt forskjellige energinivåer og derfor litt forskjellige fysisk -kjemiske egenskaper . For eksempel er smeltepunktet og kokepunktet for para-hydrogen omtrent 0,1 K lavere enn for orto- .
Hydrogenkilder
Dihydrogen er en veldig lett gass. Siden jordens tyngdekraft ikke kan holde den tilbake, slipper den naturlig fra jordens atmosfære. Derfor er det bare tilstede i spormengder (0,5 ppmv ) i luft . Denne atmosfæriske knappheten betyr at alt brukt dihydrogen produseres industrielt ved forskjellige prosesser, fra molekyler hvor hydrogenatomer er kjemisk bundet.
Imidlertid er det noen få geologiske sammenhenger der dihydrogen naturlig springer ut fra jorden . Hydrogenet som kommer fra disse sonene er betegnet med begrepet naturlig hydrogen .
Kunstig hydrogen
Den produksjon av hydrogen involverer mange forskjellige prosesser , det hydrogenatom som danner en rekke molekyler ( vann , hydrokarboner , sukker , etc. ).
Historisk produksjonsmetodeHistorisk sett i XIX th -tallet, ble det dihydrogen oppnådd ved utslipp av vanndamp (H 2 O) i en tønne fylt med jernspon og chips. Vanndampen oksiderte metallet og dannet jernoksid på den ene siden og frigjorde hydrogen på den andre. Sistnevnte forlot deretter fatet, hvor det ble filtrert inn i et annet fat fylt med vann, deretter lagret direkte i en aerostat . Denne enheten tillot hæren å blåse opp en observasjonsballong hvor som helst og på få timer .
Gjeldende metoderI 2015 ble hydrogen produsert industrielt ved forskjellige prosesser:
- for 49% ved dampreformering fra hydrokarboner (spesielt fra metan , se Reformering av metan );
- for 29% ved delvis oksidasjon av petroleum
- i 18% ved forgassing av kull
- i 4% ved elektrolyse av vann .
Andre prosesser blir også studert, fra sprekker eller delvis oksidasjon, som har fordelen av å være eksoterm .
HydrokarbondampreformeringDen dampreformering av hydrokarboner er den metode som ved begynnelsen av det XXI th århundre, er den mest brukte på industrielt nivå. Prinsippet er basert på reaksjonen av hydrokarboner (metan, etc.) i nærvær av vanndamp og varme. Den globale reaksjonen er skrevet:
.Den energieffektiviteten er rundt 40 til 45% i enkelte installasjoner . I industriell praksis er det nødvendig å akselerere reaksjonen ved hjelp av katalysatorer eller brennere. Det har den ulempen å produsere karbondioksid , en klimagass .
Katalytiske teknologier, eller mer innovative som plasma-reformatorer, er for tiden under utredning.
VannelektrolyseDen elektrolyse av vann er en teknologi som består i å føre en elektrisk strøm (direkte) i vann (til hvilken en elektrolytt som for eksempel kaustisk soda er tidligere blitt tilsatt ) for å oppnå den dissosiasjonen av molekylene av vann i hydrogen og oksygen .
Reaksjon ved anoden :
2 H 2 O(l) → O 2(g) + 4 H + (aq) + 4 e -Reaksjon ved katoden :
4 H 2 O(l) + 4 e - → 2 H 2 (g) + 4 OH - (aq)Reaksjon i vann:
4 H + (aq) + 4 OH - (aq) → 4 H 2 O (de)Generell reaksjon:
2 H 2 O(l) → 2 H 2 (g) + O 2 (g)hvor (l), (g) og (aq) betyr henholdsvis "i flytende fase", "i gassfase" og "i vandig løsning".
Denne teknologien krever store mengder strøm. I følge Ademe i 2020 er effektiviteten til hydrogenkjeden i Power-to-H2-to-Power 25%, mens effektiviteten til elektriske batterier er 70%. Det er derfor relativt lite brukt.
Delvis oksidasjon av hydrokarbonerDenne reaksjon er en “rik” forbrenning i den forstand at målet er å fremstille en gass som er rik på H 2 og CO (syntesegass); i stedet for de “klassiske” CO 2 og H 2 O produktene.
Reaksjonen er skrevet:
.Mesteparten av tiden brukes luft som oksydasjonsmiddel. Vi har da:
.Reaksjonen er eksoterm: for eksempel er entalpien til reaksjonen med metan -35,7 kJ mol -1 .
I likhet med dampreformeringsreaksjonen er det nødvendig å katalysere reaksjonen.
Interessen for den delvise oksidasjonsreaksjonen ligger i dens eksotermiske natur (i motsetning til dampreformeringsreaksjonen) som hjelper katalyse (temperaturstigning).
Den største ulempen ligger i det faktum at de prosenter av H- 2 er lavere enn dem som ble oppnådd ved dampreformering, på grunn av flertallet nærvær av nitrogen i luften. I tillegg er det en risiko for å oppnå NO x .
Virkning av en syre på et metallDihydrogen produseres ved virkningen av en syre på et metall. Eksempel:
.Dihydrogen kan også produseres ved å omsette natriumhydroksid med aluminium, i henhold til formelen:
Produksjon ved fotosyntese (cyanobakterier)Noen cyanobakterier kan kjemisk bryte ned vann til oksygen og hydrogen ved hjelp av fotosyntetiske reaksjoner. Dette ville gjøre det mulig å produsere hydrogen ved hjelp av solenergi . Det pågår forskning på dette området, spesielt når det gjelder genteknikk .
Naturlig hydrogen
Hydrogen produsert på jorden naturlig, i motsetning til hydrogen produsert kunstig ved å reformere metan eller hydrokarboner , sies å være naturlig hydrogen eller nativt hydrogen .
Fordelingen, produksjonskapasitet og fysikalsk-kjemiske mekanismer til sine kilder eller innskudd er fremdeles gjenstand for forsøksstudier i begynnelsen av XXI th århundre. I april 2019 ble forskningsprosjektet sen4H2 lansert og samfinansiert av European Space Agency , som tar sikte på å oppdage naturlige hydrogenutslipp ved bruk av satellittbilder.
Kilder til naturlig hydrogenProduksjonen av naturlig hydrogen i ryggraden har vært kjent siden 1970-tallet og har studert mer nylig. Disse er serpentinization reaksjoner ( redox av olivin ) mellom vann og vulkanske bergarter i flukt med mantelen , lettes ved varmen av disse eksoterme reaksjoner : oksygenet i H 2 O molekyler.fanget av jernet i fjellet, er hydrogenatomene fritt å assosiere i H 2. Hydrogen som produseres, rømmer gjennom hydrotermiske ventilasjonsåpninger og kan eventuelt reagere etter tur for å danne metan , deretter tyngre hydrokarboner. For dypt kan ikke disse innskuddene utnyttes i 2018
Hydrogenutslipp har også blitt oppdaget midt på kontinentale kratonger av den russiske geologen Nicolay Larin, etter hans arbeid med den hydratiserte jordhypotesen. De IFP Energies Nouvelles har bekreftet dette funnet i 2013, rapporterer lokalt viktige saker, på de fleste kontinenter, Russland , den USA , i Brasil , i Oman eller Mali .
Fenomenet er fortsatt dårlig forstått, og debatten om den nøyaktige mekanismen som genererer disse utslippene, er ennå ikke avgjort. Det kan handle om hydrering av jern med infiltrert vann, dette er tilstede i beltene til greenstone , tilstede i kratonene. Således, i Kansas , nær Junction City , ble et depositum identifisert på 1980 -tallet og ble gjenstand for fornyet interesse på 2000 -tallet; dihydrogenet ville bli oppnådd der fra slike reaksjoner av oksidasjon av jern. I Russland estimerte IFP i 2010 den daglige strømmen av en enkelt depresjon til flere titusenvis av kubikkmeter , eller tilsvarende forbruk på 500 drosjer. Et originalt geologisk eller hydrogeologisk middel hersker også for utslipp av hydrogen som er studert i Brasil, i noen fe-sirkler i bassenget i São Francisco .
I Yanartaş , Tyrkia, ville "tusenårsbrannene" på Chimera-fjellet være forbrenningen av en gass bestående av metan (87%), hydrogen (7,5 til 11%) og dinitrogen (2 til 4,9%), med dobbelt opprinnelse: serpentinisering på den ene siden, en termogen gass på den andre siden. De ville være den opprinnelige kilden til den olympiske flammen .
Den Mali er, i 2015, det eneste landet der det naturlige hydrogen utnyttes, i landsbyen Bourakébougou , 60 kilometer nord for Bamako . Gassen ville komme fra en "overdreven modning av olje" trolig begravd i nærheten, og reservene er anslått til omtrent 1,5 milliarder kubikkmeter . Trykket i brønnene reduseres ikke, så fyllingen fylles kontinuerlig, noe som gjør bærekraften til denne operasjonen mulig.
De vulkanske gassene inneholder ofte spor av hydrogen. På Hawaii viste en spektroskopisk studie utført på en vulkansk gassbrann at det var en forbrenning av dihydrogen.
Enhver vulkansk bergart vil inneholde hydrogen, opp til ca. 5 l / m 3 ; derfor viser alle borehullene hydrogenavgassing. Under det russiske eksperimentet med sg3-boring ble gjørmen ekstrahert fra hullet beskrevet som boblende med denne gassen .
UtfordringerI motsetning til kunstig hydrogen, som krever at det produseres energi, noe som reduserer det til bare å være en energibærer , er naturlig hydrogen en reell energikilde , og forbrenningen produserer ikke bare vann. I tillegg kan samproduksjoner være mulig med geotermisk energi eller heliumutvinning , noe som kan hjelpe sektoren til å være konkurransedyktig. Imidlertid er det industrielle potensialet ikke nøyaktig kvantifisert i 2020, og gruvedrift tar ikke hensyn til hydrogen i mange land. Deteksjonen av hydrogen in situ er virkelig vanskelig, selv om det er utviklet mer effektive detektorer.
Industriell bruk
Det globale hydrogenforbruket er i dag rundt 50 millioner tonn per år. Mesteparten av produksjonen av hydrogen forbrukes på stedet, hovedsakelig i den kjemiske og petrokjemiske industrien: syntese av ammoniakk (50%), raffinering og avsvovling av hydrokarboner (37%), syntese av metanol (12%).
De viktigste industrielle bruksområdene for hydrogen er:
- den metode Haber-Bosch (produksjon av ammoniakk ), idet hydrogenering av fett og oljer , og produksjonen av metanol ;
- produksjon av saltsyre , sveising , drivstoff for rakett og reduksjon av malm av metall;
- det flytende dihydrogen brukes til forskning ved svært lave temperaturer, inkludert studiet av superledningsevne ;
- hydrogen brukes som sporgass for å utføre lekkasjedeteksjonsoperasjoner i forskjellige felt (oljeraffinering, biler, varmeinstallasjoner, vanndistribusjonsnett, flytanker osv.);
- hydrogen er et tilsetningsstoff som er godkjent under kode E949 , i kategorien sporstoffer.
- hydrogen brukes også som varmeoverføringsfluid i visse kraftige maskiner (for eksempel synkron kraftverk generator);
- hydrogen ble brukt i aerostater fordi det er fjorten ganger mindre tett enn luft, men det har blitt erstattet av helium av sikkerhetsmessige årsaker; den brukes fortsatt til noen værballonger på avsidesliggende stasjoner.
- Dihydrogen ble testet som drivstoff for luftfart under en flytur 15. april 1988 med Tupolev Tu-155.
Enkelte isotoper av hydrogen har også en spesiell industriell eller teknologisk bruk:
- den deuterium ( 2 H) brukes i kjernefysiske applikasjoner som en moderator ( tungtvann eller D 2 O) for å bremse nøytroner . Deuteriumforbindelser brukes også i kjemi og biologi for å studere eller bruke den isotopiske effekten ;
- den tritium ( 3 H) en annen isotop, blir produsert i kjernereaktorer , og brukes for bygging av atombomber . Det brukes også som en isotopisk markør i biovitenskap og som en kilde til stråling i selvlysende maling;
- deuterium og tritium smeltes også sammen i forskningsreaktorer og vurderes for kontrollerte kjernefusjonsprosjekter på jorden.
Til dags dato vurderes tre hovedmåter å lagre hydrogen ombord på et kjøretøy:
- lagring i form av komprimert gass;
- lagring i flytende form ved lav temperatur;
- lagring i fast form, idet hydrogenet deretter bindes til andre komponenter (ved adsorpsjon eller i form av en kjemisk forbindelse).
Komprimert gass
Det er den vanligste formen for lagring av hydrogen.
Gasslagring i komprimert form (for tiden 350 bar) gjør det mulig å oppnå en tilfredsstillende massetetthet med komposittanker. Lagringstettheten er fortsatt lav: et trykk på 700 bar er uunngåelig for å gjøre teknologien konkurransedyktig.
Teknologien eksisterer og brukes ofte. Dens ulempe ligger i energien som kreves for kompresjon og i den lave effektiviteten når det gjelder størrelse sammenlignet med andre metoder. Denne ulempen er en av vanskelighetene for bruk av dihydrogen i form av komprimert gass i bilapplikasjoner.
Ved komprimering er tettheten av hydrogen ved 20 MPa ( 200 bar) omtrent 16,8 kg / m 3 , ved 35 MPa ( 350 bar) ca. 23 kg / m 3 og ved 70 MPa ( 700 bar)) på omtrent 38 kg / m 3 . Dette tilsvarer en energitetthetstetthet på 767 kWh / m 3 (27 ° C, 35 MPa) og fortsatt en energitetthetstetthet på 33,3 kWh / kg.
Væskelagring ved 20 K ( -253 ° C ) under 10 bar gjør det mulig å oppnå interessant volum og massetetthet, men krever tanker med høy varmeisolasjon for å minimere fordampning.
Teknologien er der. Den har bedre volumeffektivitet enn lagring av komprimert gass ( 70 kg / m 3 mot 10 kg / m 3 ved 115 bar og 0 ° C ). Imidlertid modereres denne fordelen av det relativt store volumet av de nødvendige isolerende innkapslingene.
På den annen side er det nødvendig med en betydelig mengde energi for å bytte til væskefasen: kondensering bruker 30 til 40% av gassens energiinnhold og tapet i reell bruk er betydelig (for tiden 1,25 per tusen per time), sterkt straffe lagring utover en uke.
Denne teknikken brukes spesielt i romfartssektoren, til tross for kort implementeringstid, er fyllingen kontinuerlig til siste øyeblikk.
Metallhydrider
Lagring på underlag i adsorbert form, spesielt på metallhydrider , har en veldig interessant volumtetthet, men en lav vekttetthet. I tillegg er kinetikken, temperaturen og sykkeltrykket vanskelig å kontrollere.
Hydrogenatomer lagres i noen metallforbindelser. Hydrogenet utvinnes ved oppvarming eller reduksjon av trykket. Denne teknikken er dårlig forstått i dag. Det har den ulempen at det krever et ekstremt rent dihydrogen for å unngå å ødelegge absorpsjonskapasiteten til hydrider. Oppvarming for å gjenvinne gass er også et handikap. Denne typen lagring, som fortsatt er gjenstand for forskning, er på det industrielle utviklingsstadiet, og visse demonstrasjonsprosjekter er planlagt, for eksempel med oppstarten McPhy som utvikler magnesiumhydridteknologi (teknologi fra CNRS, NEEL Institute) .
Lagringskapasitet for visse hydrider.
| Hydride | Masse prosent av H- 2 -innhold |
|---|---|
| LaNi 5 H 6.5 | 1.4 |
| ZnMn 2 H 3.6 | 1.8 |
| TiFeH 2 | 1.9 |
| Mg 2 NiH 4 | 3.6 |
| VH 2 | 3.8 |
| MgH 2 | 7.6 |
Et veldig studert metall er palladium som via hydridet PdH 2, har evnen til å absorbere en stor mengde hydrogen i krystallgitteret. Ved romtemperatur og atmosfæretrykk kan palladium absorbere opptil 900 ganger volumet av hydrogengass, og prosessen er reversibel.
Den adsorpsjon på karbon gjør det mulig å lagre på overflaten av visse karbonstrukturer , slik som aktivert karbon eller nanorør , molekylene av hydrogen. Det gjør det mulig å lagre 0,05 til 2 vekt% dihydrogen .
Denne typen lagring er på forskningsstadiet.
Produksjon og bruksområder
I en rapport publisert i juni 2019, bemerker Det internasjonale energibyrået allsidigheten av hydrogen, som kan produseres fra alle fossile brensler, fornybare energikilder og kjernefysiske stoffer, kan transporteres i gassform eller flytende form og gjøres om til elektrisitet eller i metan for en lang rekke bruksområder.
Vi kan skille mellom tre kategorier produsert hydrogen, avhengig av hvordan det produseres (se delen Gjeldende metoder ):
- den hydrogen grå , fremstilt ved omdanning av fossilt brensel uten fangst og lagring ;
- den hydrogen blå , fremstilt ved omdanning av fossilt brensel med fangst og lagring;
- det grønne hydrogenet som produseres av elektrisitet fra fornybare kilder eller kjernefysisk ( lilla for noen, gul for andre).
Hydrogen produsert i jordskorpen (ved diagenese og radiolysis ), så vel som urhydrogen (til stede siden jordens dannelse ) er andre mulige kilder, men som ennå ikke er utforsket.
I 2020 er kostnaden for grått hydrogen mellom 1 og 2 € / kg mot 4 til 7 € / kg for grønt hydrogen produsert på en industriell måte. Ifølge Julien Chauvet, Hydrogen France -direktør i Engie Solutions , "gir kiloen deg 100 km, noe som setter den på nivå med bensin og ligner diesel for lette kjøretøyer" .
Industriell produksjon
Hydrogen produseres i dag nesten utelukkende fra naturgass , petroleum og kull .
For sine egne behov produserer industrien hydrogen ( f.eks .: i Frankrike, mer enn 900 000 t / år hydrogen, spesielt for avsvovling av petroleumsbrensel og for å produsere ammoniakk i nitratgjødsel ; hydrogen er da en kjemisk tilførsel og ikke en energi transportør ). Den billigste industrielle prosessen for å produsere dette hydrogenet, i 2018, er reformering av hydrokarboner , oftest ved dampreformering av naturgass (som hovedsakelig består av metan ). Ved en temperatur mellom 700 og 1100 ° C , vanndamp til reagerer med metan gir karbonmonoksid og hydrogen. Rensingen av hydrogenet er lettere under høyt trykk, og reformeringen utføres under et trykk på tjue bar . Hydrogen / karbonmonoksidblandingen blir vanligvis referert til som " syntesegass ". Hvis reaksjonen utføres i nærvær av overflødig vanndamp, oksideres karbonmonoksidet til det høyere oksidasjonsnivået , noe som fører til karbondioksid , noe som øker produksjonen av hydrogen .
Selskapet Air Liquide har en spesiell beherskelse av denne prosessen. I 2015 bestilte den i Saudi -Arabia , på Yanbu -stedet , en enhet med en total hydrogenproduksjonskapasitet på 340 000 m 3 / t ved CNTP -ene .
I 2019 vil det australske fornybare energibyrået (ARENA) gi 9,41 millioner australske dollar (8,5 millioner euro ) til et prosjekt fra Hazer-gruppen (australsk fornybar energiselskap) som tar sikte på å konvertere biogass fra metanisering av kloakkslam til hydrogen og grafitt . Hazer ønsker å bygge et demonstrasjonsanlegg på 15,8 millioner dollar i Munster (Vest -Australia).
Hydrogensektor og utfordringer for bærekraftig utvikling
Den “tradisjonelle” industrielle produksjonen av hydrogen fra fossile hydrokarboner har dårlig karbonavtrykk og avgir mye klimagasser og når 830 millioner tonn CO 2.per år i 2020, dvs. rundt 2% av de globale utslippene og nesten like mye som luftfartssektoren eller sjøtransport. I Frankrike utgjør disse utslippene nesten ti millioner tonn CO 2 -ekvivalenter.per år rundt 2015-2017, dvs. 7,5% av klimagassutslippene fra fransk industri, ifølge ADEME . Produksjonen av hydrogen fra fornybar elektrisitet, som er mer dydig, kan se at kostnadene faller med 30% innen 2030 takket være oppgangen i fornybar energi og de tilhørende stordriftsfordelene .
Den hydrogen-sektoren produserer, butikker, fremmer og forsterker hydrogen og hydrogen forskning. I 2015 pågår eksperimenter med grønt (karbonfritt) hydrogen , men denne gassen er fremdeles "hovedsakelig produsert av naturgass ( fossil ) og brukt som en kjemisk komponent i industrielle prosesser" , med en dårlig karbonbalanse og et betydelig bidrag til drivhuseffekt . Sektoren blir likevel presentert som interessant for bærekraftig utvikling , Fordi:
- hvis den er produsert ved elektrolyse av vann og på en karbonfri måte ved å gjenvinne periodiske fornybare elektrisitetsoverskudd (hovedsakelig vind og solceller), kan denne energivektoren lagres, spesielt i inter-season sesonger, deretter brukt i metanering og / eller injisert i gassnettet (6 til 20 volum% avhengig av forholdene), og letter balansen og fleksibiliteten i strømnettet ;
- elektrisitet som kan lagres takket være omdannelsen til gass (hydrogen eller metan) vil gjøre det mulig å lagre "i størrelsesorden en terrawattime per år" og opptil flere titalls teravattimer per år med strøm i henhold til ADEME , når penetrasjonen av fornybare energier i elektrisitetsblandingen vil nå 80%, og som sådan kan "gi et viktig bidrag til overgangen til en lav-karbon energimodell, spesielt i energilagringssektoren" ;
- hydrogen kan brukes til å produsere elektrisitet lokalt, men med tap av effektivitet; den for vannelektrolyse blir nærmer seg 70%, men den totale effektiviteten av elektrisitetsproduksjonen fra H 2 vil være omkring 25% i henhold til ADEME i 2020;
- hydrogen er kompatibelt med egenforbruk av et hjem, en øy eller et distrikt, noe som tillater lagring over flere dager, uker eller måneder, i tillegg til batterier som er mer nyttige for kortvarig lagring. Det ville allerede være økonomisk berettiget I områder som ikke er sammenkoblet med det kontinentale strømnettet (for eksempel: isolerte øyer, franske utenlandske samfunn der elektrisitetsproduksjonen fortsatt er avhengig av drivstoff til høye kostnader, til 225 € / MWh i gjennomsnitt i 2013 i henhold til til ADEME);
- hydrogen kan gi drivstoff til visse flåter av profesjonelle kjøretøyer , uten å kreve et dyrt nettverk med flere hundre bensinstasjoner over hele landet. I følge Ademe er "den økonomiske modellen til en stasjon for en flåte tilgjengelig for et daglig forbruk større enn 80 kg H 2 / dag, for markedsføring av hydrogen til mindre enn 10 € / kg " . I dette tilfellet har det fordelene med en rask oppladningstid og en stor autonomi;
- hydrogen kan brukes i stålindustrien som erstatning for kull eller naturgass for reduksjon av jernmalm. Å bruke denne prosessen i Frankrike ville forbruke 700 000 tonn hydrogen, men ville unngå utslipp Av 22 MtCO 2/ år, eller nesten 5% av landets utslipp, indikerer French Association for Hydrogen and Fuel Cells (Afhypac).
de 8. juli 2020, presenterer Europakommisjonen et program for utvikling av grønt hydrogen, som setter målet om at hydrogen dekker 12 til 14% av energibehovet innen 2050 for å avkarbonisere visse sektorer innen industri og transport. Det er avhengig av hydrogen for å bidra til energiovergangen og til reduksjon av klimagassutslipp. Samtidig kunngjør EU -kommisjonær for intern handel, Thierry Breton, etableringen av hydrogenalliansen.
I FrankrikeDen ADEME vurderer en strøm blanding til 40% består av "fornybar" i 2035, og deretter til 60% og 70% i 2050 (mot nesten 18% i 2017, mens størstedelen av hydroelektrisk kilde).
Sektoren søker å industrialisere sine prosesser for å redusere kostnadene (spesielt de for brenselcellen ). Utviklingen av “hydrogen mobilitet” blir også hemmet av en fortsatt svært lavt antall ladestasjoner (og deres fremdeles lav kapasitet: 10 for å 80 kg H- 2 / d ved 350 bar). Hydrogen kan forbedre bilens kraft, utvide rekkevidden og forbedre hastigheten på lading, sammenlignet med batterier.
Ademe anser at hydrogen vil ha en viktig rolle i energiomstillingen, som en vektor for å optimalisere energinettverk, for lagring av energi i solforbruk eller solcelleforbruk, og for visse profesjonelle kjøretøyer, forutsatt at det karboniserer energien. Produksjon gjennom elektrolyse ved hjelp av grønn elektrisitet og transformasjon av biomasse ( dampreformering av biogass , pyrogasifisering av fast biomasse). Sektorens miljøprestasjoner vil fremfor alt avhenge av "den primære kilden som brukes til å produsere hydrogen". Byrået etterlyser å begrense hydrogentransportavstanden mellom produksjonsstedet og distribusjonsstasjonen til mindre enn hundre kilometer. Batteridrevne kjøretøy bør foretrekkes, når det er mulig (rekkevidde, tilgjengelighet, etc.), gitt den bedre lagringstypen, og energibesparelser forblir en prioritet. En av utviklingsmulighetene (for tiden testet i 2018/2019) er injeksjon i gassnettet i Frankrike via to demonstranter: GRHYD og Jupiter 1000 , for å fjerne de tekniske hindringene som fremdeles eksisterer.
I juni 2018, pålegger den franske regjeringen Ademe å lansere den "nasjonale hydrogenutplasseringsplanen" (eller "hydrogenplanen"), for å gi impuls til denne sektoren hvis "høye potensial" oppfattes av offentlige aktører. Regjeringens mål er "å skape en karbonfri fransk industrisektor, å åpne nye perspektiver for lagring av fornybar energi og å utvikle nullutslippsløsninger for transport" . Ett år senere ringte det offentlige byrået flere prosjekter , inkludert "Hydrogen mobilitetsøkosystemer", som gjorde det mulig å velge prosjekter "i alle territorier" og diversifiserte, for eksempel "last mile levering i urbane områder., Kollektiv persontransport med buss- eller sjøtransport, bilutleie, avfallshenting, forretningsflåter og til og med bruk av tunge lastebiler som anleggskjøretøy ” .
Den CEA løfter en ny industriell elektrolyse teknologi, som kalles rSOC med en enkelt edelt metall: Indium (et metall som brukes i LCD -skjermer ), med lavere temperatur (fra 700 ° C til 800 ° C ) og en lavere temperatur. Strømforbruk. Det er også reversibelt, noe som gjør det mulig å produsere hydrogen eller gjenopprette elektrisk energi som en brenselcelle.
På slutten av 2019 sluttet Air Liquide og Engie seg sammen med Durance-Luberon-Verdon Agglomeration (DLVA) for å produsere, lagre og distribuere "grønt hydrogen" (som en del av "HyGreen Provence" -prosjektet som ble lansert i 2017, med mål på 1300 GWh solenergi og flere tusen tonn: år med hydrogen produsert ved elektrolyse Flere titusenvis av tonn fornybart hydrogen per år kan produseres på lang sikt, som kan lagres i et lokalt saltrom .
Det franske selskapet McPhy , som allerede har installert 17 MW hydrogenproduksjonskapasitet ved elektrolyse under trykk, inkludert 6 MW hos Audi i Tyskland, kunngjør i januar 2020 undertegningen av ingeniørkontrakten for et produksjonsprosjekt på 20 MW industrielt grønt hydrogen , det største prosjekt hittil i Europa, lokalisert i Delfzijl i Nederland innen 2022. Anlegget vil produsere 3000 tonn hydrogen per år ved elektrolyse av vann med vindkraft og vil bli brukt til å produsere bioetanol. Prosjektet drar nytte av 15 millioner euro i tilskudd fra EU og et nederlandsk fond. I følge McPhy vil riktig skala være 100 eller 200 MW for å oppnå en konkurransedyktig pris i bransjen.
The Energy Climate Law of november 2019 gir regjeringen ett år for å sette opp en støtte mekanisme for "hydrogen produsert fra fornybar energi eller ved elektrolyse av vann ved hjelp av lav-karbon elektrisitet." . Før 2023 har det flerårige energiprogrammet som mål å avkarbonisere 10% av hydrogenet som forbrukes i industrien, noe som krever produksjon av 90 000 tonn grønt hydrogen. I januar 2020 lanserer regjeringen en oppfordring til interessetilkendegivelser , ment for å teste industrienes appetitt for emnet, som mottar mer enn 160 prosjekter. I januar arkiverer H2V Industry for eksempel søknader om byggetillatelse for to produksjonsanlegg for hydrogen i industriområdet Port-Jérôme, i Normandie, og på den store havnen i Dunkirk fra fornybar elektrisitet; hvis de klarer å dra nytte av en støttemekanisme, kan idriftsettingen deres finne sted i 2023-2024, og de vil produsere 56 000 tonn hydrogen. De store franske industriaktørene (Engie, EDF, Air Liquide, Vinci, etc. ) har også posisjonert seg.
Castex -regjeringen kunngjorde i september 2020 en mye mer ambisiøs plan enn den som ble presentert av Nicolas Hulot i 2018, utstyrt med 100 millioner euro: 2020 -planen sørger for å bruke 7,2 milliarder euro innen 2030 til grønt eller lavt karbonholdig hydrogen, inkludert 2 milliarder euro i 2021 og 2022 som en del av gjenopprettingsplanen. Regjeringen planlegger å subsidiere produksjonen av grønt hydrogen gjennom anbud, modellert på fornybar energi, og bygging av brenselcelleanlegg for hydrogenbiler. Partnerskap med Tyskland, som presenterte en hydrogenplan på 9 milliarder euro i juni, vurderes for å unngå duplisering.
Denne hydrogenplanen inneholder en første komponent på 1,5 milliarder euro som brukes til produksjon av elektrolysatorer, for å redusere kostnadene ved å forbedre den og øke volumene, for en kapasitet på 6,5 GW . Den andre komponenten på nesten en milliard euro vil bli brukt innen 2023 til å utvikle et tungt hydrogenmobilitetstilbud ved å redusere kostnadene og forbedre effektiviteten til brenselceller for tog, lastebiler, busser og fly, via flere utlysninger for prosjekter (350 millioner euro for demonstranter, 275 millioner til regionale eksperimenter, etc.). Endelig vil støtte til forskning og innovasjon bli stimulert, med en konvolutt som ble hevet til 650 millioner innen 2023. Bruno Le Maire håper at denne planen vil skape mellom 50 000 og 150 000 direkte og indirekte arbeidsplasser. Regjeringen vurderer samarbeid med Tyskland beskrevet som "Airbus for elektrolyse" som "Airbus for batterier". Frankrike har satt seg som mål å produsere 600 000 tonn grønt hydrogen per år, fra karbonfri elektrisitet, av fornybar eller kjernefysisk opprinnelse. I motsetning til Tyskland vil Paris imidlertid ikke subsidiere fangsten av karbon fra "grå" hydrogen. Bruno Le Maire håper å se "fremveksten av en fransk elektrolysesektor": sammen med giganter som Air Liquide er det også mange oppstartsbedrifter, for eksempel Lhyfe , basert i Nantes, som utvikler grønne hydrogenproduksjonssider for produsenter og lokale myndigheter, eller til og med McPhy , en Drôme -produsent av elektrolysatorer der EDF er aksjonær.
I BelgiaEt KUL -team designer en prototype på 1,6 m 2 fotoelektrokjemisk celle som produserer gjennomsnittlig 250 liter hydrogen per dag fra atmosfærisk vanndamp. Enheten omdanner 15% av solenergien til hydrogen og oksygen. Og denne teknologien bruker ikke edle metaller eller andre dyre materialer. Med tjue paneler ville et godt isolert hus være selvforsynt med strøm og varme i et år.
Colruyt Group (en stor belgisk forhandler) ønsker å avkarbonisere virksomheten så mye som mulig. I 2018 ble et av logistikksentrene utstyrt med 75 heiser drevet av "karbonfritt" hydrogen, og lastebilflåten må være konvertert innen 2030. Med en gassaktør forberedes et installasjonsprosjekt på 12 til 25 MW . (Utvides) å konvertere elektrisitet fra offshore vindturbiner , i industriell målestokk.
I JapanPå slutten av 2017 bekreftet Japan, en stor energiimportør, at de ønsket å bli ledende som et " hydrogenselskap " med mål om "kostnadsparitet" med bensin og LNG for strømproduksjon. Som med atomkraft tidligere, presenteres hydrogen som et viktig middel for å avkarbonisere energi, men pilotprosjektene vil gi sine konklusjoner rundt 2020. I 2018 er Japan i tet for hydrogenmobilitet, med nesten 2500 biler med hydrogenbrenselceller i sirkulasjon og mer enn hundre hydrogenstasjoner (sammenlignet med 45 i Tyskland, 42 i USA og rundt 20 i Frankrike samtidig). Landet har som mål å dele produksjonskostnadene med mer enn tre før 2030, deretter med 80% før 2050. Mellom 2013 og 2017 har den japanske staten allerede investert 1,5 milliarder dollar i FoU og utvikling av hydrogen.
I CaliforniaI oktober 2019, California har 7.570 registrerte hydrogenbiler og 42 amerikanske offentlige stasjoner.
I TysklandDen tyske regjeringen vedtar en ambisiøs plan for utvikling av "grønt" hydrogen, utstyrt med 9 milliarder euro.
Hydrogenmotor
Atomfusjon: H-bombe- og fusjonsreaktorer
Farer, risiko og forholdsregler
Dihydrogen er en gass klassifisert som "ekstremt brannfarlig ". Den er preget av et meget bredt antennelsesområde (fra 4 til 75% av volumet i luft), og forårsaker en deflagrasjon fra et veldig lavt aktiviseringsenergiinngang (en gnist er tilstrekkelig hvis den gir en. Energi på 0,02 millijoules (mJ) mens det tar 0,29 mJ å utløse en eksplosjon av metan ). Dihydrogen blandet med oksygen i støkiometriske proporsjoner er et kraftig eksplosivstoff . Dihydrogen i luft er en eksplosiv blanding når H- 2 / luft- volumforholdet er mellom 13 og 65%
Historien om bruken i luftskip er full av alvorlige ulykker, hvorav den mest kjente er Hindenburg-katastrofen . De LS 129 luftskip , oppblåst med 200.000 kubikkmeter hydrogen (fordi USA har erklært en blokade mot Tyskland for helium ) brente6. mai 1937ved ankomst til Lakehurst flyplass , nær New York ). 36 mennesker døde av de totalt 97 om bord. Mediene til stede offentliggjorde mye bilder av katastrofen, noe som førte til offentlig misnøye med ballongene. Undersøkelsene av ulykkens opprinnelse, tilrettelagt av overflod av fotografiske dokumenter, inkriminerte imidlertid ikke en eksplosjon av hydrogen, men en tenning av sammenheng, fra en brann i konvolutten (sannsynligvis forårsaket av statisk elektrisitet). Sammensetningen av det vanntette belegget på konvolutten (butyrater og aluminium) ville ha favorisert en voldsom aluminoterm reaksjon . Ulykken hadde imidlertid vært mye mindre voldelig hvis ballongen hadde blitt blåst opp med helium.
Erstatning av hydrogen med helium (mye dyrere og tettere) ga ikke den forventede gjenopplivingen av favør. Frykten for hydrogen forble; den “Hindenburg syndromet” har sannsynligvis urettferdig straffet bransjen.
Dihydrogen reagerer enda mer voldsomt med klor for å danne saltsyre (HCl), selv uten aktivering, og med difluorid for å danne farlig flussyre (HF), selv ved temperaturer der hydrogen er flytende og fluorfast, den siste reaksjonen er den mest eksoterme kjemiske reaksjon er det .
Den standard sikkerhet er styrket for å håndtere risikoen ved passering i tunneler og parkering i garasje eller underjordiske parkeringsplasser.
Globale bilreguleringer utvikles i regi av FN basert på forslag fra produsenter, men med hensyn til dihydrogen er japanske, amerikanske og europeiske produsenter ikke enige. EU-kommisjonen kunne ta stilling til midlertidige fellesskapsregler.
I Frankrike samarbeider INERIS og CEA med International Organization for Standardization ( ISO ) i en teknisk komité med navnet TC 197 om hydrogenrisikoen. Et europeisk Hysafe -prosjekt omhandler også problemet, der INERIS kritiserte utkastet til forskrift ved å foreslå en mer global og systemisk tilnærming og ikke etter komponent for homologering av hybridbiler . I 2015 utarbeidet MEDDE en oppdatering av regelverket for bensinstasjoner og flåter av kjøretøyer som kjører på hydrogen.
Fare for ozonlag
En massiv utslipp av hydrogengass har reist hypotesen om en risiko for ozonlaget .
Sikkerhetstiltak
Følgende punkter er bemerkelsesverdige:
- hydrogen er ikke iboende giftig;
- det er åtte ganger lettere enn metan. Det svært lille molekylet gir det en veldig god diffusjonskoeffisient i luften (fire ganger metan); i et ubegrenset miljø har hydrogen derfor en tendens til å stige og fort fortynnes i luften (det er en sikkerhetsfaktor i det fri, og en farefaktor på trange steder);
- det er den mest energiske kjemiske arten per masseenhet (120 kJ / g ); men per volumsenhet gass er den teoretiske eksplosive energien 3,5 ganger lavere for hydrogen enn for naturgass;
- dens nedre antennelsesgrense er 4 volum%, sammenlignbar med naturgass (5 volum%); men den øvre grensen for betennelse er betydelig høyere (75% mot 15%); dette betyr at i tilfelle lekkasje vil hydrogen antenne mye lettere enn naturgass eller flytende drivstoff;
- energien som kreves for å tenne den ved støkiometri er også betydelig lavere (omtrent 10 ganger) enn naturgass eller propan;
- hydrogenflammen, lyseblå, er nesten usynlig i løpet av dagen (risiko for nødetater);
- hydrogenflammen forplanter seg omtrent syv ganger raskere enn naturgass og risikoen for detonasjon (eksplosjon med en veldig sterk eksplosjonseffekt) forverres av sin høye diffusivitetskoeffisient.
Brennbarhet kan ytterligere reduseres ved å fortynne hydrogen i helium, selv ved veldig høy temperatur.
FN-referanse for transport av farlig gods
- Navn (fransk): Komprimert hydrogen
- Klasse: 2
- nummer: 1049
- Navn (fransk): Kjølt flytende hydrogen
- Klasse: 2
- nummer: 1966
- Navn (engelsk): Hydrogen i en metallhydridlagringsenhet
- Klasse: 2
- nummer: 3468
Merknader og referanser
- HYDROGENE , sikkerhetsark (er) for det internasjonale programmet for sikkerhet for kjemiske stoffer , konsultert 9. mai 2009
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Innbundet ( ISBN 978-1-4200-9084-0 ).
- Jean-Louis Vignes ( dir. Og medlem av Chemical Society of France) et al. , " Dihydrogen: Physico-Chemical Data " , markedsføring og utdanningsside relatert til kjemiske grunnstoffer (fra periodisk tabell av Dmitri Mendeleïev ), på lelementarium.fr , Paris og Puteaux , Société Chimique de France og Frankrike Chimie (åpnet 3. november 2019 ) .
- Pierre Ravarini (kjemisk ingeniør og hydrologist), " Gaz-Hydrogen " , stedet for vitenskapelige, tekniske og økologiske informasjon om vann, Côte de Nacre ( Calvados ) 2019(åpnet 3. november 2019 ) .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , leses online ) , s. 294
- (no) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- " Properties of Various Gases ", på flexwareinc.com (åpnet 12. april 2010 )
- Referat fra den internasjonale komiteen for mål og vekt , 78 th Session, 1989, pp. T1-T21 (og s. T23-T42, engelsk versjon).
- (in) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40.
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online presentasjon ) , s. 5-89
- Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Forgassning av kull , red. Ingeniørens teknikker, referanse J5200 , 10. desember 2009, s. 4
- " Office of Radiation, Chemical & Biological Safety (ORCBS) " (åpnet 16. april 2009 )
- EF-forordning nr . 1272/2008 , 16. desember 2008 [PDF] om EUR-Lex , s. 923 : Vedlegg VI, tabell 3.1, indeksnummer .
- " Hydrogen " i databasen over kjemiske produkter Reptox fra CSST (Quebec-organisasjonen med ansvar for arbeidsmiljø og helse), åpnet 23. april 2009
- "hydrogen" , på ESIS , åpnes den 15 februar 2009
- " Oppdagelsen av hydrogenkilder åpner veien for en ny energi " , Le Monde .
- “ Naturlig hydrogen, en energi El Dorado? » , Sciences et Avenir .
- Lavoisier eksperimenter , på lavoisier.cnrs.fr
- " Hydrogen energy " , om kunnskap om energier ,30. august 2011(åpnet 10. desember 2019 ) (oppdatert9. april 2015).
- Hydrogenkjedeutbytte (teknisk ark), Ademe ,januar 2020( les online [PDF] ).
- " Oppdagelse av naturlige hydrogenutslipp ved hjelp av satellittbilder - Lansering av sen4H2 -prosjektet " , på IFP Énergies nouvelles (åpnet 6. april 2019 ) .
- “ Deep-sea mineral resources ” , på Ifremer (åpnet 28. oktober 2019 ) .Artikkelen presenterer et kart over havbunnen som gir den kjente slangedistribusjonen langs åsene.
- Sylvestre Huet , “ Innfødt hydrogen, en ny energikilde? » , On sciences.blogs.liberation.fr , Liberation ,23. april 2013(åpnet 28. oktober 2019 ) .
- " Seawater-mantle reaction: serpentine formation " , på Ifremer (åpnet 28. oktober 2019 ) .
- " Syntese av hydrogen, metan og hydrokarboner i dyphavet, mot nye energiressurser ... " , på Ifremer (åpnet 28. oktober 2019 ) .
- " Hydrogen, yes, but natural hydrogen " , på La Tribune ,28. juni 2018(åpnet 3. oktober 2020 ) .
- Naturlig hydrogen: et bidrag til energimiksen? , IFP Nye energier ,11. april 2013.
- Julia Guélard , Karakterisering av naturlige hydrogenutstrålinger i en intrakratonisk sammenheng: eksempel på en gass / vann / berginteraksjon i Kansas (doktorgradsavhandling i geokjemi), Pierre-et-Marie-Curie University og IFP Énergies nouvelles ,2016( online presentasjon , les online ).
- (i) J. Guélard , V. Beaumont , V. Rouchon og F. Guyot , " Natural H2 in Kansas: Deep gold shallow origin? » , Geokjemi, geofysikk, geosystemer , vol. 18, n o 5,3. april 2017, s. 1841–1865 ( ISSN 1525-2027 , DOI 10.1002 / 2016GC006544 , abstrakt , lest online , åpnet 28. oktober 2019 ).
- Alain Prinzhofer, Eric Deville, Natural hydrogen - Den neste energirevolusjonen? , Ed. Belin, 2015 ( ISBN 978-27011-83848 ) .
- J. Guélard et al. , " Natural H 2 i Kansas: Dyp eller grunne opprinnelse? ", Geokjemi geofysikk geosystemer ,april 2017( DOI 10.1002 / 2016GC006544 , online presentasjon , les online [PDF] , åpnet 25. oktober 2109 ).
- (in) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau, Alain Prinzhofer Eric Deville, " Hydrogendamp i intrakratoniske områder: Nye guidelinjer for tidlig screening av bassenget " på hmdpi.com ,22. mars 2021(åpnet 16. juni 2021 )
- (i) Maria Rosanne Fabian Rupin Louis Gorintin Julio Aguilar, Helena-Fog, Werly Julien Olivier Lhote, Xi Yao, " PARHYS SYSTEM: EN NY TILNÆRMING TIL H2-KONSENTRASJONSMÅLING I UNDERSIDEN " på hnatsummit.com ,26. april 2021(åpnet 16. juni 2021 )
- (in) H. Hosgormez G. Etiope og MN Yalçin , " Nye bevis for en blandet uorganisk og organisk opprinnelse til den olympiske brannen Chimaera (Tyrkia): en bred siv av gassabiogener " , Geofluids , vol. 8, n o 4,25. november 2008, s. 263–273 ( DOI 10.1111 / j.1468-8123.2008.00226.x ).
- " Bourakébougou: løftet av en hydrogenkraftverk " ,18. februar 2013(åpnet 28. oktober 2019 ) .
- " Hydrogen ifølge Isabelle Moretti - Sciences et Avenir " , Sciences et Avenir (åpnet 2. juni 2021 ) .
- (in) "Vulkanske gasser: hydrogenforbrenning ved vulkanen Kilauea, Hawaii" på mendeley.com.
- (no) Deep Hydrogen på astrobio.net.
- (no) GJ MacDonald (1988). "Store spørsmål om dype kontinentale strukturer" Dypboring i krystallinsk grunnfjell, v. 1 : 28-48 s., Berlin: Springer-Verlag. .
- " Naturlig hydrogen en mye viktigere kilde enn tenkt i henhold til CNRS " , på http://erh2-bretagne.mystrikingly.com ,Mai 112019(åpnet 12. november 2019 ) .
- Isabelle Moretti, " Naturlig hydrogen: geologisk nysgjerrighet eller viktig energikilde i fremtiden?" » , Om kunnskap om energier .
- " 15. april 1988 flyr Tu-155 på hydrogen " , på Aerobuzz ,2. oktober 2020(åpnet 12. november 2020 )
- Hydrogen, nye energiteknologier. CEA nøkler, n o 50/51, Winter 2004-2005, ( ISSN 0,298 til 6,248 )
- europeisk prosjekt STORHY rapport, s. 8, tap av hydrogen
- Tribune-artikkelen Europe finansierer gigantisk batteri for å lagre fornybar energi
- (in) T. Mitsui, MK Rose E. Fomin, DF Ogletree og M. Salmeron, " Dissosiativ hydrogenadsorpsjon er palladium krever aggregater av tre eller flere ledige stillinger " , Nature , vol. 422,17. april 2003, s. 705-707 ( DOI 10.1038 / nature01557 , les online [PDF] ).
- (en) Hydrogens fremtid - Grip dagens muligheter [PDF] , International Energy Agency , juni 2019.
- (in) Gassdekarboniseringsveier 2020-2050 , Gass for klima,april 2020, 226 s. ( les online [PDF] ) , s. 17.
- " Gjenopprettingsplan: hvilket sted for energi? » , På connancedesenergies.org ,4. september 2020.
- (in) " Hydrogen produsert fra kjernefysisk vil bli sett på som" lav-karbon ", sier EU-tjenestemann " ["Hydrogen produsert fra atom vil bli betraktet som" lavt karbonavtrykk ", ifølge en EU-tjenestemann»], Om EURACTIV ,19. november 2020.
- " Den franske hydrogenplanen bekrefter diskret relanseringen av atomkraft " , på Reporterre ,2. februar 2021.
- " Naturlig hydrogen: en geologisk nysgjerrighet eller en stor energikilde i fremtiden?" » , På connancedesenergies.org ,22. mai 2020.
- “ Grønt hydrogen, den manglende lenken i overgangen ” , Alternativer économique (åpnet 8. august 2020 ) .
- Interaksjoner (brev til Air Liquide-aksjonærer), Air Liquide , september 2015 [PDF] , s. 5 .
- (in) Liz Gyekye [ https://biomarketinsights.com/australia-backs-tech-that-converts-biogas-into-hydrogen-and-graphite/ "Australia støtter teknologi som konverterer biogass til hydrogen og grafitt"] Biomarkedsmål 4. september 2019.
- Jérôme Marin, " Lhyfe vil produsere grønt hydrogen med vindturbiner " , La Tribune ,17. januar 2020.
- "Ademe viser" de viktigste bidragene "fra hydrogen til energiomstillingen" , Connaissance des energies , 4. april 2018.
- Hydrogenvektoren i energiovergangen , Opinion of ADEME, april 2018 [PDF] .
- Séverine Fontaine, " The Ademe ønsker hydrogen fra fornybar energi ", L'Automobile & L'Entreprise , nr . 5,februar 2016( les online ).
- " EU-kommisjonen avslører sin grønne hydrogenutviklingsplan " , på EnerGeek ,10. juli 2020(åpnet 11. juli 2020 ) .
- Hydrogen i energiovergangen , Ademe , februar 2016, 7 sider [PDF] .
- Joseph Martin , “ Development of hydrogen, ADEME takes stock ” , på RSE Magazine (åpnet 17. mai 2019 ) .
- " Grenoble forskere optimaliserer kunstig fotosyntese for å produsere hydrogen " , på placegrenet.fr ,21. april 2018(åpnet 30. mars 2019 ) .
- Véronique Pouzard, " Den høye temperaturen elektrolyse av CEA båret av oppstarten Sylfen " , Les Échos ,26. februar 2019(åpnet 30. mars 2019 ) .
- AFP (2019) “Grønt” hydrogen: samarbeid mellom Air Liquide, Engie and the Durance, Lubéron, Verdon agglomeration ; 13. nov 2019
- McPhy i sentrum av den største null-karbon hydrogenproduksjonsenheten i Europa , les échos 22. januar, innen 2020.
- Gjenopprettingsplan: Frankrike endrer skalaen i hydrogen , Les Échos , 3. september 2020.
- Hydrogen: Frankrike beskriver planen til 7 milliarder euro , Les Échos , 8. september 2020.
- Hydrogen: regjeringen ønsker å lage en "Airbus for elektrolyse" , Les Échos , 8. september 2020.
- (in) " KU Leuven-forskere knekker koden for rimelig, miljøvennlig hydrogengass " , på KU Leuven (åpnet 31. oktober 2019 ) .
- " Belgiske forskere utvikler et solcellepanel som produserer hydrogen " , på RTBF Info ,1 st mars 2019(åpnet 31. oktober 2019 ) .
- " Colruyt Group: innsatsen på hydrogenmobilitet " , på RTBF Info ,8. oktober 2018(åpnet 31. oktober 2019 ) .
- " Colruyt og Fluxys vil bygge et hydrogenanlegg, et første i Belgia " , Le Soir ,8. oktober 2019(åpnet 31. oktober 2019 ) .
- " Kjøring på hydrogen: vår erfaring " , Le Moniteur bil (åpnes 31 oktober 2019 ) .
- (no) Monica Nagashima (Institute of Energy Economics, Japan), Japans hydrogenstrategi og dens økonomiske og geopolitiske implikasjoner , Institut français des relations internationales , oktober 2018 [PDF] .
- "The" hydrogen strategy "of Japan" , Knowledge of energies, 9. oktober 2018.
- (in) " Alternative Fuels Data Center: Hydrogen Fueling Station Vacation " , på Alternative Fuels Data Center , United States Department of Energy (åpnet 31. oktober 2019 ) .
- Benoît Le Floc'h, “ Hva med hydrogen for lette nyttekjøretøyer? » , On Caradisiac ,29. november 2018(åpnet 30. mars 2019 ) .
- " California passerer milepælen til 7.500 hydrogenbiler i omløp " , på www.h2-mobile.fr (åpnet 31. oktober 2019 ) .
- (in) "Den tyske regjeringen vedtar hydrogenstrategi " ["Den tyske regjeringen vedtar strategi for hydrogen"], om den føderale regjeringen (Tyskland) ,10. juni 2020.
- Hydrogenulykke , Miljødepartementet, energi, bærekraftig utvikling og regional planlegging , 18 s. ( les online [PDF] ) , s. 4.
- Radisson, Laurent (2015) Hydrogenrisiko: Økologidepartementet jobber med nye tekster; ; News env, publisert 21. oktober 2015
- T. Rahn, JM Eiler, KA Boering, PO Wennberg, MC McCarthy, S. Tyler, S. Sc Chauffage, S. Donelly, E. Atlas, Extreme deuterium berikelse i stratosfæren hydrogen og den globale atmosfæriske budsjett på H2 , Nature 424 , 918-921, 2003.
- TK Tromp , RL Shia , Mr. Allen , JM Eiler og YL Yung , " Potensiell miljøpåvirkning av en hydrogenøkonomi på stratosfæren ," Science , nr . 300,2003, s. 1740-1742 ( DOI 10.1126 / science.1085169 ).
- Céline Duguey, " En eksplosiv opplevelse " , på Espace des sciences ,september 2009(åpnet 16. april 2020 ) .
- (i) Florent Tonus Mona Bahout , Paul F. Henry og Siân E. Dutton , " bruk av i situneutron diffraksjon for å overvåke høy-temperatur, faststoff / H2-gassreaksjoner " , Chemical Communications , n o 1821. april 2009, s. 2556–2558 ( ISSN 1364-548X , PMID 19532888 , DOI 10.1039 / B822419F , leses online , åpnes 16. april 2020 ).
Se også
Bibliografi
- Yver, Camille, Kvantifisere bruk av hydrogen fra jordsmonn: fra lokal til global skala , 2011 DOI: 10.4267 / 2042/47372 ( oppsummering - Prix Prud'homme 2011.
- Stephen Boucher, Hydrogen Revolution. Mot ren og effektiv energi? , forord av Thierry Alleau, Paris, Éd. du Felin, 2006, 160 s. , ( ISBN 2-86645-616-5 ) .
- Alain Prinzhofer, Eric Deville, Natural hydrogen - The next energy revolution? , Belin, 2015 ( ISBN 978-27011-83848 )
Relaterte artikler
Eksterne linker
- French Hydrogen Association
- Europeisk nettverk / Kompetansepol
- H2 utvikling
- CEA Technologies, Hydrogen, new energy technologies , Clefs CEA n o 50-51), 23. mars 2005
- Hydrogen sett av CEA
- INERIS: opplev tilbakemelding knyttet til lagringsvansker
- Hydrogen sett av French Chemistry Society
- Striden om bruk av hydrogen som drivstoff
- Alt om hydrogenalternativet, med en presseanmeldelse, internettlenker og videoer








