Dioksygen
| Dioksygen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Representasjoner av dioksygen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-navn | dioksygen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
molekylært oksygen |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.029.051 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 231-956-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E948 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
O = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / O2 / c1-2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | fargeløs gass ved omgivelsestemperatur og trykk; flytende gass : fargeløs til blå væske | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formel |
O 2 [Isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 31,9988 ± 0,0006 g / mol O 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,292 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −219 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | −183 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet | i vann ved 20 ° C : 3,1 ml / 100 ml, 14,6 mg l −1 (vann ved 0 ° C ), |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumisk masse |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
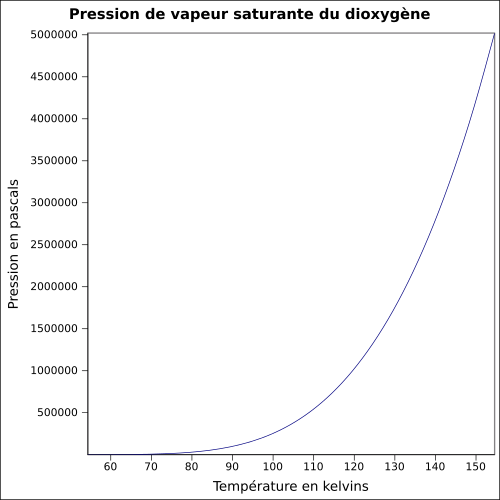
| Mettende damptrykk | ved −118 ° C : 5.080 kPa
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt |
−118,67 ° C 50,422 bar 0,636 1 kg l −1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trippel punkt |
−218,7916 ° C 0,00149 bar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighet | 330 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 213 kJ / kg | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 6,82 kJ mol −1 ( 1 atm , −182,95 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H270, H270 : Kan forårsake eller forsterke brann; oksidasjonsmiddel |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, C, A : Komprimert gass kritisk temperatur = −118,57 ° C C : Oksidasjonsmateriale forårsaker eller fremmer forbrenning av et annet materiale Avsløring ved 1,0% i henhold til klassifiseringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 3 0 OKSE | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
25 : oksiderende gass (fremmer brann) UN-nummer : 1072 : KOMPRIMERT OKSYGEN Klasse: 2 Etiketter: 2.2 : Ikke-brennbare, ikke-giftige gasser (tilsvarer grupper betegnet med A eller stort O); 5.1 : Oksiderende stoffer  
225 : kjølt flytende gass, oksidasjonsmiddel (fremmer brann) UN-nummer : 1073 : KJØLET VÆSKEOKSYGEN Klasse: 2 Etiketter: 2.2 : Ikke-brennbare, giftfrie gasser (tilsvarer grupper betegnet med hovedstad A eller O); 5.1 : Oksiderende stoffer   |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den dioksygen , vanligvis kalt oksygen er et stoff som består av molekyler O 2 (som hver består av to atomer av oksygen ). Gass under standardforhold for temperatur og trykk , fargeløs, luktfri og smakløs, den deltar i oksidasjonsreduksjonsreaksjoner , hovedsakelig forbrenning , korrosjon og respirasjon . Dioksygen er en av de allotrope formene for oksygen .
Betegnelsen " oksygen " uten ytterligere presisjon er tvetydig fordi dette begrepet kan betegne elementet oksygen (O) eller oksygengassen (O 2). Selv om ozon O 3 er også en molekylær forbindelse av elementet oksygen, er det generelt dioksygen som er referert til ved uttrykket "molekylært oksygen" og "oksygenmolekyl" anvendes.
Oppdaget uavhengig i 1772 av svensken Carl Wilhelm Scheele i Uppsala , og i 1774 av briten Joseph Priestley i Wiltshire , ble oksygen kalt slik i 1777 av franskmannen Antoine Lavoisier og hans kone i Paris fra antikkens greske ὀξύς / oxús ("akutt", altså å si her "syre") og γενής / genếs ("generator"), fordi Lavoisier feilaktig trodde - oksidasjon og forsuring var relatert - at:
"Vi har gitt basen til den pustende delen av luften navnet oksygen, avledet av to greske ord ὀξύς , syre og γείνομαι , jeg genererer , fordi faktisk en av de mest generelle egenskapene til dette grunnlaget [Lavoisier snakker om oksygen] er å danne syrer ved å kombinere med de fleste stoffer. Vi vil derfor kalle oksygengass foreningen av denne basen med kalorien. "
Dioksygen, som utgjør 20,95 volum% av jordens atmosfære (23,2 volum %), er en essensiell gass for de fleste nåværende livsformer, som den forsyner oksidasjonsmidlet som er nødvendig for cellers funksjon ( cellulær respirasjon ). I vannmiljøet er oppløst oksygen også nødvendig for livet til mange arter. Bare archaea og en minoritetsfraksjon av bakterier (kalt anaerober ) kan klare seg uten oksygen. De produserer anaerobe bakterier av oksygen som har oksidert den primitive atmosfæren, og opprinnelig redusert og deretter beriket oksygen: det er til stede i overflod i luften siden den store oksidasjonen , det er omtrent 2,4 milliarder år.
Opprinnelse og utvikling av oksygen i jordens atmosfære
Mange hypoteser er fremmet for å forklare tilstedeværelsen av oksygen i atmosfæren:
- det vanligste er at det er en gass produsert under driften av cyanobakterier , og mer generelt av klorofylliske planter , som utvinner karbon fra karbondioksid (i form av organiske forbindelser) og avviser oksygen (i form av dioksygen) ved mekanismen for fotosyntese ;
- et sekund påkaller nedbrytning, i den øvre atmosfæren , av vannmolekyler i dioksygen og hydrogen , under påvirkning av sol- og kosmisk stråling. Når dihydrogen til slutt rømmer ut i rommet (for tiden med en hastighet på rundt 3 kg / s ), akkumuleres oksygen i atmosfæren.
De to eksisterende fenomenene, virkeligheten kan være en kombinasjon av de to prosessene.
Cyanobakterier
For 4 milliarder år siden var jorden nesten helt dekket av hav, og atmosfæren besto av metan, ammoniakk og karbondioksid. De første bakteriene som finnes i havet, bruker utelukkende gjæring som energikilde. Etter hvert som de utvikler seg, blir de i stand til å bruke sollys som en energikilde , CO 2.som en karbonkilde og H 2 Oeller H 2 Ssom en kilde til hydrogen. Det er utseendet til fotosyntese . Disse autotrofiske organisasjonene , det vil si i stand til å skape sine egne næringsstoffer, vil utvikle seg, spre seg og mutere til cyanobakterier, det er 3,2 milliarder år.
Disse cyanobakteriene bruker vann som en kilde til hydrogen og frigjør dioksygen i omgivelsene, en dødelig gift for alle andre anaerobe bakterier . Denne konkurransen om oksygen mellom bakterier er et avgjørende vendepunkt i livets utvikling. Spredningen av cyanobakterier endrer fullstendig sammensetningen av atmosfæren og havene ved å berike dem med oksygen. Parallelt utvikler bakterier seg for å kunne bruke dette dioksygenet i metabolismen i stedet for gjæring , de er de første organismer som utfører cellulær respirasjon . Faktisk er energiutbyttet av respirasjon mye høyere enn gjæring, noe som gir disse levende vesener en viktigste evolusjonære fordel.
For omtrent 2 milliarder år siden svelget en primitiv eukaryot (anaerob) celle en bakterie som var i stand til å utføre respirasjon. Denne bakterien som er internalisert av fagocytose , blir mitokondriene , som for tiden er tilstede i alle aerobe celler. Det kan også bemerkes at mitokondrier har sitt eget DNA , som har alle egenskapene til bakterielt DNA ( sirkulært DNA ).
Utvikling av oksygenivået i jordens atmosfære
Dioksygen var nesten ikke-eksisterende i jordens atmosfære før arkaer og bakterier utviklet seg, sannsynligvis for rundt 3,5 milliarder år siden. Fristattsdioksygen dukket først opp i betydelige mengder under Paleoproterozoic (ca. 2,5 til 1,6 milliarder år siden). I løpet av de første milliarden årene kombineres alt oksygen som produseres av disse organismer med oppløst jern i havene for å danne jernbåndformasjoner . Når disse oksygenvasken er mettet, begynner det å frigjøres gratis oksygen fra havene for 2,7 milliarder år siden. Konsentrasjonen nådde 10% av sitt nåværende nivå for omtrent 1,7 milliarder år siden.
Tilstedeværelsen av en stor mengde oppløst oksygen i havene og i atmosfæren kan ha ført til utryddelsen av de anaerobe organismer som da lever, under den økologiske krisen som ble kalt den store oksidasjonen for ca. 2,4 milliarder år siden. Imidlertid tillater mobil respirasjon ved bruk av oksygen aerobe organismer å produsere mye mer ATP enn anaerobe organismer, og hjelper dem med å dominere jordens biosfære .
Siden begynnelsen av Kambrium for 540 millioner år siden har konsentrasjonen av oksygen i atmosfæren utviklet seg, og representerer over tid mellom 15% og 30% av volumet. Mot slutten av karbonformet for rundt 300 millioner år siden nådde det atmosfæriske oksygenivået et maksimum: det representerte da 35% av atmosfærens volum, noe som kunne ha bidratt til den store størrelsen på tidenes insekter og amfibier . Denne toppen av dens andel i jordens atmosfære på dette tidspunkt er på grunn av den enorme ekspansjon av de store fern skoger på Pangea , og til den gradvise deponering av organiske produkter som ble det kullforekomster . Menneskelige aktiviteter, inkludert forbrenning av 7 milliarder tonn fossilt brensel hvert år, har svært liten innvirkning på mengden fritt oksygen i atmosfæren. Med den nåværende hastigheten av fotosyntese vil det ta omtrent 2000 år å produsere alt oksygenet som er tilstede i atmosfæren i dag.
Biologiske roller
Fotosyntese
I naturen produseres gratis oksygen ved fotolyse av vann gjennom fotosyntese . I følge noen estimater gir grønne alger og cyanobakterier som finnes i det marine miljøet omtrent 70% av det frie oksygenet som produseres på jorden, og resten produseres av terrestriske planter . Andre estimater hevder at havenes bidrag til atmosfærisk oksygenforsyning er større, men andre hevder det motsatte, noe som tyder på at havene produserer omtrent 45% av atmosfærisk oksygen hvert år.
En global og forenklet formel som oversetter fotosyntese er skrevet:6 CO 2+ 6 H 2 O+ fotoner → C 6 H 12 O 6+ 6 O 2
eller ganske enkelt: karbondioksid + vann + sollys → glukose + oksygen.
Den fotolytiske evolusjonen av dioksygen forekommer i tylakoid av fotosyntetiske organismer og krever energien til fire fotoner . Mange av trinnene er komplekse, men resultatet er dannelsen av en elektrokjemisk gradient over thilakoid som brukes til å syntetisere adenosintrifosfat (ATP) via prosessen med fotofosforylering . Dioksygenet som er igjen etter oksidasjonen av vannmolekylet frigjøres i atmosfæren.
Puster
Dioksygen er viktig i cellulær respirasjon i alle aerobe organismer . De mitokondrier bruke den til å bistå i produksjon av ATP i ferd med oksidativ fosforylering . Reaksjonen som modellerer aerob respirasjon er generelt det motsatte av den modellerende fotosyntesen og er skrevet på en forenklet måte og i tilfelle av et utbytte av oksidasjonen av glukose med et utbytte på 100%:C 6 H 12 O 6+ 6 O 2→ 6 CO 2+ 6 H 2 O+ 2880 kJ mol −1 .Faktisk brukes energi under dannelsen av ATP (molekylet som tillater lagring av energi i cellen) fra ADP, så vel som for å tillate transport av molekylene som er nødvendige for denne reaksjonen inne i cellen. Dermed er energien som faktisk er lagret i form av ATP og derfor kan brukes av kroppen heller 1162,8 kJ for en mol glukose som forbrukes, det vil si:C 6 H 12 O 6+ 6 O 2→ 6 CO 2+ 6 H 2 O+ 1162,8 kJ mol −1 .Hos virveldyr diffunderer oksygen gjennom cellemembraner inn i lungene og røde blodlegemer . Den hemoglobin binder oksygen og forårsaker en fargeendring av proteinet som passerer fra blålig rød til lys rød. Andre dyr bruker ikke hemoglobin for transport av oksygen: bløtdyr og noen leddyr bruker hemocyanin mens edderkopper og hummer bruker hemerytrin . En liter blod kan oppløse 200 cm 3 av oksygen.
De reaktive derivater av oksygen , slik som ione- superoksid O to- og hydrogenperoksyd H 2 O 2, er giftige biprodukter av oksygen som brukes av organismer. Imidlertid produserer deler av immunsystemet til avanserte organismer peroksid, superoksid og singlet oksygen for å drepe invaderende mikroorganismer . Reaktive dioksygenderivater spiller også en viktig rolle i plantenes overfølsomme respons mot patogene angrep.
En hvilende voksen inhalerer mellom 1,8 og 2,4 gram oksygen per minutt. Dette tilsvarer over seks milliarder tonn oksygen innåndet av menneskeheten hvert år.
Den aerobe respirasjonen er å absorbere oksygenet som er nødvendig for katabolisme oksidativt og bidraget til energi til cellene. Organismer har en begrensende evne til absorpsjon , kalt maksimalt oksygenopptak .
Forbruket av oksygen er en indeks over mobil aktivitet. Denne bemerkningen er opprinnelsen til en karakterisering av den biologisk nedbrytbare forurensningen av en vannprøve, det biologiske oksygenbehovet .
Tilstedeværelse i kroppen av virveldyr
Det er i luftveiene enn partialtrykket av oksygen i kroppen av et levende virveldyr er den høyeste. Det er svakest i arteriene , deretter i perifere vev, og enda mer i venene . Deltrykket til dioksygen er trykket som dioksygen ville ha hvis det alene okkuperte det vurderte volumet.
| Enhet | Gasstrykk i lungealveolene |
Arteriell blodgass | Blodgass i venene |
|---|---|---|---|
| kPa | 14.2 | 11–13 | 4.0–5.3 |
| mmHg | 107 | 75–100 | 30-40 |
Struktur
Geometrisk struktur
Molekylet er diatomisk, og den gjennomsnittlige avstanden mellom de to atomene er 120,74 µm i grunntilstand.
I de to første spente tilstandene (se spektroskopidelen nedenfor) øker denne avstanden til 121,55 mikrometer i den første tilstanden og til 122,77 mikrometer i den andre.
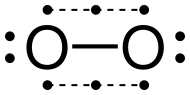
Representasjon av Lewis
Den nåværende Lewis-representasjonen av dioksygen, slik at de to atomene følger byte-regelen , er en dobbeltbinding , med hvert atom i tillegg to par ikke- delte elektroner . Imidlertid tar denne strukturen ikke hensyn til paramagnetismen til dette molekylet. Det er mulig å foreslå et Lewis-skjema som respekterer denne eksperimentelle observasjonen med en enkeltbinding (og ikke en dobbeltbinding) og et enkelt elektron per oksygenatom.
Den ukonvensjonelle representasjonen, med en enkeltbinding, har den ulempen at den ikke tar hensyn til den korte bindingsavstanden ( d = 120,74 pm ), mye kortere enn en enkelt OO-binding som i hydrogenperoksid. HOOH for hvilken bindingslengden er 145,7 um . Dette forklarer spesielt hvorfor denne strukturen i praksis bare brukes til pedagogiske formål, for å understreke molekylets diradiske natur . En mer effektiv beskrivelse oppnås med molekylære orbitaler .
Molekylært bane diagram
I det teoretiske rammeverket av molekylære orbitaler ( CLOA-metoden ) gjenspeiles samspillet mellom to oksygenatomer for å danne et molekyl i diagrammet motsatt.
De to 2s-orbitalene til de to oksygenatomene, opprinnelig med samme energi, gjennomgår degenerasjon og danner en binding σ 2s orbital og en σ-orbital*
2s antiliante, begge fullt opptatt, noe som resulterer i ingen binding mellom de to atomene. De seks 2p-orbitalene til de to atomene gjennomgår også degenerasjon, og danner tre σ 2px , σ 2py og σ 2pz- orbitaler og tre σ-orbitaler*
2px , σ*
2py og σ*
2pz anti-lim. De åtte (2 × 4) 2p-elektronene fordeles som følger:
- seks elektroner okkuperer de tre lavenergibindende orbitalene;
- de to gjenværende elektronene okkuperer hver sin antiliterende bane.
Denne kombinasjonen av 2p-orbitaler resulterer derfor i tre bindende molekylære orbitaler og en antiliante, altså en bindingsindeks på 2. Fordelingen av de to elektronene på de to antilaterende orbitalene forklarer også den diradiske naturen til dioksygen. Denne egenskapen til å være radikal mens antall elektroner i molekylene er jevn, er unik blant diatomiske molekyler. Denne fordelingen forklarer også den paramagnetiske karakteren av dioksygen, som ikke kan forutsies fra sin "klassiske" Lewis-representasjon.
Denne triplettilstandsstatusen gir molekylets magnetiske egenskaper (se nedenfor) og kan gjøres ansvarlig for kjemisk inertitet ved romtemperatur. Faktisk reaksjonen av O 2med et annet molekyl (H 2organiske molekyler) som nesten alltid er i en singlettilstand for å danne et molekyl i singlettilstanden, fortsetter uten bevaring av total spinn; Dette er årsaken til at kjemiske reaksjoner som involverer oksygen ved normal temperatur og trykk, er veldig langsomme.
Spektroskopi
De to første eksiterte nivåene av dioksygen er to singletilstander ved 15.800 cm -1 ( 94,72 kJ mol -1 ) og 21 100 cm -1 ( 157,85 kJ mol -1 ) (se diagram). Disse overgangene er spinn forbudt, noe som fører til at oksygen blir fargeløst. Dette er tilfelle i gassfasen, den blå fargen på atmosfæren skyldes Rayleigh-spredning .
Den blå fargen i flytende tilstand (se nedenfor) er resultatet av absorpsjon av to fotoner ved 7 918 cm -1 på en kombinasjon av to molekyler dioksygen ( O 4 dimer ).
Magnetisme
Dioksygen er paramagnetisk . Denne egenskapen ble observert av Faraday så tidlig som i 1848. Det oksygenmolekylære orbitale diagrammet sporet av CLOA-metoden gjenspeiler dette. Den elektroniske konfigurasjonen inneholder faktisk to enkeltelektroner på de to Π * orbitalene ( triplettilstand ).
I kjernemagnetisk resonans (NMR), for fine målinger, er det viktig å avfase prøven for å eliminere molekylært oksygen, som er paramagnetisk og vil forstyrre deteksjonen ved å få toppene til å utvide seg. Denne avgassingen oppnås generelt ved å boble en inert gass (nitrogen eller argon) i løsningen for å erstatte gassene oppløst av denne inerte og ikke-paramagnetiske gassen.
Produksjon
Industriell produksjon
Dioksygenet oppnås industrielt hovedsakelig (ved 95%) ved kryogen separasjon av forbindelser fra luft , det vil si ved kondensering av luft etterfulgt av fraksjonell destillasjon .
De kritiske temperaturene på nitrogen N 2( T c = −146,9 ° C ) og oksygen O 2( T c = −118.4 ° C ) tillater ikke flyting av luft ved enkel kompresjon . Luften må derfor komprimeres mellom 5 og 7 bar, deretter filtreres, tørkes, karboniseres ved adsorpsjon på en molekylsikt og til slutt avkjøles ved varmeveksling mellom den innkommende gassen og de flytende gassene. Kjøletapene kompenseres ved en utvidelse på 5 til 10% av den behandlede gassstrømmen, i en turbin hvis ytre arbeid er utvinnbart.
Destillasjonen utføres i den mest brukte prosessen i en dobbel kolonne som gjør det mulig å oppnå kontinuerlig rene gasser. Den første kolonnen (middels trykk, 5 bar) utfører en første separasjon av luften i ren gassformig nitrogengass (ved 99,999%) øverst og en væske rik på oksygen (ca. 40%) i bunnen. Denne væsken sendes deretter halvveis opp i den andre destillasjonskolonnen (lavtrykk, 1,3 bar). Oksygen O 2mellom 99,5% og 99,7% utvinnes ved bunnen av denne andre kolonnen. Den inneholder mindre enn 1 ppm nitrogen, den viktigste urenheten er argon .
Destillasjonskolonnene er mellom 1 og 6 m i diameter og måler 15 til 25 m i høyden. De er laget av rustfritt stål eller aluminium og har rundt hundre skuffer. Varmeisolasjonen utføres med perlit (utvidet silisiumsand). Å opprettholde kolonnens temperatur forbruker bare 6 til 7% av den totale energiforbruket.
Energiforbruket er 0,4 kWh m −3 gassformig oksygen, eller 50 til 60% av kostprisen.
Cirka 5% av industrielt oksygen produseres av en annen, ikke-kryogen prosess kalt VPSA ( Vacuum-press swing adsorption ) eller adsorpsjon ved vekslende trykk og vakuum.
Den omgivende luft blir tørket og renset ved filtrering, passerer så gjennom en kolonne av zeolitter som adsorberer nitrogen N 2 raskere.enn oksygen O 2. Zeolitter kan fiksere 10 liter nitrogen per kilo. Når de er mettet, sendes luften til en andre kolonne, mens dinitrogen fra den første kolonnen desorberes under vakuum. Renheten av dioksygenet som er oppnådd ved å fjerne nitrogen fra luften kan nå 90 til 95%. Dette dioksygen inneholder fortsatt 4,5% argon som, i likhet med dioksygen, ikke adsorberes. Energiforbruket er 0,4 til 0,5 kWh m −3 oksygen. Denne metoden brukes mer og mer i industrielle prosesser med behov under 100 tonn per dag, så vel som i åndedrettsvern som brukes hjemme. Se også Oksygenkonsentrator .
Oksygenet som produseres transporteres:
- i flytende eller gassform gjennom rørledninger kalt oksider eller oksygenrørledninger ;
- i gassform komprimeres i stålflasker eller tanker på 200 bar;
- i flytende form, i tankbiler .
I 1995 produserte åtte selskaper over hele verden nesten alt industrielt oksygen:
- Luftvæske (Frankrike): 17%;
- BOC (Storbritannia): 14% (kjøpt av Linde i 2006);
- Praxair (USA): 14%;
- Air Products (USA): 8%;
- Nippon Sanso (Japan): 7%;
- AGA (Sverige): 7% (kjøpt av Linde i 2000);
- Messer (Tyskland): 6%;
- Linde (Tyskland): 6%.
De viktigste produserende landene i 1996 var:
- USA: 27 millioner tonn;
- Japan: 12,7 millioner tonn;
- Frankrike: 3,23 millioner tonn.
Over hele verden var den totale produksjonen rundt 100 millioner tonn i 1996, eller 1 ⁄ 10 milliondel av oksygenet i atmosfæren.
I laboratoriet
Dioksygen har lenge blitt tilberedt i små mengder, i laboratoriet, ved reaksjon av oksylitten Na 2 O 2 med vann.
Den kan produseres ved katalytisk nedbrytning av hydrogenperoksid i nærvær av mangan ( IV ) oksid MnO 2.
Disse to produksjonsmetodene bruker vanligvis en vannforskyvningsenhet for å samle oksygen som produseres.
Det kan også tilberedes ved elektrolyse av vann til pedagogiske demonstrasjoner, men denne teknikken er langsom og kostbar i energi.
Reaktivitet
Dioksygen er termodynamisk veldig reaktiv, og de fleste av reaksjonene er sterkt eksoterme. Denne store reaktiviteten finner vanligvis ikke sted ved romtemperatur. De kinetiske årsakene er beskrevet ovenfor.
Med enkle kropper
Få enkle legemer kombineres ikke direkte med oksygen: wolfram W, platina Pt, gull Au og edelgasser . Det skal bemerkes at oksygenholdige forbindelser av edelgasser eksisterer imidlertid (XeO 3), men de kunne aldri oppnås ved direkte handling med O 2.
Det faktum at oksider eksisterer for nesten alle kjemiske elementer, hjalp i stor grad Mendeleev til å klassifisere elementene ( 1869 ). Videre var det faktum at visse grunnstoffer har flere forskjellige oksider (for eksempel nitrogen ), opprinnelsen til fremveksten av begrepet atom av Dalton ( 1800 ).
Ioner av O 2
Mange ioner av O 2 er kjent :
- dioxygenyl ion , O 2+ , i sjeldne forbindelser;
- superoksyd- ion , O 2- , hyppig anion i biologiske systemer der redoks ofte er monoelektronisk; det er en ustabil enhet;
- den peroksid ion O to2- , anion som er vanlig i metall-peroksyder så som bariumperoksyd BaO 2 ; dioksygen har samme grad av oksidasjon som i hydrogenperoksid H 2 O 2.
Singlet oksygenreaksjon 1 O 2
Singlet dioksygen produseres ved lysbestråling av triplet dioksygen (dets grunntilstand ) 3 O 2med et fotosensibilisator. For det må den eksiterte tilstanden til sistnevnte være større enn 94,7 kJ mol −1 (se spektroskopidelen ovenfor ).3 O 2+ 1 Sensitizer - hν → 1 O 2+ 3 Sensitizer.
Singlet dioxygen kan også produseres kjemisk, for eksempel i alkoholholdig oppløsning, med en blanding av hydrogenperoksid og blekemiddel :H 2 O 2+ ClO - → Cl - + H 2 O+ 1 O 2.
Singlet dioxygen er veldig reaktiv, både kjemisk og biologisk.
Bruker
Dioksygen, i luften, brukes til forbrenning (oppvarming, transport).
Separert fra nitrogen, er dens viktigste bruk i stålindustrien . Jernet som forlater masovnene er i form av Fe 3 C- karbid, ubrukelig fordi den inneholder mer enn 4 masseprosent karbon. Dette karbonet blir brent ved å injisere oksygen direkte i det smeltede jernet. Dette er prinsippet for omformere . 60 m 3 CNTP av O 2 er nødvendigper tonn jern. Forbruket av et stålverk er i tusen tonn O 2 per dag.
Den petrokjemiske er også en viktig forbrukeren når det gjelder å fremstille etylenoksyd , av propylenoksyd , av vinylklorid ved oksyklorering , ved raffinering av petroleumsprodukter, for regenerering av katalysatorer, etc.
Andre prosesser krever også store mengder oksygen:
- syntesen av titandioksid ved klorprosessen ;
- den bleking av massen , noe som begrenser forbruket klor Cl 2 som forblir i hovedblekemiddel;
- gjenbehandling av visse kjemiske avfall, for eksempel svovelholdige avfall fra produksjon av metylmetakrylat , som fører til utvinning av H 2 SO 4.
Andre sporadiske bruksområder er for eksempel:
- produksjon av flammer ved høy temperatur, slik som den for knall fakkel ;
- som medisinsk gass :
- Normobarisk oksygenbehandling (ved atmosfæretrykk): i åndedrettsassistanse av personer med pustevansker (sykdommer som astma eller kronisk respirasjonssvikt , eller under anestesi ), for kunstig ventilasjon ( stopp av puste ),
- hyperbar oksygenbehandling (høyt trykk): for behandling av visse gassforgiftninger (særlig karbonmonoksid ), dekompresjonsulykker ved dykking eller visse forbrenninger, visse arteritiske patologier.
-
Diagram over en omformer med tilførsel av oksygen direkte til det smeltede metallet.
-
Konverter i drift; reaksjonen av smeltet jern med oksygen produserer lysbyger.
-
Flaske medisinsk oksygen.
Diverse
Dioxygen er en del av Verdens helseorganisasjons modelliste over viktige medisiner (listen oppdatert iApril 2013).
Merknader og referanser
Merknader
- Den samme tvetydigheten gjelder mange andre grunnstoffer ( hydrogen , nitrogen , klor , etc. ).
- Karbondioksid frigjøres fra en annen del av hemoglobinet via Bohr-effekten .
- (1,8 gram / minutt per person) × (60 minutter / time) × (24 timer per dag) × (365 dager / år ) × (6,6 milliarder mennesker) ÷ (1.000.000 gram per tonn) = 6,24 milliarder tonn.
Referanser
- OXYGENE et OXYGENE (LIQUEFIED) , sikkerhetsdatablad (e) til det internasjonale programmet for sikkerhet for kjemiske stoffer , konsultert 9. mai 2009.
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Oppføring av CAS-nummer "7782-44-7" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), tilgang 28. januar 2009 (JavaScript kreves) .
- (en) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50.
- Referat fra den internasjonale komiteen for mål og vekt , 78 th Session, 1989, s. T1-T21 (og s. T23-T42, engelsk versjon).
- (in) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40.
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Innbundet ( ISBN 978-1-4200-9084-0 ).
- Indeksnummer i tabell 3.1 i vedlegg VI til EF-forordning nr . 1272/2008 (16. desember 2008).
- " Oksygen " i databasen over kjemiske produkter Reptox fra CSST (Quebec-organisasjonen som er ansvarlig for arbeidsmiljø og helse), åpnet 25. april 2009.
- Lavoisier A. (1789). Elementær avhandling om kjemi , 1864, s. 48 .
- (in) University of Wisconsin. (2006), Oppløst oksygen: liv i vann er avhengig av det , Water Action Volunteers-Volunteer Stream Monitoring Factsheet Series , les online (åpnet 25. februar 2010).
- " Hva var Jordens atmosfære som 4 milliarder år siden?" - notre-planete.info ” , på our-planete.info (konsultert 15. februar 2018 ) .
- (i) Heinrich D. Holland, "Oksygeneringen av atmosfæren og havene" , Phil. Trans. R. Soc. B , 361, 903–915, 19. mai 2006, DOI : 10.1098 / rstb.2006.1838 .
- Archean .
- Tidlig proterozoisk .
- Hoveddelen av proterozoikumet .
- Sen proterozoikum .
- fanerozoikum .
- (in) Neil A. Campbell og Jane B. Reece , Biology , San Francisco, Pearson-Benjamin Cummings2005, 7 th ed. , 1231 s. ( ISBN 0-8053-7171-0 ) , s. 522-23.
- (in) Scott Freeman , Biological Science, 2. , Upper Saddle River, NJ, Pearson-Prentice Hall,2005( ISBN 0-13-140941-7 ) , s. 214, 586.
- (en) Robert A. Berner , “ Atmosfærisk oksygen over fenerozoisk tid ” , Proceedings of the National Academy of Sciences i USA , vol. 96, n o 201999, s. 10955–57 ( PMID 10500106 , DOI 10.1073 / pnas.96.20.10955 , les online ).
-
DOI : 10.1111 / j.1472-4669.2009.00188.x
Dette tilbudet genereres i løpet av få minutter. Du kan hoppe over halen eller fullføre den for hånd . - (no) John Emsley , Nature's Building Blocks: An AZ Guide to the Elements , Oxford, England, Oxford University Press ,2001, 538 s. ( ISBN 0-19-850340-7 , leses online ) , s. 297-304.
- (in) Malcolm Dole , " The Natural History of Oxygen " , The Journal of General Physiology , vol. 49, n o 1,1965, s. 5-27 ( PMID 5859927 , DOI 10.1085 / jgp.49.1.5 , les online ).
- (i) William Fenical , "marine planter: en unik og Unexplored Resource" i planter: mulighetene for å ekstrahere protein, legemidler og andre nyttige kjemikalier (verksted saksbehandlingen) Diane ForlagsSeptember 1983( ISBN 1-4289-2397-7 , leses online ) , s. 147.
- (i) JCG Walker , The oxygensyklus i det naturlige miljø, og de kretsløp , Springer-Verlag ,1980.
- (i) Theodore L. Brown og Burslen LeMay , Chemistry: The Central Science , Prentice Hall / Pearson Education,2003( ISBN 0-13-048450-4 ) , s. 958.
- (en) Peter H. Raven , Ray F. Evert og Susan E. Eichhorn , Biology of Plants, 7. utgave , New York, WH Freeman and Company Publishers,2005( ISBN 0-7167-1007-2 ) , s. 115-27.
- “ Ingrediensene av livet på jorden og i rommet ” , European Space Agency (åpnet 28. juni 2013 ) , s. 3.
- (i) Albert Stwertka , til Elements Guide , Oxford University Press ,1998, 240 s. ( ISBN 0-19-508083-1 ) , s. 48-49.
- Charles A. Janeway og Paul Travers ( trans. Fra engelsk) Immunobiology: den grunnleggende og patologisk immunsystem , Paris / Brussel, De Boeck,2003, 784 s. ( ISBN 2-7445-0150-6 ) , s. 41.
- (in) " Strømningsbegrensning for måling av luftveisparametere " , Patenstorm (åpnet 28. juni 2013 ) : " For mennesker er det normale volumet 6-8 liter per minutt. " .
- (i) Charles Henrickson , Chemistry Cliffs Notes2005, 440 s. ( ISBN 0-7645-7419-1 ).
- Resultat oppnådd fra verdien i mmHg ved bruk for konvertering 0,133 322 kPa / mmHg .
- (in) ' Normal Reference Range Table " , University of Texas Southwestern Medical Center, Dallas (åpnet 28. juni 2013 ) .
- (in) " The Medical Education Division of the Brookside Associates → ABG (Arterial Blood Gas) " (åpnet 28. juni 2013 ) .
- Elementets kjemi , s. 606.
- (in) NN Greenwood og A. Earnshaw, Chemistry of the Elements , Boston Oxford, Butterworth-Heinemann,1997, 2 nd ed. ( 1 st ed. 1984), 1341 s. ( ISBN 978-0-7506-3365-9 , OCLC 804401792 ) , s. 615.
- Vigne J.-L., Industrielle data .
- (in) WHO Model List of Essential Medicines, 18. liste , april 2013.
Se også
Relaterte artikler
Bibliografi
- Davis JC (1975), vannbårne krav og kriterier for oppløst oksygen med særlig vekt på det kanadiske miljøet , i Associate Committee on Scientific Criteria for Quality , National