Organomagnesium
En organomagnesium er en organisk forbindelse med en karbon - magnesium -binding . Dette er en viktig familie av organometalliske forbindelser i organisk syntese fordi den inkluderer Grignards reagenser , som er blandede organomagnesiums med formen R - Mg X , hvor R er en karbonkjede og X er et halogen , generelt brom. Eller klor , noen ganger jod - fluor blir vanligvis ikke brukt på grunn av den for lave polarisasjonsevne av difluor F 2. Disse reagensene er mye brukt i bransjen, og deres oppdagelse på slutten av XIX - tallet av den franske kjemikeren Victor Grignard har gjort det mulig å få Nobelprisen for kjemi i 1912 fordi de kan binde et bredt utvalg av byggesteiner til organiske molekyler .
I tillegg til Grignard-reagenser, organomagnesiumforbindelser innbefatter molekyler, slik som dimetylmagnesium (CH 3 ) 2- Mg-, Dibutylmagnesium (CH 3 CH 2 CH 2 CH 2 ) 2 Mgeller antracen-magnesium .
Organometallisk karakter av R - Mg - X
Carbon har en elektro sterk: . Og det merker vi også . Dette fysiske faktum pålegger derfor polarisering av C - M: C — M- koblingen . Vi merker en inversjon av polariteten til de klassiske karbonbindinger: i en organometallisk bærer karbonet en ladning (dette karbonet kalles karbanion), dessuten er denne bindingen 35% ionisk, noe som vil tillate reaksjon med for eksempel et halogenidalkyl ( R —X ) skaper en karbon-til-karbonbinding .
Organomagnesium er en av de sterkeste Brönsted- basene innen organisk kjemi med en pKa i størrelsesorden 40 til 60. R-Mg-X er en kraftig nukleofil .
Syntese av organomagnesium
På grunn av deres ekstreme basalitet, eksisterer ikke organomagnesium naturlig. De samlede resultatene av syntesen er som følger:
Driftsmodus
Den syntese av organomagnesium er delikat: det reaksjonsmediet må være vannfrie, på grunn av egenskapene til det ønskede produkt; reaksjonen er sterkt eksoterm og løsningsmidlet er flyktig og brannfarlig. Feil håndtering resulterer også i opprettelsen av et parasittisk produkt - kalt “ Wurtz Coupling ”.
Nødvendige materialer :
- Tricolor ball;
- Isobarisk støptrakt;
- Reflux kondensator;
- Holder CaCl 2 (eller arbeide under en inert atmosfære);
- Magnetomrører med oppvarming;
- Magnesiumspon;
- Dietyleter eller vannfri THF;
- Halogenerte derivater;
- Bain marie så kaldt vann.
Driftsmodus
- Utfør en tilsetningsenhet med tilbakeløp, med beskyttelse av reaksjonsmediet mot luftfuktighet, og ved å plassere en ovoid magnetstang i den trehalsede kolben.
- Plasser magnesiumsponene, som tidligere har blitt aktivert i ovnen, i trikolen. Dekke dem med noen få cm 3 vannfri etyleter. Tilsett en liten krystall med diode.
- Kondens hellestrakten med løsningen av det halogenerte derivatet i vannfri etyleter, og stopp den med en glasspropp.
- Hell noen dråper av halogenidløsningen på magnesiumsponene, vent noen minutter på observasjon av misfarging i reaksjonsmediet.
- Når jodfargen har forsvunnet i reaksjonsmediet, varmes det opp i et vannbad for å få tilbakeløp, og hell halogenid langsomt og dråpe for dråpe mens du omrører magnetisk.
- Når tilsetningen er fullført, oppvarm reaksjonsmediet til tilbakeløp for å oppnå en fullstendig reaksjon.
Kommentarer
For å forhindre at en Würtz-kobling oppstår mellom det syntetiserte organomagnesium og halogenidet. Fra reaksjonens start koker eteren: tilbakeløpet tjener til å kondensere eterdampene som strømmer i kolben; tilbakeløpet skal også holdes veldig lavt for ikke å skape den parasittiske reaksjonen nevnt ovenfor. Det er ikke nødvendig å varme opp hele manipulasjonen fordi reaksjonen er veldig eksoterm .
Den endelig oppnådde løsningen har generelt en ganske lys grå farge.
Løsemiddel
Eter spiller en dobbelt rolle her, det oppløser organo-magnesium dannet og stabiliserer den, organomagnesiumforbindelsen er her en Lewis-syre, oppløsningsmidlet her spiller rollen av Lewis-basen , og dermed de ikke-bindende dubletter av oksygen går til å stabilisere det reaktive sentrum magnesium . Det er for eksempel mulig å bruke dietyleter , ellers THF - tetrahydrofuran , jfr. figuren nedenfor.

Miljøet der organomagnesium er badet må være helt vannfritt: vann / RMgX-reaksjonen er livlig.
Reaktivitet av organomagnesium
Reaksjoner på vanlige organiske forbindelser
På vannetOmsetningen av organomagnesiums på vann er meget livlig (det er en syre-base-reaksjon : p K en (RH / R-) = 50), og eksoterm. Dette er grunnen til at driftsmodusen krever total dehydrering av luften i glassutstyret, så vel som overflatene og løsningsmidlene. Med unntak av spesielle tilfeller anses denne reaksjonen å være parasittisk, og fører til ødeleggelse av organomagnesium.
Reaksjonen av organomagnesium på vann er som følger:
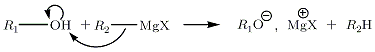 Med karboksylsyrer
Med karboksylsyrer
 Med aminer
Med aminer
 Med terminale alkyner
Med terminale alkyner

Nukleofile substitusjonsreaksjoner
Nukleofil substitusjon, eksempel på I 2Vi foreslår den nukleofile substitusjonen av RMgX på I 2 (polariteten til dette molekylet er indusert).
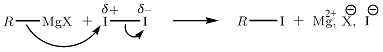 Nukleofil erstatning med halogenerte derivater
Nukleofil erstatning med halogenerte derivater
Halogenert derivat: R'-X-mekanisme: SN2
R-MgX + R'-X -> RR '+ MgX2
Merk: fungerer bra med RI og Ar-CH2X da de stabiliseres av induktiv effekt for RI og mesomer for Ar-CH2X
Reaksjon på epoksyerMekanisme: SN2
I eteren:
R ---- Mg ---- X + O (CH2) 2 (syklus) → R-CH2-CH2-O-Mg-X
Deretter H3O + syrehydrolyse:
R-CH2-CH2-O-Mg-X + H + → R-CH2-CH2-OH + MgX +
Nukleofile addisjonsreaksjoner ...
... på aldehyder og ketoner- På aldehyder :

Reaksjonen mellom organomagnesium- og aldehyder fører til dannelsen av en sekundær alkohol, dersom R 1 og R 2 kjeder inneholder minst en karbon. Hvis det bærende karbonet i den endelige alkoholgruppen er asymmetrisk, dvs. hvis de to R- kjedene er forskjellige, vil produktet være sammensatt av de to isomerer med R- og S-konfigurasjon.
- På ketoner :

Denne reaksjonen fører til dannelsen av en tertiær alkohol. Når det gjelder aldehyder, hvis det dannede karbon er asymmetrisk, oppnås en R / S 50/50 blanding; dermed er det ingen stereoselektivitet. En studie av reaksjonsmekanismen viser at det faktisk er et syklisk mellomprodukt:

- Spesielt tilfelle av syntesen av en primær alkohol :
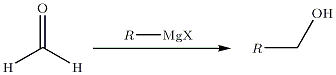 ... på estere
... på estere
Reaksjonen er lik reaksjonen på et keton. Etter hydrolyse får vi hemiacetal på en mellomliggende måte ;
Dette er ustabilt, det gjennomgår eliminering som fører til et keton. Det tilstedeværende organomagnesium vil reagere kjemoselektivt med ketonet før esteren, noe som er mindre reaktivt fordi karbonkjernen til karbonylen er noe maskert av de ikke-bindende elektronene til oksygenet bundet av en enkeltbinding. Den samlede vurderingen av reaksjonen fører derfor til dannelsen av en tertiær alkohol, uten mulighet for å isolere det mellomliggende keton.
... på acylkloriderReaksjonen ligner på reaksjonen på et keton, men raskere fordi karbonkjernen bundet til klor viser en positiv ladning som er mer attraktiv for organomagnesiumradikalen.
R ---- Mg ---- X + R'-CO-Cl → R'-CO-R + Cl-Mg-X
Reaksjonen fører derfor til dannelsen av et isolerbart keton hvis det ikke er for mye organomagnesium. Denne ustabile ketonen vil reagere med organomagnesiummidlet som er i reaksjonsmediet i henhold til følgende reaksjon: R'-CO-R + RMgX → R-R'COMgX-R og deretter får vi under virkningen av H2O en tertiær alkohol. Hvis vi vil stoppe på ketonstadiet, må vi operere ved -65 ° C
... på CO 2
Bruk av karbondioksid i form av tørris . Reaksjonen ved -40 ° C fører til dannelsen av en karboksylsyre R-COOH.
Merknader og referanser
- Victor Grignard , " Om noen nye organometalliske kombinasjoner av magnesium og deres anvendelse på synteser av alkoholer og hydrokarboner ", ukentlige rapporter om øktene til Académie des sciences , vol. 130, 1900, s. 1322-1325 ( les online )
- (in) " Nobelprisen i kjemi i 1912 " (åpnet 27. oktober 2018 ) .




