Aldehyde
Et aldehyd er en organisk forbindelse , som tilhører familien av karbonylforbindelser , et av atomene av karbon primært (forbundet med høyst ett karbonatom) i karbonkjeden bærer en karbonylgruppe. Et aldehyd inneholder derfor sekvensen:
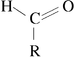 (R representerer en karbonkjede.)
(R representerer en karbonkjede.)
Det enkleste aldehydet (R redusert til enkelt H-atom) er formaldehyd (eller metanal ), også kalt formalin når det er i vandig løsning:
Et aldehyd er formelt avledet fra en primær alkohol ( oksidasjon ) der hydroksydgruppen -OH er i enden av kjeden og dannes etter fjerning av to H-atomer, derav navnet " al cool de s hyd rogéné" eller aldehyd .
Nomenklatur
Aldehydet vil ha navnet på den tilsvarende alkanen, som tillegges suffikset "-al". For resten er reglene de samme som angitt for alkener . Når aldehyd utgjør den prioriterte funksjonelle gruppen til molekylet, er det ikke nødvendig å tilordne en posisjonsindeks til det, siden det alltid er i terminalposisjonen (1).
CH 3 - CHO: ethanal
CH 3 - CH (CH 3 ) - CH 2 - CHO: 3-metylbutanal
Når aldehydet er en substituent på en syklisk forbindelse som benzen , bærer den deretter navnet karbaldehyd eller karboksaldehyd som er to ekvivalente termer. For eksempel kan følgende forbindelse kalles benzen karbaldehyd eller benzen karboksaldehyd (det vanlige navnet benzaldehyd er også akseptert):
C 6 H 5 - CHO
Når aldehydgruppen ikke er prioritert, tildeles den et prefiks av alkanoylformen . For eksempel kalles følgende forbindelse ethanoylbenzensulfonsyre :
OHC - CH 2 - C 6 H 5 - SO 3 H
Hovedaldehyder
| Methanal | Ethanal | Propanal | Butanal | Pentanal |
| VSH 2 O | C 2 H 4 O | C 3 H 6 O | C 4 H 8 O | C 5 H 10 O |
Egenskaper, reaktivitet
De er vanligvis vanlige for aldehyder og ketoner (se karakteristikkene av karbonylforbindelsen ).
Produksjon og syntese
Ved hydroformylering
Også kalt okso prosess , blir denne reaksjon anvendes for å oppnå C 3 -C 19 -aldehyderfra alkener er det hovedprosessen for produksjon av butanal . Anvendes karbonmonoksyd og dihydrogenfosfat ved et trykk på 10 til 100 atmosfærer og en temperatur på 40 for å 200 ° C i nærvær av en katalysator (et overgangsmetall , for eksempel rhodium ).
Ved oksidasjon av alkoholer
Aldehyder oppnås ved oksidasjon av primære alkoholer og ketoner ved oksidasjon av sekundære alkoholer (tertiær alkohol kan bare oksidere under ekstreme forhold, det regnes ofte som ikke-oksiderbar).
Denne oksidasjonen involverer derfor redoks-paret:
Imidlertid er aldehyder fortsatt gode reduksjonsmidler. De oksyderes derfor veldig lett til karboksylsyrer :
Det er til og med et tilfelle der reaksjonen fortsetter: metanol. Den oksyderer først til metanal, deretter til metansyre og til slutt til karbondioksid.
- oksidasjon av O 2 luft
Katalysatoren kan anvendes som Fe 2 O 3 eller MnO 3 til 400- C , eller en sølvkatalysator til 600 ° C .
- Katalytisk dehydrogenering av primære alkoholer
Alkohol er kullsyreholdig. CuO rundt 400 til 500 ° C , Ag, Cu rundt 300 ° C , ZnO eller ZrO rundt 300 til 400 ° C blir brukt som katalysator .
- En metode fra Hoechst-Wacker
Oksidasjon av etylen til acetaldehyd
Kjemisk oksidasjonEn "mild" oksidant må brukes under strenge driftsforhold for å unngå den andre oksidasjonen. Generelt brukes et krom VI-derivat i støkiometriske proporsjoner. Det er to historiske metoder:
- For aldehyder som har et kort karbonkjede, og som derfor er mer flyktig, kaliumdikromat K 2 Cr 2 O blir 7 anvendes , i et surt medium, ved en temperatur over kokepunktet av aldehydet, som tillater dens utvinning etter trening.
- For de andre aldehyder, Sarett-reagens, som består av seksverdig krom-trioksyd CrC 3 i pyridin , ved lav temperatur ( 0 ° C ) benyttes.
Imidlertid er pyridin- og kromforbindelser veldig giftige og kan ikke lenger brukes. Andre metoder er utviklet:
- Den PCC og PDC, alltid basert på krom, men i mindre mengder;
- Aktiverte DMSO-metoder (inkludert Swerns oksidasjon );
- Periodater ( Dess-Martin reagenser , IBX).
Ved ozonolyse av alkener
Aldehyder kan oppnås ved ozonolyse av alkener. Det er viktig å bruke et reduserende tilsetningsstoff under reaksjonen, slik som et sulfid (konvensjonelt dimetylsulfid) eller et fosfin (trifenylfosfin, mindre luktende enn svovelforbindelser), for å fange de oksiderende biproduktene (hydrogenperoksid). Ellers observeres overoksidering av aldehydet til karboksylsyre .
bruk
Aldehyder er veldig kraftige syntetiske produkter som uavhengig av sin egen lukt gir en stor diffusjonskraft til sammensetningene. I parfymeri gjelder dette hovedsakelig alifatiske aldehyder. Oppdagelsen av aldehyder ga skaperne en ny palett. Deres markante bruk er opprinnelsen til parfymer av den såkalte "Aldehyde" -typen. Aldehyder brukes som et desinfeksjonsmiddel og ved fremstilling av organisk tilberedning. Aldehyder og ketoner brukes til fremstilling av plast, løsemidler, fargestoffer, parfymer og medisiner. For eksempel har aldehyd C 17 en kirsebærlukt.
Acetalisering
Den acetaliseringen er en reversibel reaksjon for å transformere en karbonylforbindelse og to alkoholer (eller diol) i acetal . Denne reaksjonen beskytter faktisk karbonylgruppen, eller alkoholen.
Reaksjon- Varmeapparat
- Syrekatalyse (generelt APTS )
- Når et aldehyd brukes, kalles det oppnådde produktet "acetal". Når vi bruker keton, kaller vi produktet ”ketal”. Imidlertid blir begrepet acetal mer og mer brukt som et generisk begrep for å betegne de to produktene. På den annen side kalles reaksjonen (både for aldehyder og for ketoner) alltid "acetalisering".
- Denne reaksjonen er generelt til fordel for acetal (i motsetning til ketaler).
Hvis vi ønsker å fremme det i denne retningen, bruker vi et overskudd av alkohol (som samtidig fungerer som løsningsmiddel), og vi kan også destillere vannet (heteroazeotrop destillasjon) ved hjelp av apparatet fra Dean og Stark . For å fremme omvendt reaksjon er det motsatt: vi legger et overskudd av vann for å hydrolysere acetal.
- Når vi ønsker å beskytte karbonylfunksjonen, bruker vi vanligvis en diol, som etan-1,2-diol :
- Denne reaksjonen kan også meget godt tjene til å beskytte en alkoholfunksjon, spesielt vicinaldiolene .
- I noen tilfeller kan reaksjonen stoppe med hemiacetal (tilfelle sykliske hemiacetals).
Virkning av et Grignard-reagens
Et Grignard-reagens reagerer med et aldehyd og danner en sekundær alkohol (→ reaksjon ).
Wittig-reaksjon
Det Wittig-reaksjonen omdanner et aldehyd inn i en etylen-derivat. Det gjør faktisk C = O-bindingen til en C = C-binding.
Reduksjon av aldehyder
I alkoholer IndustrieltDen brukte dihydrogen H 2 i et inert oppløsningsmiddel i nærvær av en katalysator ( heterogen katalyse ). Dette er veldig ofte metaller, slik som platina (Pt), palladium (Pd), nikkel (Ni) eller rodium (Rh). Hvis aldehydet noen gang også har en C = C-binding, blir dette også hydrogenert (reaksjonen er lettere på C = C enn på C = O). reaksjonen er eksoterm .
Av hydridesDIBAL kan brukes til reduksjon av aldehyder til alkohol.
I alkanAnerkjennelsestester
For å demonstrere tilstedeværelsen av aldehyd, kan vi gjøre en gjenkjenningstest:
- Tilsetning av forbindelsene med Z-NH 2 (amin) Type: dannelse av et bunnfall.
- Testen til Fehlings løsning som tar en murstein rødglødende i nærvær av aldehyd.
- Den såkalte " silver mirror " -testen, ved bruk av Tollens 'reagens, og resulterte i dannelsen av et solid sølvavleiring.
- Schiff's reagens test , som når den er kald, farger løsningen rosa.
Men disse metodene som bruker kjemiske reaksjoner med aldehydet ødelegger det. Spektrometri-metoder (NMR og infrarød) som gjør det mulig å oppdage denne funksjonen uten å ødelegge prøven, blir nå lettere brukt.