Diborane
| Diborane | |||
| |||
 | |||
| Struktur av diboran | |||
| Identifikasjon | |||
|---|---|---|---|
| IUPAC-navn | diboran (6) | ||
| Synonymer |
boranylidyneboran |
||
| N o CAS | |||
| N o ECHA | 100.039.021 | ||
| N o EC | 242-940-6 | ||
| N o RTECS | HQ9275000 | ||
| PubChem | 6328200 | ||
| ChEBI | 33590 | ||
| SMIL |
[BH2] 1 [H] [BH2] [H] 1 , |
||
| InChI |
InChI: InChI = 1 / B2H6 / c1-2 / h1-2H3 Std. InChI: InChI = 1S / B2 / c1-2 Std. InChIKey: ZOCHARZZJNPSEU-UHFFFAOYSA-N |
||
| Utseende | Komprimert, fargeløs gass med en karakteristisk lukt. | ||
| Kjemiske egenskaper | |||
| Brute formel | B 2 H 6 | ||
| Molarmasse | 27,67 ± 0,014 g / mol H 21,86%, B 78,14%, |
||
| Fysiske egenskaper | |||
| T ° fusjon | −165 ° C | ||
| T ° kokende | −92 ° C | ||
| Løselighet | i vann: hydrolysert til hydrogen og borsyre | ||
| Volumisk masse | 1,18 kg · m -3 til 15 ° C | ||
| Selvantennelsestemperatur | 40 til 50 ° C | ||
| Flammepunkt | 38 ° C | ||
| Eksplosjonsgrenser i luft | 0,8 - 88 % vol | ||
| Kritisk punkt | 40,5 bar , 289,8 k | ||
| Termokjemi | |||
| Δ vap H ° | 14,28 kJ · mol -1 ( 1 atm , -92,49 ° C ) | ||
| Forholdsregler | |||
| SGH | |||
   Fare H220, H280, H330, P210, P260, P304, P315, P340, P377, P381, P403, P405, H220 : Ekstremt brannfarlig gass H280 : Inneholder gass under trykk; kan eksplodere ved oppvarming H330 : Dødelig ved innånding P210 : Holdes borte fra varme / gnister / åpen ild / varme overflater. - Røyking forbudt. P260 : Unngå innånding av støv / røyk / gass / tåke / damp / spray. P304 : Ved innånding: P315 : Søk øyeblikkelig legehjelp. P340 : Flytt personen i frisk luft og hold deg i ro i en stilling som er behagelig å puste. P377 : Lekkasje på antennet gass: Ikke slukk hvis lekkasje ikke kan stoppes trygt. P381 : Fjern alle antenningskilder hvis det kan gjøres uten risiko. P403 : Oppbevares på et godt ventilert sted. P405 : Oppbevares låst. |
|||
| NFPA 704 | |||
| 4 4 3 W | |||
| Transportere | |||
263 : giftig gass, brannfarlig FN-nummer : 1911 : DIBORANE, KOMPRIMERT Klasse: 2.3 Etiketter: 2.3 : Giftige gasser (tilsvarer gruppene betegnet med store bokstaver T, dvs. T, TF, TC, TO, TFC og TOC) . 2.1 : Brennbare gasser (tilsvarer gruppene betegnet med hovedstad F);   |
|||
| Økotoksikologi | |||
| Luktterskel | lav: 1,8 spm høy: 3,5 spm |
||
| Enheter av SI og STP med mindre annet er oppgitt. | |||
Den diboran er en kjemisk forbindelse med formel B 2 H 6. Dette molekylet , bestående av bor og hydrogen , et resultat av foreningen av to borangrupper BH 3koblet av to av deres hydrogenatomer. Det må ikke forveksles med diboran (4) , med formel B 2 H 4, hvor de to boratomer er bundet av en kovalent binding ; diboran er noen ganger referert til som diboran (6) for å skille den fra denne forbindelsen.
Ved romtemperatur er det en fargeløs gass med en søt lukt som lett antennes i nærvær av fuktighet. Det danner svært eksplosive blandinger med luft. Det er en viktig borforbindelse med forskjellige bruksområder. Dannelsen er endoterm og den frie entalpi av dannelsen er positiv ( 36 kJ · mol -1 ) . Diboran har derfor tendens til å dekomponere, frigjør hydrogen H 2 , men med ganske treg kinetikk .
Egenskaper og struktur
Diborane er en fargeløs gass lettere enn luft; den kondenserer ved −92,5 ° C under 101,3 kPa ; dens tetthet er 421 g · m -3 og dens latente fordampningsvarme er 515,39 kJ · mol -1 . Det stivner ved -165 ° C . Ved 15 ° C , det mettede damptrykket er 3,94 MPa og forholdet mellom volumene av gass og væske er lik 362. Gassformet, er det meget brennbart og kan føre til voldsomme eksplosjoner spontant i luft. Dens kritiske punkt er ved 16,6 ° C og 4,053 MPa .
Diboran dekomponerer langsomt selv ved romtemperatur, til hydrogen og høyere bor- hydrider . Denne nedbrytningen akselererer med økende temperatur. Diborane er følsom for fuktighet og hydrolyserer umiddelbart til hydrogen og borsyre H 3 BO 3 etter den eksoterme reaksjonen:
B 2 H 6+ 6 H 2 O→ 2 H 3 BO 3+ 6 H 2.Ved kontakt med litium og aluminium danner diboran hydrider som kan antennes spontant. Det trenger ikke ha en korroderende virkning på vanlige metaller , men angrep fleste gummi og plast , med unntak for eksempel polytetrafluoretylen [CF 2 -CF 2 ] nog polyklortrifluoretylen [CClF-CF 2 ] n.
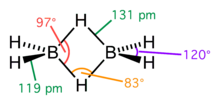
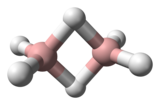
Diborane har en D 2h geometrimed to bindende hydrogenatomer og fire terminale hydrogenatomer. De bindinger mellom boratomer og terminal hydrogen er konvensjonelle (et par av elektroner som er involvert i hver BH-binding, danner en kovalent binding ), men de mellom boratomer og bindehydrogenatomer er av en annen art (et par av elektroner som er involvert i hver BHB bro , danner en tre-senter, to-elektronbinding ). Lengden på disse bindingene er derfor forskjellig: 119 μm for terminal BHs, men 133 μm for BH-bindingene til BHB-broene, noe som betyr at styrken til disse bindingene også er forskjellig (svakere i BHB-broen enn i terminalen BH knytte bånd).
Den gallium danne en forbindelse med lignende struktur: digallane Ga 2 H 6.
Klargjøring av diboran
Diborane er en sentral forbindelse i borkjemi og har derfor blitt studert spesielt, slik at mange synteser eksisterer. De fleste preparater bruker hydrider med halogenider eller alkoholater. Industriproduksjon bruker bortrifluorid BF 3 :
2 BF 3+ 6 NaH→ B 2 H 6+ 6 NaFTo laboratoriepreparater bruker bortriklorid BCl 3med litiumtetrahydruroaluminat LiAlH 4, eller bortrifluorid BF 3med natriumborhydrid NaBH 4 ; disse to metodene har et utbytte på 30% diboran:
4 BCl 3+ 3 LiAlH 4→ 2 B 2 H 6+ 3 LiAlCl 4 4 BF 3+ 3 NaBH 4→ 2 B 2 H 6+ 3 NaBF 4Oksidasjon av borhydridsalter kan brukes til å fremstille små mengder:
2 NaBH 4+ I 2→ 2 NaI+ B 2 H 6+ H 2Reaksjoner og bruk
Diborane er et reagens som finner et stort antall applikasjoner. Reaksjonene der det griper inn involverer ofte Lewis-baser for å gi nye molekyler. Det reagerer med ammoniakk til skjema borazane BH 3 NH 3eller borazin B 3 N 3 H 6 avhengig av driftsforholdene.
Det har blitt studert som drivmiddel i rakettdrift (med fluorerte oksidanter som fluor F 2og OF 2 oksygen difluorid), for vulkanisering av elastomerer , som en katalysator i polymeriseringen av organiske monomerer, for å øke flammehastigheten, som et dopemiddel i halvlederindustrien og som et reagens for produksjon av ultrarent silisium beregnet på elektroniske kretser.
Merknader og referanser
- DIBORANE , sikkerhetsark (er) til det internasjonale programmet for sikkerhet for kjemiske stoffer , konsultert 9. mai 2009
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- " Properties of Various Gases ", på flexwareinc.com (åpnet 12. april 2010 )
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Innbundet ( ISBN 978-1-4200-9084-0 )
- Oppføring "Diborane" i den kjemiske databasen GESTIS fra IFA (tysk instans ansvarlig for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 14. september 2011 (JavaScript kreves)
- " Diborane " , på hazmap.nlm.nih.gov (åpnet 14. november 2009 )
- Som gir høy effekt hypergolic driv : 372 s av spesifikk impuls for OF to driv/ B 2 H 6, nå forlatt fordi det er dyrt og frigjør giftige produkter.
