Arylhalogenid
I organisk kjemi er arylhalogenider eller haloarener en klasse av organiske forbindelser avledet fra arener (aromatiske hydrokarboner) hvor minst ett av hydrogenatomene har blitt substituert med et halogenatom ( fluor , klor , brom) eller jod ). Som sådan er de et spesielt tilfelle av aromatiske halogenider som omfatter minst ett halogen og en aromatisk ring, men ikke nødvendigvis ett halogen på den aromatiske ringen.
Arylhalogenider skilles fra alkylhalogenider ved forskjellige egenskaper og fremgangsmåter for fremstilling. Den mest studerte undergruppen og med flest forbindelser i dagens bruk er utvilsomt den for arylklorider.
Halogenbenzener
De enkleste forbindelsene som tilhører denne familien er halogenbenzener eller monohalogenbenzener, de halogenerte derivater av benzen .
| Representasjon |

|

|

|

|
| Etternavn | Fluorbenzen | Klorbenzen | Brombenzen | Jodbenzen |
| Fusjonspunkt | −42 ° C | −45,2 ° C | −31 ° C | −29 ° C |
| Kokepunkt | 85 ° C | 132 ° C | 156 ° C | 188 ° C |
| Kompakt modell |

|

|

|

|
Eiendommer
Fysiske egenskaperMonohalobenzener er fargeløse væsker, hvis kokepunkter øker kraftig med molær masse. Omvendt varierer smeltepunktene mindre brått, klorbenzen har til og med et litt lavere smeltepunkt enn fluorbenzen ( -45,2 ° C mot -42 ° C ).
Kjemiske egenskaperEn karakteristisk reaksjon av arylhalogenider, og spesielt halogenbenzener, er aromatisk nukleofil substitusjon .
Arylhalogenider kan reagere med magnesium for å danne de tilsvarende Grignard (blandede organomagnesium) reagensene .
Syntese
Klorbenzen og brombensen kan oppnås ved halogenering av henholdsvis benzen i nærvær av klor eller dibrom og av en Lewis-syre .

På den annen side fungerer ikke denne typen reaksjon med fluor, som er altfor reaktiv, og produserer blant annet multifluorerte forbindelser, og heller ikke med jod som tvert imot ikke er tilstrekkelig reaktivt.
Klorbenzen, brombenzen og jodbenzen kan oppnås ved Sandmeyer-reaksjon , fra anilin- og halogenerte kobbersalter:

Fluorbenzen kan produseres ved Balz-Schiemann-reaksjonen :

Dihalogenbenzener
Det er ti forbindelser som er dihalogenerte fra benzen. Hver av disse forbindelsene eksisterer som tre isomerer , orto , meta og para .
| Fluorbenzen (–F) | Klorbenzen (–Cl) | Brombenzen (–Br) | Jodbenzen (–I) | |
| Fluorbenzen (–F) | Difluorbenzen | Klorfluorbenzen | Bromfluorbenzen | Fluorjodbenzen |
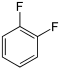  |
  
|
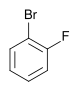 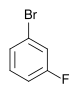 
|
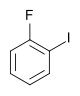 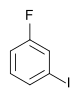 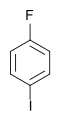
|
|
| Klorbenzen (–Cl) | Diklorbenzen | Bromklorbenzen | Klorjodbenzen | |
 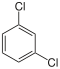 |
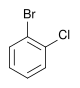  
|
 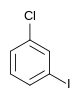 
|
||
| Brombenzen (–Br) | Dibrombenzen | Bromoiodobenzene | ||
  |
 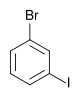 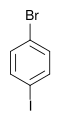
|
|||
| Jodbenzen (–I) | Diiodbenzen | |||
 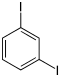 | ||||
Halogenbenzener med andre funksjonelle grupper
Benzenderivater med konvensjonelle funksjonelle grupper, slik som fenol ( hydroksylgruppe ), anilin ( amingruppe ), anisol ( metoksylgruppe ), toluen ( metylgruppe ), nitrobenzen ( nitrogruppe ), l ' benzylalkohol (hydroksymetyl), benzaldehyd ( gruppe karbonyl ), kan benzoesyren også være substituert med halogen. Generelt er navnet på derivatet ganske enkelt navnet på moderforbindelsen foran prefikset halogen-. Når det er en disubstituert benzen, eksisterer den som de tre isomerer orto , meta og para .
På grunn av den -I effekten av halogen, halofenoler og halobenzoic syrer har en høyere surhetsgrad i forhold til den ikke-halogenforbindelse, og derfor har en lavere p K A (fenol: 9,99, halogenfenol: 9, 06, benzosyre: 4,20, halobenzoic syre: 3,58).
| –F | –Cl | –Br | -JEG | |
|---|---|---|---|---|
| Fenol (–OH) | Fluorfenol | Klorfenol | Bromfenol | Jodofenol |
| Aniline (–NH 2 ) | Fluoroanilin | Kloranilin | Bromoanilin | Jodoanilin |
| Anisole (–OCH 3 ) | Fluoranisole | Kloroanisol | Bromoanisole | Jodoanisole |
| Toluen (–CH 3 ) | Fluorotoluen | Klortoluen | Bromotoluen | Jodotoluen |
| Nitrobensen (–NO 2 ) | Fluoronitrobenzen | Kloritrobenzen | Bromonitrobenzen | Joditrobenzen |
| Benzylalkohol (-CH 2 OH) | Fluorbenzylalkohol | Klorbenzylalkohol | Brombenzylalkohol | Jodbenzylalkohol |
| Benzaldehyd (–CHO) | Fluorbenzaldehyd | Klorbenzaldehyd | Brombenzaldehyd | Jodbenzaldehyd |
| Bensoesyre (–COOH) | Fluorbenzoesyre | Klorbenzoesyre | Brombenzoesyre | Jodbenzoesyre |
Merknader og referanser
- Oppføring "Fluorbenzen" i den kjemiske databasen GESTIS fra IFA (tysk instans ansvarlig for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 29. juli 2019 (JavaScript kreves)
- Oppføring "Klorbenzen" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 29. juli 2019 (JavaScript kreves)
- Oppføring "Brombenzen" i den kjemiske databasen GESTIS fra IFA (tysk instans ansvarlig for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 29. juli 2019 (JavaScript kreves)
- Sigma-Aldrich- ark av forbindelsen Iodbenzene , konsultert 29. juli 2019.
- CRC Handbook of Bord for Organic Compound Identifikasjon , 3- e ed. , 1984 ( ISBN 0-8493-0303-6 ) .
- Gjennomsnitt av p K A av de forskjellige derivatene, gitt til sammenligning. De orto- forbindelser , hvor halogenet er nærmest den annen substituent, og derfor hvor -I effekt er sterkest, er den mest sure, effekten å være en tendens til å øke med atommasse.