Klortoluen
Den klortoluen eller metyl- er en aromatisk forbindelse med formelen C 7 H 7 Cl. Den består av en benzenring erstattet av en metylgruppe og et kloratom . Som alle disubstituerte benzener, eksisterer den i form av tre strukturelle isomerer , orto- , meta- og para- forbindelsene , avhengig av den relative posisjonen til de to substituentene på ringen.
Den benzylklorid , noen ganger referert til som α-klortoluen, er en isomer chlorotoluenes hvor klor er substituert på metylgruppen, men det anses ikke som sådan som et klortoluen.
Eiendommer
| Klortoluen | |||
| Etternavn | 2-klortoluen | 3-klortoluen | 4-klortoluen |
| Andre navn | 1-klor-2-metylbenzen o -chlorotoluene orto klortoluen |
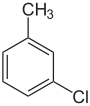
1-klor-3-metylbenzen m -chlorotoluene meta klortoluen |
1-klor-4-metylbenzen p -chlorotoluene para klortoluen |
| Representasjon |

|
|

|
| CAS-nummer | |||
| (blanding av isomerer) | |||
| ECHA | 100,002,205 | 100,003,255 | 100,003,089 |
| 100.042.438 ( 100.137.417 ) (blanding av isomerer) | |||
| PubChem | 6945 | 8489 | 7474 |
| Brute formel | C 7 H 7 Cl (C 6 H 4 ClCH 3 ) | ||
| Molarmasse | 126,586 g mol −1 | ||
| Stat ( CNTP ) | væske | ||
| Utseende | fargeløs flytende aromatisk lukt |
fargeløs flytende aromatisk lukt |
fargeløs væske |
| Fusjonspunkt | −35 ° C | −48 ° C | 7,5 ° C |
| Kokepunkt | 159 ° C | 162 ° C | 162 ° C |
| Tetthet ( 20 ° C ) | 1,08 g · cm -3 | 1,08 g · cm -3 | 1,07 g · cm -3 |
| Mettende damptrykk | 3,82 hPa ( 20 ° C ) | 3,8 hPa ( 20 ° C ) | 3,6 hPa ( 20 ° C ) |
|
Flammepunkt (lukket kopp) |
43 ° C | 48 ° C | 49 ° C |
| Selvantennelsespunkt | > 550 ° C | > 550 ° C | 570 ° C |
| Eksplosive grenser | 1,3 - 8,3 vol.% (68 - 435 g / m³) |
1,3 - 8,3 vol.% (68 - 435 g / m³) |
1,3 - 8,3 vol.% (68 - 435 g / m³) |
|
Løselighet (vann) |
0,05 g l −1 ( 20 ° C ) | 0,106 g l −1 ( 25 ° C ) | 0,11 g l −1 ( 25 ° C ) |
| Fordelingskoeffisient for oktanol / vann ( LogP ) |
3.42 | 3.28 | 3.33 |
|
SGH |
   
|
  
|
  
|
| H- og P-setninger |
H226, H332, H361d, H410,
H226 : Brannfarlig væske og damp H332 : Farlig ved innånding H361d : Mistenkes å skade det ufødte barnet . H410 : Meget giftig for vannlevende organismer, med langvarige virkninger |
H226, H332, H411,
H226 : Brannfarlig væske og damp H332 : Farlig ved innånding H411 : Giftig for vannlevende organismer, med langvarige virkninger |
H226, H317, H332, H411,
H226 : Brannfarlig væske og damp H317 : Kan forårsake en allergisk hudreaksjon H332 : Farlig ved innånding H411 : Giftig for vannlevende organismer, med langvarige effekter |
|
P210, P273, P280, P310, P304 + P340,
P210 : Holdes borte fra varme / gnister / åpen ild / varme overflater. - Røyking forbudt. P273 : Unngå utslipp til miljøet. P280 : Bruk vernehansker / verneklær / øyevern / ansiktsbeskyttelse. P310 : Kontakt et GIFTINFORMASJONSSENTER eller lege. P304 + P340 : Etter innånding: Flytt personen i frisk luft og hold den i ro i en stilling som er behagelig å puste |
P210, P273, P304 + P340 + P312,
P210 : Holdes borte fra varme / gnister / åpen ild / varme overflater. - Røyking forbudt. P273 : Unngå utslipp til miljøet. P304 + P340 + P312 : Ved innånding: flytt personen til frisk luft og hold den i en stilling som er behagelig å puste. Ring et GIFTINFORMASJONSSENTER / lege hvis du føler deg uvel. |
P273, P280,
P273 : Unngå utslipp til miljøet. P280 : Bruk vernehansker / verneklær / øyevern / ansiktsbeskyttelse. |
|
Klortoluener er i form av fargeløs væske, veldig lite løselig i vann, de kan imidlertid oppløses i andre organiske løsningsmidler som benzen , etanol , eter , etylacetat eller kloroform . Smeltepunktene til orto- og metaforbindelsene er relativt nærme, for para- forbindelsen , som har en mye større symmetri, er derimot mye høyere. På den annen side er fordampningspunktene til tre isomerer veldig nærme.
|
Parametere av Antoine ligningen log 10 (P) = A- (B / (T + C)) | ||||
| T (K) | PÅ | B | VS | |
| 2-klortoluen | 278.4–432.5 | 4.48741 | 1768.105 | −38.389 |
| 3-klortoluen | 277,9–435,5 | 4.48148 | 1807 576 | −32.105 |
| 4-klortoluen | 278,7 K - 435,5 | 4.47458 | 1795,293 | −34.380 |
Produksjon
Klortoluener kan fremstilles fra de tilsvarende toluidiner via Sandmeyer-reaksjonen . En blanding av 2- og 4-klortoluener oppnås ved å klore toluen med klor og jern, og danne jern (III) klorid som Lewis-syre .
Bruker
Chlorotoluenes brukes som løsemidler og som mellomprodukter i produksjonen av tinkturer, fytosanitære produkter og legemidler.
2- og 4-klortoluen er forløpere av benzylklorid (ClC 6 H 4- CH 2 Cl) med benzaldehyd (ClC 6 H 4 CHO) og benzoylklorid (ClC 6 H 4- C (O) Cl).
Merknader og referanser
- (de) Denne artikkelen er delvis eller helt hentet fra Wikipedia-artikkelen på tysk med tittelen " Chlortoluole " ( se forfatterliste ) .
- Entry "Chlorotoluene, blandede isomerer" i stoffkartoteket GESTIS av IFA (tysk organ med ansvar for sikkerhet og helse) ( tysk , engelsk ), tilgang til 06.09.2020 (Javascript kreves) .
- Oppføring "2-Chlorotoluene" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 6. september 2020 ( JavaScript kreves) .
- Oppføring "3-Chlorotoluene" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 6. september 2020 ( JavaScript kreves) .
- Oppføring "4-Chlorotoluene" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 6. september 2020 ( JavaScript kreves) .
- Stull, DR: Damptrykk av rene stoffer Organiske forbindelser , i: Ind. Eng. Chem. 39 (1947) 517–540, doi: 10.1021 / ie50448a022 .
- (fra) Organikum , Johann Ambrosius Barth,1993( ISBN 3-335-00343-8 ) , s. 566
- Ullmann's Encyclopedia of Industrial Chemistry , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.o06_o03 )
Se også
- Benzylklorid eller α-klortoluen
- Diklortoluen
- Triklortoluen
- Tetraklortoluen
- Pentaklortoluen
| - F | - Cl | - Br | - Jeg | |
|---|---|---|---|---|
| Benzen | Fluorbenzen | Klorbenzen | Brombenzen | Jodbenzen |
| Fenol (–OH) | Fluorfenol | Klorfenol | Bromfenol | Jodofenol |
| Aniline (–NH 2 ) | Fluoroanilin | Kloranilin | Bromoanilin | Jodoanilin |
| Anisole (–OCH 3 ) | Fluoranisole | Kloroanisol | Bromoanisole | Jodoanisole |
| Toluen (–CH 3 ) | Fluorotoluen | Klortoluen | Bromotoluen | Jodotoluen |
| Nitrobensen (–NO 2 ) | Fluoronitrobenzen | Kloritrobenzen | Bromonitrobenzen | Joditrobenzen |
| Benzylalkohol (-CH 2 OH) | Fluorbenzylalkohol | Klorbenzylalkohol | Brombenzylalkohol | Jodbenzylalkohol |
| Benzaldehyd (–CHO) | Fluorbenzaldehyd | Klorbenzaldehyd | Brombenzaldehyd | Jodbenzaldehyd |
| Bensoesyre (–COOH) | Fluorbenzoesyre | Klorbenzoesyre | Brombenzoesyre | Jodbenzoesyre |