Fenol (sammensatt)
| Fenol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur av fenol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-navn | fenol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
Karbolsyre |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,003,303 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 203-632-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03255 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 996 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 3223 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
c1 (ccccc1) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C6H6O / c7-6-4-2-1-3-5-6 / h1-5.7H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | fargeløs til gul eller lysrosa krystaller, med en karakteristisk lukt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C 6 H 6 O [Isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 94,1112 ± 0,0055 g / mol C 76,57%, H 6,43%, O 17%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | pKa (PhOH 2 + / PhOH) = -6,4 pKa (PhOH / PhO - ) = 9,95 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolar øyeblikk | 1,224 ± 0,008 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,557 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | 43 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | 182 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet | 76,04 g · l -1 vann | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighetsparameter δ |
25,1 J 1/2 · cm -3/2 ( 40 ° C ); 11,4 cal 1/2 · cm -3/2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumisk masse |
1,073 g · cm -3
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selvantennelsestemperatur | 715 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | 79 ° C (lukket kopp) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosjonsgrenser i luft | 1,36 - 10 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mettende damptrykk | ved 20 ° C : 47 Pa
ligning:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 61,3 bar , 694,2 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
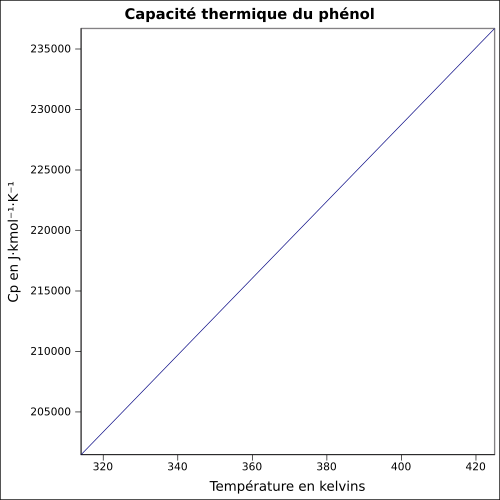
| C s |
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 3053,5 kJ · mol -1 ( 25 ° C , fast) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallografi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallklasse eller romgruppe | P 112 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh-parametere |
a = 6,050 Å b = 8,925 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volum | 788.01 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brytningsindeks | 1,5427 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Fare H301, H311, H314, H331, H341, H373, H301 : Giftig ved svelging H311 : Giftig ved hudkontakt H314 : Forårsaker alvorlige hudforbrenninger og øyeskader H331 : Giftig ved innånding H341 : Mistenkes for å kunne forårsake genetiske defekter (angi eksponerings hvis aktuelt) er det endelig bevist at ingen annen rute for eksponering fører til samme fare) H373 : Antatt risiko for alvorlig skade på organer (angi alle berørte organer, hvis kjent) etter gjentatt eksponering eller langvarig eksponering (angi eksponeringsveien hvis det er endelig bevist at ingen annen eksponeringsvei fører til samme fare) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  D1A, E, D1A : Meget giftig materiale med alvorlige øyeblikkelige effekter Transport av farlig gods: klasse 6.1 gruppe II E : Etsende materialnekrose i huden hos dyr Informasjon om 1,0 % i henhold til listen over ingredienser |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 4 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
60 : stoffer som er giftige eller som presenterer en mindre grad av toksisitet UN : 1671 : fenol-SOLID Klasse: 6,1 Label: 6,1 : Giftige stoffer Emballasje: Emballasje gruppe II : moderat farlige stoffer; 
60 : stoffer som er giftige eller som presenterer en mindre grad av toksisitet UN : 2312 : SMELTET FENOL Klasse: 6,1 Label: 6,1 : Giftige stoffer Emballasje: Emballasje gruppe II : moderat farlige stoffer; 
60 : stoffer som er giftige eller som presenterer en mindre grad av toksisitet UN : 2821 : fenoloppløsning Klasse: 6,1 Label: 6,1 : Giftige stoffer Emballasje: Emballasje gruppe II / III : moderat / svakt farlige stoffer.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- klassifisering | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe 3: Kan ikke klassifiseres som kreftfremkallende for mennesker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1.46 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Luktterskel | lav: 0,0045 ppm høy: 1 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den fenol , også kjent som hydroksybenzen , syre karbolsyre , eller karbolsyre , er sammensatt av en kjerne fenyl og en funksjon hydroksyl . Det er det enkleste molekylet i fenolfamilien .
Representasjoner
-
Kompakt modell
-
Kuler og pinner modell
Historie
Det ble oppdaget i en uren tilstand av Johann Rudolf Glauber i 1650 , fra destillasjon av tjære fra kull . Glauber beskriver det som " en knallrød blodolje som tørker opp og helbreder alle våte sår ."
I 1834 , Friedrich Ferdinand Runge lykkes i å isolere den og kalte det karbolsyre .
I 1836 oppfant Auguste Laurent begrepet "phene" for benzen; dette er roten til begrepene "fenol" og "fenyl".
I 1841 fikk den franske kjemikeren Auguste Laurent den i ren form.
Fra 1865 til 1880-tallet ble fenol brukt som et antiseptisk middel under ledelse av Joseph Lister , noe som reduserte dødeligheten under kirurgi fra 65% til 20%.
Fenol ble syntetisert og produsert i 1889 av selskapet BASF .
Enol
Fenol er også enol (alkoholholdig derivat med alkenfunksjon). Det er den tautomere formen av cykloheksa-2,4-dienon. Men i motsetning til de fleste enoler, er det den mest stabile formen sammenlignet med det tautomere ketonet , stabilitet hovedsakelig på grunn av tilstedeværelsen av en aromatisk ring som ikke er tilstede i den tilsvarende ketonen.

Fysiske egenskaper
Fenol har en kryoskopisk molalkonstant på 6,84 ° C ∙ kg / mol og en ebullioskopisk molalkonstant på 3,54 ° C ∙ kg / mol.
Ren hvit i fargen, den har en tendens til å oksidere litt ved kontakt med luft for å gi spor av kinoner som farger den rosa, deretter rød.
Produksjon
I 2005 ble det produsert 8,8 millioner tonn fenol over hele verden, hvorav rundt 26% i USA og 2% i Frankrike. Hovedprodusenten er Ineos Phenol (Storbritannia) med en produksjonskapasitet på 1,6 millioner tonn.
Mer enn 85% av fenol produseres i dag ved hjelp av kumene . Denne prosessen, utviklet i 1944 av Hock og Lang, har blitt brukt siden 1950-tallet. Fordelen ligger i enkelheten med implementeringen, det gode utbyttet (90%) og det faktum å få fenol og aceton fra kumen, tilgjengelig i store mengder av petrokjemikalier . Den består av en oksidasjon av kumen med luft som gir kumenhydroperoksyd som et mellomprodukt som i et surt vandig medium gir fenol og aceton.
bruk
- To tredjedeler av produksjonen av fenol brukes til å produsere plast ( polykarbonater , epoksyharpikser ).
- Viktig mellomprodukt for mange synteser av farmasøytiske produkter. Se fenol (gruppe) .
- I parfymeri : tymol , estragol , eugenol , vanillin , etc.
- I medisin brukes det hovedsakelig som et kraftig antiseptisk middel . Det brukes også i dermatologi ved behandling av inngrodde tånegler (fenolisering).
- I molekylærbiologi brukes fenol til å fjerne proteiner i nukleinsyreekstraksjonsprotokoller .
- Fremstilling av fenolftalein , en pH- metrisk indikator kjent for kjemikere.
- Ved innvirkning av klorgass på fenolen oppnås klorfenoler , slik som 2,4,6-triklorfenol .
- Brukes i entomologi for å bevare insektbed mot muggsopp.
- I mat , for konservering av kjøtt .
- Fenol brukes til produksjon av papir.
- I kombinasjon med konsentrert svovelsyre brukes den som en metode for farging av karbohydrater for deres bestemmelse ved spektrofotometri .
sikkerhet
Fenol er veldig etsende for levende organismer. En 1% vandig løsning er tilstrekkelig til å forårsake alvorlig irritasjon.
Fenolforbrenninger er veldig smertefulle og tar lang tid å gro. I tillegg kan de følges av alvorlige komplikasjoner som kan føre til døden på grunn av toksisiteten til denne forbindelsen og dens evne til å komme inn i kroppen gjennom huden.
Disse egenskapene gjør fenol til et middel for kjønnslemlestelse . Faktisk gikk D r Kellogg inn for å brenne klitorisfenol som et "middel" mot onani.
Under andre verdenskrig ble fanger i Auschwitz og andre leire henrettet med en punktering av fenol i hjertet. Maximilien Kolbe ble drept av en injeksjon av fenol i armen etter fjorten dagers forvaring uten mat. SS-lege Karl Babor som tjenestegjorde i Gross-Rosen-leiren var spesialist i attentat på fenolsprøyter.
Relaterte artikler
- Kresol , fenol substituert med en metylgruppe
-
Benzeniol , fenol substituert med en andre hydroksylgruppe
- Pyrocatechol (catechol), ortho- isomer
- Resorcinol (resorcinol), meta- isomer
- Hydrokinon , para isomer
- Benzenetriol
- Benzenetrol
- Benzenepentol
- Benzenheksol
Merknader og referanser
- FENOL , sikkerhetsark (er) til det internasjonale programmet for sikkerhet for kjemiske stoffer , konsultert 9. mai 2009
- (i) David R. Lide, håndbok for kjemi og fysikk , Boca Raton, CRC,16. juni 2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 og 1-4200-6679-X ) , s. 9-50
- (en) Yitzhak Marcus, The Properties of Solvents , vol. 4, Storbritannia, John Wiley & Sons Ltd,1999, 239 s. ( ISBN 0-471-98369-1 )
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- (en) Şerban Moldoveanu, Forberedelse av prøver i kromatografi , Elsevier ,2002, 930 s. ( ISBN 0-444-50394-3 ) , s. 258
- (in) JG Speight, Norbert Adolph Lange, Lange's Chembook , McGraw-Hill,2005, 16 th ed. , 1623 s. ( ISBN 0-07-143220-5 ) , s. 2.289
- (no) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- " Properties of Various Gases ", på flexwareinc.com (åpnet 12. april 2010 )
- (i) Carl L. yaws, Handbook of Thermodynamic diagrammer: Organic Compounds C8 til C28 , vol. 2, Huston, Texas, Gulf Pub. Co.,1996, 396 s. ( ISBN 0-88415-858-6 )
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online presentasjon ) , s. 5-89
- (no) “ Fenol ” , på www.reciprocalnet.org (åpnet 12. desember 2009 )
- IARC arbeidsgruppe for evaluering av kreftfremkallende risikoer for mennesker, “ Global Carcinogenicity Assessments for Humans, Group 3: Unclassifiable as to their carcinogenicity for Humans ” , på http://monographs.iarc.fr , IARC,16. januar 2009(åpnet 22. august 2009 )
- indeksnummer (en) i tabell 3.1 tillegg VI regulering EC n o 1272/2008 (16.12.2008)
- " Fenol " i databasen over kjemiske produkter Reptox fra CSST (Quebec-organisasjonen med ansvar for arbeidsmiljø og helse), åpnet 25. april 2009
- Oppføring "Fenol" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 25. august 2009 (JavaScript kreves)
- (in) " Phenol " på hazmap.nlm.nih.gov (åpnet 14. november 2009 )
- Auguste Laurent, om klorfenise og klorfenisiske og klorfenesiske syrer ,1836, Jeg gir navnet fen til den grunnleggende radikalen til de foregående syrene ( φαινω , jeg opplyser), siden bensin finnes i lysgassen .
- Annales de chimie et de physique , V. Masson (Paris), 1816-1913 ( les online )
- (in) Bedriftsnettsted
- Data om industriell produksjon av fenol , Chemical Society of France , 8 th ed. , 2009
- Heinrich Hock (1887-1971) er en tysk kjemiker, utdannet ved det tekniske universitetet i München av Karl Andreas Hofmann . Han underviste fra 1927 til 1958 ved Institut des Charbonnages i Mülheim, deretter eksplosiv kjemi ved École des Mines i Clausthal .
- Shon Lang var Heinrich Hocks kollega i Clausthal.
- " Inngrodd tåneglbehandling av Phenol inngrodd tånegl med e-sante.fr " på e-sante.fr (åpnet 6. mai 2016 ) .
- (i) Michel. DuBois , KA Gilles , JK Hamilton og PA Rebers , “ Kolorimetrisk metode for bestemmelse av sukker og relaterte stoffer ” , Analytical Chemistry , vol. 28 n o 3,Mars 1956, s. 350–356 ( ISSN 0003-2700 og 1520-6882 , DOI 10.1021 / ac60111a017 , leses online , åpnes 10. november 2019 )
- S. Suzanne Nielsen , “Phenol-Sulphuric Acid Method for Total Carbohydrates” , i Food Analysis Laboratory Manual , Springer US,2010( ISBN 9781441914620 , DOI 10.1007 / 978-1-4419-1463-7_6 , les online ) , s. 47–53
- (in) John Harvey Kellogg, Plain Facts for Old and Young ,1888, 644 s. ( ISBN 978-0-405-05808-0 )