Epiklorhydrin
| (±) -Epiklorhydrin | |||
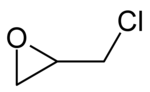
| |||
  R- enantiomer av epiklorhydrin (venstre) og S- epiklorhydrin (høyre) |
|||
| Identifikasjon | |||
|---|---|---|---|
| IUPAC-navn | 2- (klormetyl) oksiran | ||
| Synonymer |
1-klor-2,3-epoksypropan |
||
| N o CAS | (R,S) | ||
| N o ECHA | 100,003,128 | ||
| N o EC | 203-439-8 | ||
| PubChem | |||
| SMIL |
ClCC1CO1 , |
||
| InChI |
InChI: InChI = 1 / C3H5ClO / c4-1-3-2-5-3 / h3H, 1-2H2 |
||
| Utseende | fargeløs væske | ||
| Kjemiske egenskaper | |||
| Formel |
C 3 H 5 Cl O [isomerer] |
||
| Molarmasse | 92,524 ± 0,005 g / mol C 38,94%, H 5,45%, Cl 38,32%, O 17,29%, 92,52 g / mol |
||
| Fysiske egenskaper | |||
| T ° fusjon | −48 ° C | ||
| T ° kokende | 116,56 ° C | ||
| Løselighet | 6,59 g / 100 ml (vann, 25 ° C ); Blandbar med alkohol, eter, kloroform , trikloretylen , karbontetraklorid ; Blandbar med petroleum hydrokarboner |
||
| Løselighetsparameter δ | 22,5 MPa 1/2 ( 25 ° C ) | ||
| Volumisk masse | 1,18066 g · cm -3 til 20,0 ° C | ||
| Selvantennelsestemperatur | 415,6 ° C | ||
| Flammepunkt | 40,6 ° C | ||
| Mettende damptrykk | 1,333 kPa ved 16,6 ° C | ||
| Dynamisk viskositet | 1,03 MPa · s ved 25 ° C | ||
| Forholdsregler | |||
| SGH | |||
     H226, H301, H311, H314, H331, H350,
H226 : Brannfarlig væske og damp
H226, H301, H311, H314, H331, H350,
H226 : Brannfarlig væske og damp H301 : Giftig ved svelging H311 : Giftig ved hudkontakt H314 : Gir alvorlige etseskader på huden og øyeskader H331 : Giftig ved innånding H350 : Kan forårsake kreft (angi eksponeringsvei hvis det er beviselig at ingen annen eksponeringsvei fører til samme fare) |
|||
| WHMIS | |||
   B3, D1A, D2A, E, |
|||
| NFPA 704 | |||
| 3 3 2 | |||
| Transportere | |||
63 : giftige og brennbart materiale (flammepunkt 23 for å 60 ° C , inkludert grenseverdier) UN : 2023 : epiklorhydrin Klasse: 6.1 Etiketter: 6,1 : Giftige stoffer 3 : Brennbare væsker Pakking: Emballasje gruppe II : moderat skadelige stoffer ;   |
|||
| IARC- klassifisering | |||
| Gruppe 2A, kreftfremkallende | |||
| Innånding | TLV: 2 spm | ||
| Hud | 7,6 mg / m3 | ||
| Økotoksikologi | |||
| DL 50 |
90 mg · kg -1 (rotte, oral ) 154 mg · kg -1 (rotte, iv ) 150 mg · kg -1 (rotte, sc ) 113 mg · kg -1 (rotte, ip ) |
||
| LogP | 0,45 | ||
| Luktterskel | lav: 0,93 ppm | ||
| Enheter av SI og STP med mindre annet er oppgitt. | |||
Den epiklorhydrin eller epiklorhydrin og 1-klor-2,3-epoksypropan , er en klorert organisk forbindelse med strukturformel CH 2 CHOCH 2 Cl, flytende, flyktig toksisk, fargeløs til sterk hvitløk lukt. Et karbonatom av epiklorhydrin er kiralt , så er det to enantiomere former av denne forbindelse.
Til tross for navnet tilhører ikke epiklorhydrin klorhydrinfamilien , siden det ikke er en halogenert alkohol, men et epoksid . På den annen side er visse direkte mellomprodukter i sin syntese, slik som 2,3-diklor-1-propnol og 1,3-diklor-2-propnol, klorhydriner.
Produksjon
Epiklorhydrin er laget av allylklorid i to trinn, først hydroklorering ved bruk av hypoklorsyre , noe som resulterer i en blanding av klorhydriner :
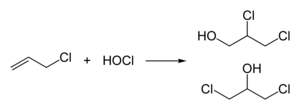
Den andre fasen resulterer i dannelsen av epoxy ved behandling med en base :

På denne ruten produseres det over 800.000 tonn (1997) epiklorhydrin årlig.
Glyserolvei
Epiklorhydrin ble først beskrevet i 1848 av Marcellin Berthelot . Forbindelsen ble isolert under studier av reaksjonene mellom glyserol og hydrogenkloridgass .
Minner om opplevelsen av Berthelot, har glyserol-epiklorhydrin (GTE, for glyserol-til-epiklorhydrin ) fabrikker blitt markedsført. Denne teknologien utnytter tilgjengeligheten av rimelige glyseroler fra prosessering av biodrivstoff . I prosessen utviklet av Dow Chemical gjennomgår glyserol to substitusjonsreaksjoner når de behandles med hydrogenklorid i nærvær av en karboksylsyre som brukes som katalysator . Reaksjonen danner et av de samme to mellomproduktene som i allylklorid / hypoklorsyre-prosessen, 1,3-diklor-2-propnol, og den behandles også med en base for å danne epiklorhydrin.

Andre ruter
Andre ruter som involverer færre klorerte mellomprodukter, blir fortsatt utforsket. Det kan for eksempel nevnes epoksydering av allylklorid .
bruk
Syntese av glyserol og epoksyharpikser
Epiklorhydrin omdannes primært til bisfenol-A-diglycidylether (en) , en grunnleggende byggestein i fremstillingen av epoksyharpikser . Det er også en monomerforløper for andre harpikser og polymerer, inkludert ionebytterharpikser , polyeterpolyoler for flammehemmende polyuretanskum , alkylglyseryletersulfonater for vaskemidler, elastomerer ( polymerkoder CO, ECO) og spesielle harpikser for papirbehandling.
En annen bruk er omdannelsen til syntetisk glyserol . Imidlertid har den raske økningen i produksjonen av biodiesel , hvor glyserol er avfall, resultert i en overflod av glyserol på markedet, noe som gjør denne prosessen ulønnsom. Syntetisk glyserol brukes nå bare i sensitive farmasøytiske og bioteknologiske applikasjoner der kvalitetsstandardene er veldig høye.
Mindre og nisjeapplikasjoner
Epiklorhydrin er en allsidig forløper i syntesen av mange organiske forbindelser. For eksempel kan det omdannes til glycidylnitrat , et energisk bindemiddel som brukes i eksplosive og drivstoffblandinger. Epiklorhydrin reageres med et alkalinitrat, slik som natriumnitrat , og produserer glycidylnitrat og et alkaliklorid. Det brukes som et løsningsmiddel for cellulose , harpiks og maling, og det har funnet bruk som et fumigant mot insekter.
Polymerer laget av epiklorhydrin, for eksempel polyamid-epiklorhydrinharpikser, brukes i papirforsterkning og i næringsmiddelindustrien til å lage teposer , kaffefiltre og syntetiske pølse / pølsehylser , samt til vannrensing .
Et viktig biokjemisk anvendelse av epiklorhydrin er dets anvendelse som et tverrbindingsmiddel for fremstilling av størrelse -eksklusjonskromatografi harpikser på Sephadex (en) fra dekstran .
sikkerhet
Epiklorhydrin er klassifisert av flere etater og internasjonale helseforskningsgrupper som sannsynlig eller sannsynlig kreftfremkallende hos mennesker. Langvarig (oral) inntak av høye nivåer av epiklorhydrin kan føre til mageproblemer og økt risiko for kreft. Yrkesmessig eksponering for epiklorhydrin ved innånding kan forårsake irritasjon i lungene og økt risiko for lungekreft.
Epiklorhydrin er brannfarlig og danner farlige nedbrytningsprodukter under brannforhold. Det er giftig ved innånding, hudkontakt og svelging, og kan forårsake forbrenning. Det kan forårsake sensibilisering ved hudkontakt.
Merknader og referanser
- ( fr ) Denne artikkelen er helt eller delvis hentet fra Wikipedia-artikkelen på engelsk med tittelen " Epichlorohydrin " ( se listen over forfattere ) .
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- (en) Guenter Sienel, Robert Rieth, Kenneth T. Rowbottom, Epoxides , Wiley-VCH Verlag GmbH & Co, koll. "Ullmann's Encyclopedia of Industrial Chemistry",15. juni 2000( DOI 10.1002 / 14356007.a09_531 , online presentasjon )
- "EPICHLOROHYDRIN" i databanken for farlige stoffer , åpnet 16. juli 2012
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , leses online ) , s. 294
- Oppføring "Epiklorhydrin" i den kjemiske databasen GESTIS fra IFA (tysk instans ansvarlig for arbeidsmiljø og helse) ( tysk , engelsk ), åpnet 3. desember 2010 (JavaScript kreves)
- "Epichlorohydrin" i databasen over kjemikalier Reptox fra CSST (Quebec-organisasjonen med ansvar for arbeidsmiljø og helse), åpnet 3. desember 2010
- UCB University of Colorado
- (in) " Epichlorohydrin " på ChemIDplus , åpnet 3. desember 2010
- "1-klor-2,3-epoxypropane" , på ESIS , åpnet 3. desember 2010
- Ullmann's Encyclopedia of Industrial Chemistry , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a01_425 )
- Marcellin Berthelot , “ Om kombinasjonene av glyserin med syrer og om syntesen av de umiddelbare prinsippene for animalsk fett ”, Ann. Chim. Phys. , vol. 41,1854, s. 216–319 ( les online [ arkiv av2. april 2015] , åpnet 2. mars 2015 )
- Doris de Guzman, “ Voksende planter av glyserin til ECH ” , ICIS Green Chemicals,20. januar 2011
- Bruce M. Bell , John R. Briggs , Robert M. Campbell , Susanne M. Chambers , Phil D. Gaarenstroom , Jeffrey G. Hippler , Bruce D. Hook , Kenneth Kearns , John M. Kenney , William J. Kruper , D James Schreck , Curt N. Theriault og Charles P. Wolfe , “ Glyserin som et fornybart råstoff for epiklorhydrinproduksjon. GTE-prosessen ”, CLEAN - Soil, Air, Water , vol. 36, n o 8,2008, s. 657 ( DOI 10.1002 / clen.200800067 , les online [ arkiv av18. juli 2012] [fulltekstopptrykk], åpnet 5. mars 2012 )
- Jun Li, Gongda Zhao, Shuang Gao, Ying Lv, Jian Li og Zuwei Xi, “ Epoxidation of Allyl Chloride to Epichlorohydrin by a Reversible Supported Catalyst with H2O2 under Solvent-Free Conditions ”, Org. Prosess Res. Dev. , vol. 10, n o 5,2006, s. 876–880 ( DOI 10.1021 / op060108k )
- Ha Q. Pham og Maurice J. Marks , " Epoxy Harpiks ", Wiley-VCH , Weinheim,2012( ISBN 978-3527306732 , DOI 10.1002 / 14356007.a09_547.pub2 )
- " Terskler for akutt toksisitet - epiklorhydrin " , INERIS
- Phil Taylor , “ Syntetisk glyserin er tilbake (men gikk aldri helt bort)! » , In-Pharma Technologist ,16. oktober 2008(åpnet 29. november 2018 )
- Gould, RF Advanced Drivell Chemistry , ACS Chemistry Series 54, 1966
- " Suburban Water Testing Labs: Epichlorohydrin Fact Sheet " [ arkiv av5. april 2012] , H2otest.com (åpnet 2. desember 2011 )
- " Government of Canada Chemical Substances: Oxirane, (chloromethyl) - (Epichlorohydrin) CAS registreringsnummer 106-89-8 " (åpnet 7. mai 2013 )
- " GE Healthcare Life Sciences - Instruksjoner for Sephadex Media " [ arkiv av18. februar 2012] , .gelifesciences.com (åpnet 2. desember 2011 )
- " EPA Integrated Risk Information System: Epichlorohydrin (CASRN 106-89-8) " (åpnet 7. mai 2013 )
- " Regjeringen i Canada: Screening Assessment for Epichlorohydrin " (åpnet 7. mai 2013 )
- " NIOSH Pocket Guide to Chemical Hazards - Epichlorohydrin " (åpnet 20. september 2013 )
- " Grunnleggende informasjon om epiklorhydrin i drikkevann " (åpnet 7. mai 2013 )
- " Regjeringen i Canada: Screening Assessment for Epichlorohydrin " (åpnet 7. mai 2013 )
