Brommetan
| Brommetan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Synonymer |
Metylbromid |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.740 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-813-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6323 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 39275 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
CBr , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3Br / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | Fargeløs, luktfri, flytende komprimert gass. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C H 3 Br [Isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 94,939 ± 0,002 g / mol C 12,65%, H 3,19%, Br 84,16%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolar øyeblikk | 1,8203 ± 0,0004 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −93,66 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | 3,56 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet | i vann ved 20 ° C : 1,5 ml / 100 ml | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighetsparameter δ | 19,6 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
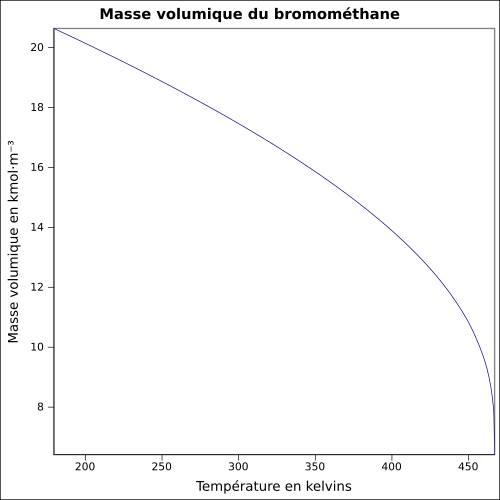
| Volumisk masse |
3,9739 g · cm -3 ( 0 ° C , 1013 mbar )
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selvantennelsestemperatur | 537 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | < 194 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosjonsgrenser i luft | 8,6 - 20 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
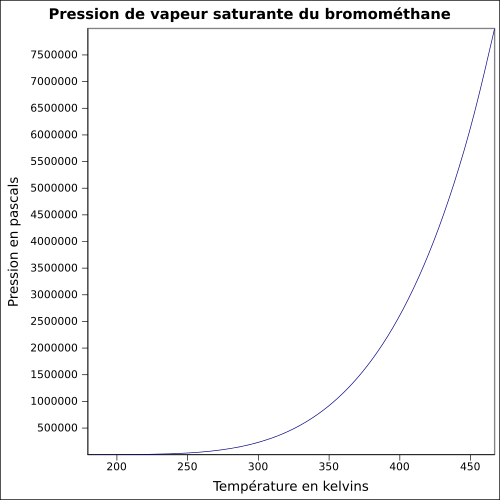
| Mettende damptrykk |
1,89 bar ved 20 ° C 2,6 bar ved 30 ° C 4,9 bar ved 50 ° C ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | ( 194 ° C ), 52,3 bar , 0,577 kg · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trippel punkt | ( −93,7 ° C ), 0,002 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 væske, 1 bar | 155,14 J · K- 1 - mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gass | -34,3 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 væske | -60,6 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 6,0 kJ · mol -1 til -93,65 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 23,24 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
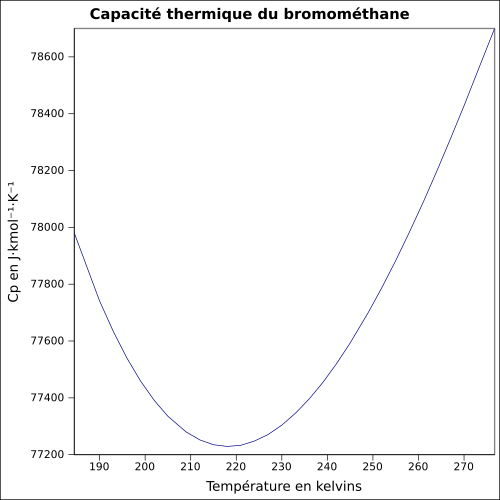
| C s |
114,6 J · K -1 · mol -1 (væske, 9,85 ° C )
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 10,541 ± 0,003 eV (gass) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    Fare H301, H315, H319, H331, H335, H341, H373, H400, EUH059, H301 : Giftig ved svelging H315 : Forårsaker hudirritasjon H319 : Forårsaker alvorlig øyeirritasjon H331 : Giftig ved innånding H335 : Kan irritere luftveiene H341 : Mistenkes for å kunne forårsake genetiske defekter (angi svei dersom det er bevist at ingen andre eksponerings forårsaker samme fare) H373 : Mistenkt risiko for alvorlig organskade (liste opp alle berørte organer, hvis kjent) som følge av eksponering gjentatt eller langvarig eksponering (angi eksponeringsvei hvis det er endelig bevist at ingen annen eksponeringsvei forårsaker samme fare) H400 : Meget giftig for vannlevende organismer EUH059 : Farlig for ozonlaget |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, D1A, D2B, E, A : Komprimert gass absolutt damptrykk ved 50 ° C = 480 kPa D1A : Meget giftig materiale med alvorlige øyeblikkelige effekter Transport av farlig gods: klasse 2.3 D2B : Giftig materiale med andre toksiske effekter Kronisk toksisitet E : Etsende materialnekrose av menneskelig hud Avdekking ved 1,0% i henhold til klassifiseringskriterier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
26 : giftig gass UN-nummer : 1062 : METYLBROMID Klasse: 2.3 Merking: 2.3 : Giftige gasser (tilsvarer gruppene betegnet med store bokstaver T, dvs. T, TF, TC, TO, TFC og Bam). Emballasje: -  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- klassifisering | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe 3: Kan ikke klassifiseres som kreftfremkallende for mennesker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Svelging | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Annen | depresjon i sentralnervesystemet . Leverskader og nyrer . Åndedrettsstans. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1.19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Luktterskel | lav: 20 spm høy: 1000 spm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den metylbromid eller metylbromid er en organisk kjemisk forbindelse halogeneres hvis kjemiske formel er: C H 3- Br . Det er en del av metylhalogenidene ( halokarboner ):
Det er en giftig og sterkt økotoksisk gass , fargeløs og ikke-brennbar uten særegen lukt. Dens kjemiske egenskaper er ganske like klormetan .
Det er et plantevernmiddel ( insektmiddel ), av biocider- familien . Det er en del av kjølemediumgassene. Metanbromid markedsføres under forskjellige navn, hvorav den mest kjente er Embafume og Terabol . Det er også kjent under navnet R40B1 .
Siden det både er en klimagass (kraftig) og en av gassene som ødelegger ozonlaget som beskytter jorden mot overdreven ultrafiolett stråling , er det planlagt å forby lenge, men bare visse land har brukt dette forbudet, Frankrike siden 2005 (med unntak for visse bruksområder) og EU siden 2011.
På det trettiende møte for partene til Montreal-protokollen om stoffer som tømmer ozonlaget, som finner sted i Quito , hovedstaden i Ecuador, Canada , Australia , Argentina og Sør-Afrika , fikk også unntak for bruk av metylbromid for 2019 og 2020
Opprinnelse
Metanbromid eksisterer i små mengder i naturen der det dannes naturlig i havet , syntetisert av fytoplankton (og tang ?).
Når den er biogen (av naturlig opprinnelse, produsert av levende organismer), spiller den en rolle i naturen som fremdeles ikke er forstått. Det kan muligens være involvert i tilbakemeldinger fra klimaet (fordi hvis oppholdstiden i atmosfæren er kort (ca. 1 år), er den en kraftig klimagass og den hemmer produksjonen av stratosfærisk ozon .
Under et nylig geoingeniøreksperiment som tar sikte på å øke kapasiteten til marine karbonvask ved å gjødsle havet med jern i middels skala (overflateareal mindre enn 1000 km 2 ), ble en negativ effekt observert: økt produksjon av oceanisk brommetan.
Den kommer også fra visse jordbaserte planter, spesielt de fra brassica- familien .
Industrielt, som et biocid, er det laget ved å reagere metanol med hydrobromsyre .
Bruker
Inntil produksjonen og bruken ble redusert eller forbudt av Montreal-protokollen (signert 1987, men fremdeles ufullstendig respektert), ble den mye og mye brukt som jordsterilisasjonsmiddel , hovedsakelig for produksjon av frø, men også for visse grønnsaksavlinger som jordbær .
Metanbromid har også blitt brukt som et generelt formål for å bekjempe et bredt utvalg av skadedyr, fra rotter og insekter til mikroskopiske sopp. Det brukes fortsatt til visse bruksområder (desinfisering av importert tre). Den fungerer også som en forløper for fremstilling av andre kjemikalier, og den ble brukt som løsningsmiddel for utvinning av oljer fra frøene og som avfettingsmiddel av ull .
Da Montreal-protokollen sterkt begrenset bruken av metylbromid på internasjonalt nivå, oppfordret noen land, inkludert USA, unntak for bruk av produktet i kontrollert bruk. I 2004, det siste året det foreligger data, ble mer enn 3000 tonn metanbromid sprayet i kaliforniske felt.
I 2017 hadde nesten 10 000 tonn metylbromid blitt brukt til karantene og behandlinger før forsendelse, og tallet økte. I løpet av det siste tiåret hadde mengden metylbromid som ble brukt til karantene og behandlinger før forsendelse, mer enn doblet seg i noen land, muligens på grunn av økt handel, farer ved karantene skadedyr og / eller feilklassifisering av visse bruksområder som karantene og pre- forsendelse bruker. Dette var hovedkomponenten i de globale utslippene, og utgjorde omtrent 7500 tonn per år. Metylbromidet som ble brukt til karantene og behandlinger før forsendelse var meget flyktig (opptil 95% av metylbromidet som ble brukt, kunne frigjøres direkte til atmosfæren etter gassbehandling). Fremskritt innen teknikker for utvinning og destruksjon kan imidlertid redusere utslippene betydelig.
Metan bromid ble brukt i spesialitet brannslukningsapparater , før ankomsten av mindre toksiske halon , fordi det er elektrisk ikke-ledende og etterlater ingen rester. Den ble hovedsakelig brukt til elektriske transformatorstasjoner, militære fly og mot visse industrielle farer. Det har aldri vært så populært som andre midler på grunn av høye kostnader og toksisitet. Metanbromid ble brukt fra 1920 til 1960. I Frankrike ble dekret nr. 59-449 av21. mars 1959forbudt fra 1 st januar 1961, produksjon, besittelse, fylling, overføring mot betaling eller gratis av brannslukningsapparater lastet med metylbromid eller karbontetraklorid .
Ozonlagsdestruksjon
Metanbromid er på listen over stoffer som er forbudt i Montreal-protokollen på grunn av risikoen for å ødelegge ozonlaget . Siden brom er 60 ganger mer skadelig enn klor , er til og med en liten mengde metylbromid nok til å forårsake betydelig skade på ozonlaget . I 2005 og 2006 ble det imidlertid gitt fritak for kontrollert bruk under Montreal-protokollen.
Kontroverser
Den Montreal-protokollen fastslår at anvendelse av brommetan må forbys, men dette produktet ga mange fordeler, spesielt for behandling av trevirke, jord, korn og frø, og for visse anvendelser, er det ingen erstatningsprodukter. Tilgjengelig på samme kostnad eller så praktisk. Metan bromide brukes i USA for å forberede golfbaner og torv overflater brukes til ulike idrettskonkurranser, spesielt for vedlikehold av Cynodon dactylon torv . Den administrasjonen til George W. Bush har vedtatt fritak for å hindre markedet avbrudd.
En risikovurdering ble oppdatert i 2010 av EFSA
Helseeffekter
Hvis det inhaleres i høy konsentrasjon i kort tid, forårsaker det hodepine, svimmelhet, kvalme, oppkast, utilpashed. Disse symptomene kan følges av tegn på nervøs spenning, kramper og til og med akutte psykiske forstyrrelser som manisk uro . Langvarig innånding ved lavere konsentrasjoner kan forårsake bronkial irritasjon og lungeskader.
Væsken brenner huden, forårsaker kløe og erytem, og blærer deretter flere timer etter kontakt. Væske og gass forårsaker alvorlige etseskader på øynene.
Eksponeringsnivåer som kan forårsake død varierer fra 1600 til 60 000 ppm , avhengig av eksponeringens lengde.
Åndedretts-, nyre- og nevrologisk skade påvirker flere mennesker. Ingen tilfeller av alvorlige langtidsvirkninger på nervesystemet har blitt notert hos mennesker etter eksponering for lave nivåer, men studier på kaniner og aper har vist lesjoner klassifisert som moderat til alvorlig.
Produksjon og nedbrytning
Kilder til produksjon av CH 3 Br inkluderer havproduksjon, utslipp fra planter og myrer , forbrenning av biomasse , røyking av jord og eksos fra blyholdig drivstoff , samt industri., Produksjon av holdbare forbruksvarer og lett bedervelige varer. Dens industrielle produksjon går ned, men har ikke blitt stoppet, inkludert i Frankrike
Nedbrytningen av den forurensende skjer ved fotokjemisk nedbrytning i atmosfæren (reaksjon med den kjemiske radikal hydroksyl (OH)) og ved oksydasjon (som gir som sekundære produkter BRC (O) CH 3 og BRC (O) H), eller ved fotodekomponeringsprodukter ved høyere høyder.
Til disse eliminasjonsmåtene må det legges til tap (adsorpsjon, nedbrytning) i jord, kjemisk og biologisk nedbrytning i havet, og noe resirkulering av grønne planter.
Alternativer
For mange bruksområder (f.eks. Vedbehandling av tre, røyking av jorda før planting) er det ikke noe alternativ som er så enkelt å implementere (ellers med større toksisk risiko, hvis man for eksempel bruker kloropikrinet som ble brukt under andre verdenskrig jeg som en krigsgass og som gass for å drepe dyrene i hulene sine, eller dazomet ...)
- Varmebehandlinger kan brukes til å desinfisere drivhusgulv (unntatt mot vinduene) eller hønehus (med samme utstyr som for termisk lukking om nødvendig)
- Integrert skadedyrsbekjempelse; for eksempel ifølge ANSES, for jordbruk, kan bonden assosiere
- nøye undersøkelse av multiplikasjonsplottene,
- dyrking av varianter med høyt motstandsnivå,
- produksjon av frø på uskadede tomter,
- prøvetaking og analyse av frøpartier,
- eliminering av planteavfall assosiert med frøene,
- kulturelle praksis som begrenser risikoen for et patogenutbrudd (rotasjoner, etc.).
Merknader og referanser
- METYLBROMID , sikkerhetsark (er) til det internasjonale programmet for kjemisk sikkerhet , konsultert 9. mai 2009
- (i) David R. Lide, håndbok for kjemi og fysikk , Boca Raton, CRC,16. juni 2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 og 1-4200-6679-X ) , s. 9-50
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Oppføring "Bromomethane" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for arbeidsmiljø og sikkerhet) ( tysk , engelsk ), åpnet 19. februar 2009 (JavaScript kreves)
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , online presentasjon ) , s. 294
- (no) Robert H. Perry og Donald W. Green , Perrys Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- (en) "Methyl bromide" , på NIST / WebBook , tilgjengelig
- (i) Carl L. yaws, Handbook of Thermodynamic diagrammer , vol. 1, 2 og 3, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 , 0-88415-858-6 og 0-88415-859-4 )
- (i) David R. Lide, håndbok for kjemi og fysikk , Boca Raton, CRC,2008, 89 th ed. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- IARC arbeidsgruppe for evaluering av kreftfremkallende risikoer for mennesker, “ Global Evaluations of Carcinogenicity for Humans, Group 3: Unclassifiable as to their Carcinogenicity for Humans ” , på http://monographs.iarc.fr , IARC,16. januar 2009(åpnet 22. august 2009 )
- Indeksnummer i tabell 3.1 i vedlegg VI til EF-forskrift nr. 1272/2008 (16. desember 2008)
- " Bromometan " i databasen over kjemiske produkter Reptox fra CSST (Quebec-organisasjonen med ansvar for arbeidsmiljø og helse), åpnet 25. april 2009
- " Metylbromid " på hazmap.nlm.nih.gov (åpnet 14. november 2009 )
- "brommetane" , på ESIS , åpnet 4. februar 2010
- FNs miljøprogram, rapport fra det trettiende møtet mellom partene i Montreal-protokollen om stoffer som tømmer ozonlaget, beslutning XXX / 9: Unntak for kritisk bruk for metylbromid for 2019 og 2020.
- Havgjødsling: redusering av miljøpåvirkningen av vitenskapelig forskning ; Canadian Science Advisory Secretariat Science Advisory Report 2010/012 (versjon publisert i april 2010 og oppdatert: juni 2010, konsultert 2013-09-17); se side 9/15 i PDF-filen
- Rapport fra det trettiende møtet mellom partene i Montreal-protokollen om stoffer som tømmer ozonlaget, UNEP / Ozl.Pro.30 / 11, vedlegg VI, punkt 74.
- " forbud mot brannslukningsapparater lastet med metylbromid " , på aroma (åpnet 23. januar 2021 )
- EFSA 12/01/11 < Peer Review av risikoen for plantevernmidler av det aktive stoffet metylbromid
- | http://www.ifen.fr/uploads/media/couche_ozone_01.pdf Nåværende og potensielle produksjonsdata for Frankrike]
- Atmosfærisk oksidasjonsmekanisme av brometan
- Duniway, JM (2002). Status for kjemiske alternativer til metylbromid for røyking av jord før planten . Fytopatologi, 92 (12), 1337-1343.
- ANSES (2013) Skadedyrsanalyse Ditylenchus dipsaci på lucerne ANSES-mening Samleekspertutredningsrapport , april 2013, PDF, 146 sider
Eksterne linker
- (no) Sikkerhetsdatablad for INRS (2007-utgivelsen)
- (no) Kanadisk faktaark om bærekraftig og integrert fjerning av skadedyrsbekjempelse av metylbromid (PDF, 41p)
- MSDS : Farlig kjemisk database
- ChemSub Online (brommetan) .