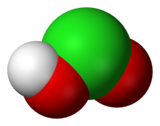
Klorsyre
| Klorsyre | ||

| ||
 | ||
| Identifikasjon | ||
|---|---|---|
| IUPAC-navn |
klorsyre
hydrogenkloritt |
|
| Synonymer |
saltsyre |
|
| N o CAS | ||
| PubChem | 24453 | |
| ChEBI | 29219 | |
| SMIL |
OCl = O , |
|
| InChI |
InChI: InChI = 1S / ClHO2 / c2-1-3 / h (H, 2,3) InChIKey: QBWCMBCROVPCKQ-UHFFFAOYSA-N |
|
| Kjemiske egenskaper | ||
| Brute formel |
H Cl O 2 [isomerer] |
|
| Molarmasse | 68,46 ± 0,003 g / mol H 1,47%, Cl 51,79%, O 46,74%, |
|
| pKa | 1,93-1,97 | |
| Enheter av SI og STP med mindre annet er oppgitt. | ||
Den klorsyrling er en uorganisk forbindelse med den empiriske formel H Cl O 2 . Det er en svak syre . Den kloratom er der på oksydasjonsgraden + III. Denne forbindelsen er ustabil i ren form.
Fysisk-kjemiske egenskaper
Denne forbindelse er ustabil i ren form, det disproportionates til underklorsyrling HClO, som klor oksidasjonstilstand er 1, og inn i klorsyre , HClO 3 (klor oksydasjonstilstand +5):
2 HClO 2 → HClO + HClO 3I kald og fortynnet vandig løsning er klorsyre i likevekt med klordioksid og saltsyre , og klorsyreformen er i mindretall:
5 HClO 2 4 ClO 2 + HCl + 2 H 2 OPå den annen side, kloritt anioner , den korresponderende base av denne syre, danner salter , som for eksempel natriumkloritt , som er stabile selv i ren tilstand.
Produksjon og syntese
En klorsyreoppløsning kan fremstilles ved å reagere bariumkloritt med fortynnet svovelsyre :
Ba (ClO 2 ) 2 + H 2 SO 4 → BaSO 4 + 2HClO 2Den bariumsulfat bunnfall , og således etterlater en klorsyrling løsning.
Stabilitet
Klor er det eneste halogenet som en oksosyre med formel HXO 2 kan isoleres for. Den fluor har ikke en høyere oksydasjonstilstand, og ett eller bromous syre eller den iodeux syre ble isolert. På den annen side, hvis noen sjeldne salter av bromsyre , bromittene , er kjent, er ingen joditt det.
Merknader og referanser
- (en) / (de) Denne artikkelen er helt eller delvis hentet fra artiklene rett i engelsk " klorsyrling " ( se listen over forfattere ) og i tysk " Chlorige Säure " ( se listen over forfattere ) .
- [PDF] pKa av forskjellige syrebasepar på iutmp.u-3mrs.fr
- Tabell over syrer og baser på kst-chemie.ch
- Arnold F. Holleman, Nils Wiberg, Lehrbuch der Anorganischen Chemie , 2007, 102 Ed., Berlin. ( ISBN 978-3-11-017770-1 ) .
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Egon Wiberg, Arnold Frederick Holleman, Inorganic Chemistry , 2001, Elsevier. ( ISBN 0-12-352651-5 ) .
Se også
- hypoklorsyre , HClO
- klorsyre , HClO 3
- perklorsyre , HClO 4
