Etanol
| Etanol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Etanolmolekyl |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikasjon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-navn | Etanol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymer |
etylalkohol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 000 526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-578-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kode | D08 , V03 , V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB00898 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 702 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16236 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E1510 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2419 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMIL |
CCO , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H6O / c1-2-3 / h3H, 2H2,1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Utseende | fargeløs væske med en karakteristisk lukt. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kjemiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formel |
C 2 H 6 O [Isomerer] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarmasse | 46,0684 ± 0,0023 g / mol C 52,14%, H 13,13%, O 34,73%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolar øyeblikk | 1,66 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekylær diameter | 0,469 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusjon | −114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kokende | 79 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighet | i vann: blandbar, Komplett i polare og ikke-polære løsemidler ( aceton , dietyleter ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Løselighetsparameter δ |
26,0 MPa 1/2 ( 25 ° C ); 11,2 cal 1/2 · cm -3/2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumisk masse |
0,789
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selvantennelsestemperatur |
423 til 425 ° C ; 363 ° C (avhengig av kilder) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Flammepunkt | lukket kopp: 13 ° C ren 17 ° C 95 % vol . 21 ° C 70 % vol . 49 ° C 10 % vol . 62 ° C 5 % vol . |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eksplosjonsgrenser i luft | Nedre: 3,3 % vol Øvre: 19 % vol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mettende damptrykk | ved 20 ° C : 5,8 kPa
ligning:
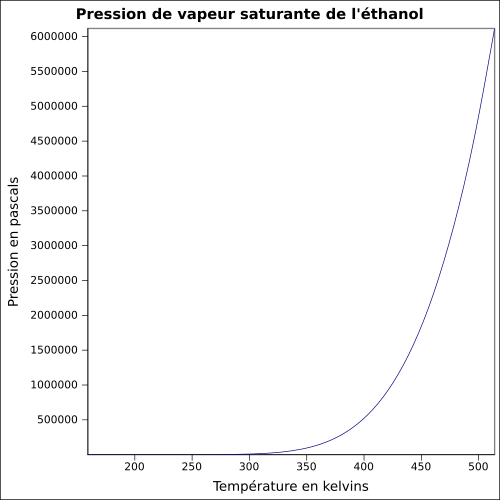
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamisk viskositet | 1,20 × 10 −3 Pa s ved 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritisk punkt | 240,85 ° C , 6,14 MPa , 0,168 l mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lydens hastighet | 1162 m s −1 ved 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokjemi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 væske, 1 bar | 159,86 J · mol -1 · K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gass | −235,3 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 væske | −277,0 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
111 J · K- 1 · mol -1
ligning:
ligning:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1 366,8 kJ · mol -1 (flytende) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ioniseringsenergi | 10,43 ± 0,05 eV (gass) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallografi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystallklasse eller romgruppe | Pc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh-parametere |
a = 5,377 Å b = 6,882 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volum | 298,57 Å 3 tetthet = 0,7893 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiske egenskaper | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brytningsindeks | 1.3594. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forholdsregler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Fare H225, P210, P305 + P351 + P338, P370 + P378, P403 + P235, H225 : Meget brannfarlig væske og damp P210 : Holdes borte fra varme / gnister / åpen ild / varme overflater. - Røyking forbudt. P305 + P351 + P338 : Ved øyne: Skyll forsiktig med vann i flere minutter. Fjern kontaktlinser hvis offeret bruker dem og de lett kan fjernes. Fortsett å skylle. P370 + P378 : I tilfelle brann: Bruk ... til utryddelse. P403 + P235 : Oppbevares på et godt ventilert sted. Hold deg kult. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transportere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : svært brannfarlig væske (flammepunkt under 21 ° C ) UN-nummer : 1170 : ETHYLALKOHOL som inneholder mer enn 24 prosent etanol, volumprosent; ETYLALKOHOLLØSNING inneholdende mer enn 24 volumprosent etanol, ETHANOL som inneholder mer enn 24 volumprosent etanol, eller etanolløsning innehold mer enn 24 prosent etanol, vol Klasse: 3 Etikett: 3 : Brennbare væsker Emballasje: Emballasje gruppe II : mellom farlige materialer;  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- klassifisering | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe 1: Kreftframkallende for mennesker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Innånding | rus, kvalme, oppkast | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hud | ingen effekt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Øyne | farlig | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Svelging | rus, kvalme, oppkast, etylkoma (som kan føre til døden) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Økotoksikologi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 5 til 20 g kg −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CL 50 | 20 000 til 30 000 ppm i 4 til 6 timer | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,32 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Luktterskel | lav: 49 spm høy: 716 spm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Farmakokinetiske data | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metabolisme | i leveren i etanol og deretter eddiksyre , ved ~ 100 mg kg −1 per time | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Psykotropisk karakter | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori | Depressant | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Måte å konsumere |
Svelging |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Andre navn |
Alkohol (se Alkoholholdige drikker ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fare for avhengighet | Student | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enheter av SI og STP med mindre annet er oppgitt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Den etanol, eller etylalkohol (eller enklere alkohol ) er en alkohol med strukturformelen CH, 3 -CH 2 -OH. Det er en fargeløs væske, flyktig , brannfarlig og blandbar med vann i alle proporsjoner. Det er et psykotropisk medikament , og et av de eldste rekreasjonsmedisinene , i form av en alkoholholdig drikke . Etanol brukes av næringsmiddelindustrien (spesielt for produksjon av brennevin ), parfymeri og farmasøytiske farmasøytiske produkter (som løsningsmiddel ) så vel som i biodrivstoff ( bioetanol ). Det brukes også i alkoholtermometre .
Formel
Etanol er en primæralkohol med to karbon med den rå formelen C 2 H 6 Oog av den semi-strukturformelen CH 3- CH 2- OHeller CH 3 -CH 2 -OH, Noe som indikerer at karbonet i metyl- gruppen (CH 3 -) Er festet til metandiyl gruppe (-CH 2 -) selv bundet til hydroksylgruppen (-OH). Det er en konstitusjonsisomer av metyleteren . Etanol betegnes vanligvis med forkortelsen "EtOH", etylgruppen (C 2 H 5 -) blir ofte forkortet "Og" i organisk kjemi .
Etternavn
Etanol er det systematiske navnet definert av nomenklaturen for organiske forbindelser for et molekyl med to karbonatomer (prefiks eth- ) med en enkelt binding mellom seg (suffiks -an ) og bundet til en hydroksylgruppe (suffiks -ol ).
Historie
Den gjæring av sukker til etanol er en av de eldste bioteknologi brukt av mennesker, spesielt i alkoholindustrien og har vært brukt siden forhistorisk tid for å oppnå alkoholholdige drikkevarer . Kjemiske analyser av organiske forbindelser som absorberes i krukker som stammer fra den stein periode funnet i en landsby i provinsen Henan i Kina , avslørte at blandinger av gjærede drikkevarer som består av ris, honning og frukt ble produsert fra den VII th tusen BC. AD .
Selv om destillasjon er en teknikk kjent alkymistene gresk-egyptiske (som zosimos av panopolis ), den første skriftlige registreringer av produksjon av alkohol fra vin går tilbake bare XII th århundre med arbeidet til alkymistene i School of Medicine of Salerno . Den første omtale av skillet mellom absolutt alkohol og vann-alkohol-blandinger er rapportert til XIII th tallet av Raymond Lully . Vær imidlertid oppmerksom på at de lærde persiske raser har isolert etanol i det nåværende X - tallet.
I 1796 fikk Johann Tobias Lowitz ren etanol ved å filtrere destillert etanol gjennom aktivt karbon . Antoine Lavoisier fastslår at etanol er sammensatt av karbon , oksygen og hydrogen , og i 1808 , Nicolas Théodore de Saussure bestemmer dets rå formel . I 1858 , Archibald Scott Couper publisert den kjemiske struktur av etanol, som var en av de første strukturer bestemt.
Etanol ble først fremstilt syntetisk i 1826 av det uavhengige arbeidet til Georges Serullas i Frankrike og Henry Hennel i Storbritannia . I 1828 , Michael Faraday syntetisert etanol ved syrekatalysert hydratisering av etylen , en syntese i likhet med industriprosessen som brukes i dag.
Etanol ble også brukt som drivstoff i lamper, og som drivstoff for biler frem til 1930-tallet . For eksempel kunne Ford T kjøre frem til 1908 på ren etanol.
Naturlig tilstedeværelse
Etanol er et flyktig biprodukt av gjær metabolisme . Det er derfor til stede i habitatene til disse organismer og i atmosfæren vår. Det finnes også utsendt av moden frukt, og i mange planter på grunn av naturlige anaerobe forhold under spiring eller når planter som mangler oksygen (i tilfelle flom for eksempel) henter energi fra gjæring.
På begynnelsen av 2000-tallet var den atmosfæriske syklusen fortsatt dårlig forstått. Vi søker å kvantifisere etanolen som avgis av planter og gjær, nivåene i atmosfæren og omdannelseshastigheten via luftens hydroksyl (ved titrering av metylkloroform ). Et første grovt estimat ga en etanolutslippsrate av planter på mellom 10 og 38 Tg / år, dvs. et stort bidrag til den estimerte totale etanol som innføres i atmosfæren årlig (mellom 25 og 56 Tg / år). År). Deretter reviderte nytt arbeid utslipp fra planter oppover: 70 Tg / år (fra 50 til 90 Tg / år), rundt 75% av etanolen som ble introdusert fra luften, ble i realiteten ødelagt av reaksjon med hydroksylradikaler i tørr eller fuktig luft. Tørr og våt avleiringer på tørt land eksisterer også.
Etanol har også blitt oppdaget i rommet , og dekker i fast form støvkorn i interstellare skyer .
Fysisk-kjemiske egenskaper
Etanol er en flyktig , fargeløs væske som har lukt. Forbrenningen er røykfri og gir en blåaktig flamme. De fysikalsk-kjemiske egenskapene til etanol kommer hovedsakelig fra tilstedeværelsen av hydroksylgruppen og den korte karbonkjeden . Hydroksylgruppen kan danne hydrogenbindinger , noe som gjør etanol mer tyktflytende og mindre flyktig enn organiske løsningsmidler med tilsvarende molekylvekt . Den brytningsindeks av etanol er høyere enn for vann (1,3594 ved 25,0 ° C ). Den trippelpunktet etanol blir observert ved -123,15 ° C for et trykk på 4,3 x 10 -4 Pa .
Egenskaper som løsemiddel
Etanol er et polært protisk løsningsmiddel . Det er blandbart med mange organiske løsningsmidler , slik som klorerte løsningsmidler ( karbontetraklorid , kloroform , trikloretan , tetrakloretylen ), alifatiske hydrokarboner ( pentan , heksan ), aromatiske løsningsmidler ( benzen , toluen , pyridin ), eddiksyre , aceton , dietyleter , den etylenglykol eller nitrometan . Imidlertid har blandingen av etanol med alifatiske hydrokarboner en tendens til å avta med økningen i lengden av karbonkjeden til alkanen og temperaturnedgangen, hvor blandbarhetsgrensen f.eks. Er 13 ° C for dodekan .
På grunn av den polare natur av den hydroksyl -gruppen , kan også oppløse etanol ioniske forbindelser , slik som natrium- og kalium -hydroksyder , magnesium- , kalsium- og ammonium-klorider, eller ammonium og natrium bromider. . Natrium- og kalium- klorider er bare svakt løselig i etanol.
Den ikke- polare delen av etanol lar den oppløse hydrofobe stoffer , spesielt essensielle oljer og mange luktende, fargestoffer og medisinske forbindelser.
Etanol kan benyttes som et oppløsningsmiddel i mange kjemiske reaksjoner under synteser , for eksempel i nukleofile S N 1 substitusjoner , under katalytiske hydrogeneringer , i løpet av aldol reaksjoner , under Wittig-reaksjoner , i løpet av Diels- reaksjoner. Alder eller ved diazotering reaksjoner .
Etanol er inert mot nesten alle mykgjorte overflater i hverdagen, lakker (unntatt celluloselakk og de med skallakk ), akryl- og glyserftalsmalinger mens det er et veldig godt løsningsmiddel. Dette gjør det til et mye brukt rengjøringsmiddel alene eller i blanding med andre forbindelser.
Blandbarhet med vann
Vann-etanolblandinger opptar et volum mindre enn summen av volumene av de to komponentene tatt hver for seg. Blandingen av et volum vann og et volum etanol gir for eksempel et ekvivalent volum på 1,92. Reaksjonen av blanding av vann og etanol er eksoterm , og ved 24,85 ° C kan opp til 777 J mol −1 frigjøres. Etanolens polare natur gjør den hygroskopisk , så mye at den absorberer fuktighet fra luften.
En azeotrop dannes med vann ved 89,47 mol-% etanol og 10,53 mol-% vann ved atmosfæretrykk . Den kokepunktet for etanol er 78,4 ° C og 100 ° C for vann, men azeotropen koker ved 78,2 ° C , som er lavere enn kokepunktene for hver. Bestanddeler. Andelene av den azeotrope blandingen varierer som en funksjon av trykket.
| Press | Kokepunkt | Etanol molfraksjonen |
|---|---|---|
| 0,1 MPa | 78,35 ° C | 0,894 |
| 0,334 MPa | 112,6 ° C | 0,882 |
| 0,689 MPa | 135,7 ° C | 0,874 |
| 1,378 MPa | 164,2 ° C | 0,862 |
| 2.068 MPa | 182,6 ° C | 0,852 |
Å tilsette noen prosent etanol i vannet reduserer vanns overflatespenning drastisk . Denne egenskapen hjelper til med å forklare fenomenet vinsyrer . Når det virvles vin i et glass, fordamper etanol raskere i den tynne filmen langs sidene av glasset. Andelen etanol avtar, slik at overflatespenningen øker og filmen blir til dråper. Dette fenomenet kalles Marangoni-effekten , og ble beskrevet og forklart i 1855 av James Thomson.
Den alkoholstyrke , også kalt alkoholisk grad er forholdet mellom volumet av alkohol som inneholdes i blandingen og det totale volum av blandingen til 20 ° C . Den brukes til å bestemme andelen alkohol, det vil si etanol, i en alkoholholdig drikke . Enheten som brukes til å uttrykke titeren er volumfraksjonen (% vol) eller grad (angitt "°").
Vann-etanolblandinger som inneholder mer enn 50% etanol er brannfarlige ved romtemperatur , men ved oppvarming kan en blanding som inneholder mindre enn 50% etanol antennes. Den matlaging teknikk bruker denne egenskapen. Alkohol tilsatt i en varm panne brenner opp i flammer og gir en kompleks reaksjon. Temperaturen på alkoholen som brenner kan deretter overstige 240 ° C og fører til karamellisering av det tilstedeværende sukkeret .
Produksjon
Etanol kan produseres industrielt fra petrokjemikalier ved hydrering av etylen og ved alkoholgjæring av gjær eller cellulose . Den mest økonomiske prosessen avhenger hovedsakelig av oljemarkedet .
Direkte katalyse
Denne prosessen, utviklet på 1970-tallet, har fullstendig fortrengt andre produksjonsmetoder. Den således produserte etanolen brukes av industrien som råvare eller løsningsmiddel . Den er produsert gjennom petrokjemi , ved hjelp av hydrering ved syrekatalyse av etylen , etter reaksjonen:
H 2- C = CH 2-+ H 2 O↔ CH 3 CH 2 OHDen mest vanlig brukte katalysator er fosforsyre , adsorbert på en porøs støtte , slik som silikagel eller kiselgur . En økning i trykket hjelper til med å forskyve likevekten mot produksjon av etanol, i henhold til prinsippet i Le Chatelier , og det er derfor å bruke en katalysator under høyt trykk av vanndamp for å nærme seg likevekt raskt. Sluttproduktet er en vann-etanol-blanding som inneholder mellom 10 % og 25 % m etanol.
Indirekte katalyse
En tidligere prosess, men nå foreldet, utviklet på 1930-tallet av Union Carbide , og vil bli brukt for mye av XX th århundre . Den etylen blir forestret med svovelsyre for å produsere etyl-sulfat , som deretter hydrolyseres for å gi etanol og svovelsyre, som således tjener som en katalysator i denne reaksjon:
H 2- C = CH 2-+ H 2 SO 4→ CH 3 CH 2 SO 4 H CH 3 CH 2 SO 4 H+ H 2 O→ CH 3 CH 2 OH+ H 2 SO 4Denne prosessen forbruker store mengder svovelsyre og krever en gassblanding av god kvalitet som tilførsel.
Gjæring
Etanol som brukes i alkoholholdige drikker produseres ved alkoholgjæring . På samme måte kommer det meste av bioetanol fra gjæringsbehandlingen av sukkerplanter, som rødbeter og sukkerrør , eller korn, som mais og hvete . Visse typer gjær , som Saccharomyces cerevisiae , metaboliserer sukker i etanol og karbondioksid , etter disse reaksjonene:
C 6 H 12 O 6→ 2-CH 3- CH 2- OH+ 2 CO 2 C 12 H 22 O 11+ H 2 O→ 4-CH 3- CH 2- OH+ 4 CO 2Fermenteringen er den gjær dyrket under gunstige betingelser for å oppnå alkoholen, ved en temperatur på omtrent 35 til 40 ° C . De mest resistente gjærstammene kan overleve i en konsentrasjon på ca. 15 vol% etanol. Toksisiteten til etanol for gjær begrenser konsentrasjonen av alkohol som kan oppnås ved brygging , og høyere konsentrasjoner kan oppnås ved mutasjon eller destillasjon . Under fermentering dannes sekundære produkter, slik som glyserol , av ravsyre , eddiksyre og amylalkohol .
For å produsere etanol fra stivelse , for eksempel fra frokostblandingsfrø, må den først omdannes til sukker. Ved brygging øl, er et frø lov til å spire ( malting ), som tillater produksjon av visse enzymer, så som cytases , amylaser , fosfataser eller peptidaser , som er nødvendige for forsukring av stivelse. For bioetanol kan denne prosessen akselereres ved bruk av svovelsyre eller ved bruk av en amylase produsert av sopp.
Celluloseholdig etanol
Den fermentering kan også fås fra cellulose , men inntil nylig kostnaden av cellulase , et enzym som er i stand til å bryte ned cellulose, ikke tillot industrien til å utvikle industrielt. I 2004 bygde det kanadiske selskapet Iogen Corporation det første anlegget basert på produksjon av etanol fra cellulose. Utviklingen av denne teknologien kan gjøre det mulig å bruke og resirkulere mye planteavfall fra jordbruk som inneholder cellulose, som sagflis eller halm . Andre bioteknologiselskaper utvikler for tiden sopp som er i stand til å produsere store mengder cellulase og xylanase for å konvertere andre landbruksrester til cellulose, som maisavfall eller bagasse fra sukkerrør .
Rensing
De forskjellige produksjonsprosessene av etanol produserer vann-etanol-blandinger. For bruk i industrien eller som drivstoff, må etanol renses. Den fraksjonerte destillasjon kan konsentrere etanol til 95,6 vol% (89,5 mol% ), og danner en blanding azeotrop med vann, hvis kokepunkt er 78,2 ° C . De vanlige metodene for å oppnå absolutt etanol inkluderer bruk av tørkemidler , slik som stivelse , glyserol eller zeolitter , azeotrop destillasjon og ekstrakt destillasjon .
Etanolegenskaper
Ulike grader av etanol er tilgjengelig for forskjellige bruksområder:
- at denaturert alkohol er typisk etanol, som er tilsatt et denatureringsmiddel for å gjøre feil blanding til matinntak. Denatureringsmidlene som brukes kan være isopropylalkohol , metanol , dietylftalat , tiofen , dietyleter eller annet naturgasskondensater . Den brukes til rengjøring, rengjøring, desinfisering og i alkoholovner . Et løsemiddel for møbelsnekker for sine shellaklakker , det er også en avfettingsmiddel i industrien, verdsatt for sin lave toksisitet på huden. Vanligvis ved 95 % vol ;
- metylert brennevin er en blanding av etanol og metanol . Metylert sprit er svært giftig på grunn av tilstedeværelsen av metanol (vanligvis 5 til 10 % vol ). Den brukes til å rengjøre vinduer og plastoverflater;
- den rektifiserte alkoholen er et destillat som måler fra 70 til 96% vol etanol ved bruk av metoden fraksjonell destillasjon . Den maksimale konsentrasjon som kan oppnås ved destillasjon av rå alkohol er 96 % vol på grunn av dannelsen av en vann-etanol- azeotrop . Den brukes til å lage likører eller vodka , men også til husholdningsvedlikehold, rengjøring eller desinfisering;
- den absolutte etanolen er etanol som inneholder maksimalt 1% vann, men de fleste av de største leverandørene innen kjemi selger under betegnelsen absolutt etanoletanol 99,8%. Det brukes som løsningsmiddel for laboratorie- og industrielle applikasjoner, og som drivstoff;
- vannfri etanol er etanol hvorfra vann er fjernet så mye som mulig. For eksempel produserer reaksjonen av absolutt etanol med metallisk magnesium etterfulgt av destillasjon ved atmosfæretrykk etanol ved 50 ppm vann (0,005% massevann eller 1/20 000). Denne etanolkvaliteten gjør det mulig å bruke den i reaksjonsfølsomme reaksjoner.
Reaktivitet og reaksjoner
Etanol er en primær alkohol og en svak syre ( p K en = 15,5), hvis korresponderende base er etanolat . Det er også en god nukleofil på grunn av reaktiviteten til de ikke- oksygenbindende dublettene . Dens reaktivitet, hovedsakelig på grunn av tilstedeværelsen av hydroksylgruppen , kan involvere reaksjoner av dehydrering , dehydrogenering , oksidasjon og forestring .
Syre-base kjemi
Etanol er et nøytralt molekyl, og pH i en løsning av etanol i vann er 7,00. Etanol kan kvantitativt omdannes til konjugatbasen , etanolationet , ved å reagere det med et alkalimetall , slik som natrium :
2 CH 3 CH 2 OH+ 2 Na→ 2 CH 3 CH 2 ONa+ H 2eller med en sterk base , slik som natriumhydrid :
CH 3 CH 2 OH+ NaH→ CH 3 CH 2 ONa+ H 2Forestring
Etanol reagerer med karboksylsyrer i nærvær av en sterk syre ( katalyse ) for å gi etyl -estere og vann i henhold til følgende reaksjon:
RCOOH+ CH 3 CH 2 OH→ RCOOCH 2 CH 3+ H 2 ODenne reaksjonen er reversibel og likevekt oppnås sakte, og krever bruk av sure katalysatorer , slik som svovelsyre , saltsyre , bortrifluorid eller paratoluensulfonsyre . For å oppnå riktige utbytter krever denne reaksjonen, som brukes i storskala industri, fjerning av vann fra reaksjonsblandingen når den dannes. Etanol kan også danne estere med uorganiske syrer, og gjør det mulig å fremstille forbindelser som er mye brukt i organisk syntese , slik som dietyl-sulfat (C 2 H 5 ) 2 SO 4eller trietylfosfat (C 2 H 5 ) 3 PO 4. Den nitritt etyl- CH 3- CH 2- O-N = Okan på samme måte fremstilles av etanol og natriumnitritt , og ble ofte brukt som et vanndrivende middel eller et middel mot influensa eller forkjølelse , før det ble trukket ut av markedet tidlig på 1980 - tallet .
Den forsåpningsreaksjon , noe som gjør det mulig for etanol som skal reformeres fra etylestere, i nærvær av en syre eller en base for å gi et karboksylat , er anvendt for fremstilling av såper .
Dehydrering
Bruk av sterke syrer kan tillate at etanol blir dehydrert for å danne dietyleter , og det produseres flere tonn dietyleter hvert år med svovelsyre som katalysator . Reaksjonen kan beskrives som følger:
2 CH 3 CH 2 OH→ CH 3 CH 2 OCH 2 CH 3+ H 2 O(ved 120 ° C )Den etylen er hovedproduktet når temperaturen overstiger 160 ° C :
CH 3 CH 2 OH→ H 2- C = CH 2-+ H 2 OForbrenning
Den forbrenning av etanol er røken og gir en blålig flamme. Forbrenningsreaksjonen danner karbondioksid og vanndamp :
CH 3 CH 2 OH( l ) + 3 O 2( g ) → 2 CO 2( G ) + 3 H 2 O( g )Den brennverdien (Δ c H °) av etanolforbrenningen er 1366,8 kJ mol −1 ved 25 ° C , og den spesifikke varmekapasiteten (C v ) er 2,438 kJ kg −1 K −1 .
Oksidasjon
Den oksidasjon (eller dehydrogenering ) etanol i nærvær av katalysatorer som gjør det mulig å oppnå etanal (eller acetaldehyd ), i henhold til følgende reaksjon:
CH 3 CH 2 OH→ CH 3 CHO+ H 2I hepatocytter i leveren , enzymet alkoholdehydrogenase tilsvarende omvendte etanol for å etanal. Ethanal er mer giftig enn etanol, og kan være ansvarlig for mange bakrus symptomer , selv om det ikke er tilstede i blodet under symptomer. I hjernen har alkoholdehydrogenase en mindre rolle i å omdanne etanol til etanol, og det er katalaseenzymet som primært katalyserer denne reaksjonen.
De siste trinnene av alkoholfermentering involverer omdannelse av pyruvat til etanol av enzymet pyruvat dekarboxylase , etterfulgt av reduksjon (eller hydrogenering ) av etanol til etanol av enzymet alkohol dehydrogenase , i dette tilfellet katalyserer den motsatte reaksjonen. Som en endogen metabolitt er etanol giftig og er mistenkt kreftfremkallende. Det skader de hematopoietiske stamcellene (ansvarlig for kontinuerlig fornyelse av blodet ); på den ene siden er det kilden til brudd i det dobbeltstrengede DNAet til disse cellene (som fremmer deres tilbakegang og skaper kromosomale omlegginger ), og på den andre siden forhindrer det riktig reparasjon ( s. 53 ) av denne skaden, som forårsaker maligniteter.
Halogenering
Etanol reagerer med hydrogenhalogensyrer for å produsere halogenalkaner , så som kloretan og brometan , via en S- N- 2 reaksjon :
CH 3 CH 2 OH+ HCl→ CH 3 CH 2 Cl+ H 2 ODenne reaksjonen krever bruk av en katalysator , slik som sinkklorid . De alkylhalogenider kan også syntetiseres ved hjelp av halogeneringsmidler så som tionylklorid eller fosfortribromid :
CH 3 CH 2 OH+ SOCl 2→ CH 3 CH 2 Cl+ SO 2+ HClHaloformreaksjon
Den haloformreaksjon er en kjemisk reaksjon som består i å syntetisere en trihalogenomethane , slik som kloroform (CHCl 3), bromform (CHBr 3) eller jodform (CHI 3), og er en av de eldste organiske reaksjonene som er beskrevet som sådan. I 1822 , Georges Serullas rapporterte omsetning av etanol med diodine og natriumhydroksyd i vann, danner natriumformiat og iodoform , deretter kalt "carbon-hydrojodid".
Etanol reagerer med natriumhypokloritt for å gi kloroform, i henhold til følgende syntese:
CH 3 CH 2 OH+ NaClO→ CH 3 CHO+ NaCl+ H 2 O CH 3 CHO+ 3 NaOCl→ CCI 3 CHO+ 3 NaOH CCI 3 CHO+ NaOH→ CHCI 3+ HCO 2 NaPå samme måte oppnås bromform og jodform henholdsvis fra natriumhypobromitt og natriumhypojoditt. Etanol er den eneste primære alkoholen som tillater denne reaksjonen.
bruk
Brensel
Etanol produsert over hele verden brukes hovedsakelig som drivstoff . Mengden etanol kan variere fra noen prosent i bensin i Vest-Europa til 95 % vol bensin i Brasil , hvor 90% av nye biler bruker flex fuel teknikken og kan kjøre på denne blandingen. Over 66% av etanolen som brukes som drivstoff, kommer fra alkoholholdig gjæring .
E85- drivstoff distribuert i Frankrike inneholder mellom 65% og 85% bioetanol, resten er bensin; frekvensen varierer mellom 65% og 75% om vinteren, og når 85% om sommeren.
Assosiert med vann, var det drivstoff for mange fly ( forbrenningsmotorer ) og raketter under andre verdenskrig, for land med få petroleumsressurser.
I Frankrike er 1% av landet viet til bioetanol. Av de atten millioner hektoliter som produseres i Frankrike årlig, brukes tolv millioner til å produsere biodrivstoff, hvorav 30% markedsføres utenfor Frankrike. Av de åtte millioner hektoliter bioetanol beregnet på biodrivstoff i Frankrike, brukes en million (eller 12%) i E85-drivstoff . En liten mengde etanol brukes også til å produsere ED95 (95% bioetanol og 5% pro-cetanadditiv) for spesielt motoriserte tunge lastebiler (inkludert busser og busser).
Alkoholholdige drikker
Etanolinnholdet (eller graden av alkohol ) i alkoholholdige drikkevarer varierer med produksjonsmåten og råmaterialet. De fleste alkoholholdige drikker kan klassifiseres mellom gjærede drikker og brennevin . De viktigste gjærede drikkene er øl , produsert av korn eller andre stivelsesproduserende planter , viner og cider , produsert av fruktjuice og mjød , produsert av honning . De åndene er produsert ved destillasjon av gjærede drikkevarer . Vi kan skille forskjellige typer spiritus , for eksempel whisky , destillert fra fermenterte frokostblandingsfrø, konjakk , destillert fra gjæret fruktjuice eller rom , destillert fra melasse eller juice. Av sukkerrør . Mange eaux-de-vie og likører tilberedes også ved å tilsette frukt, urter og krydder i brennevin , for eksempel gin som er skapt ved å infisere enebær i rettet alkohol .
Andre metoder kan brukes til å øke alkoholnivået , for eksempel fraksjonert størkning , som brukes til å lage applejack av eplejuice. Den berikede vinen tilberedes ved å tilsette den til livsvannet eller andre brennevin til delvis gjæret vin, hvilken metode som dreper gjæren mens du opprettholder noe av sukkeret.
Alkoholholdige drikker brukes til matlaging for sin duft og fordi alkohol løser opp hydrofobe luktforbindelser . Etanolen fra disse drikkene brukes også til å produsere eddik , på samme måte som industriell etanol brukes til produksjon av eddiksyre .
Råmateriale
Etanol er et viktig syntetisk mellomprodukt i kjemisk industri . Den brukes spesielt under fremstillingen av etyl- halogenider , etyl- estere, etyl- aminer , dietyleter , eddiksyre , og i mindre grad butadien .
Antiseptisk middel
Etanol brukes i det medisinske feltet i kompresser som et antiseptisk middel . Det brukes også i hydroalkoholiske oppløsninger i en konsentrasjon på ca. 60 % vol . Etanol dreper organismer ved å denaturere proteinene sine og oppløse lipidene. Det er effektivt mot de fleste bakterier og sopp , mange virus , men er ineffektivt mot sporer .
Løsemiddel
Etanol kan blandes med vann og er et godt løsningsmiddel . Det finnes i maling , industrielle fargetoner, tradisjonelle lakker, alkoholholdige drikker , markører og i kosmetikk som parfymer og deodoranter .
Medisinsk bruk
Den absolutte etanolen injiseres noen ganger i svulster for å forårsake nekrose . Imidlertid har den ikke en målrettet aktivitet siden den utvilsomt forårsaker nekrose av sunt og kreftvev.
Etanol brukes også til å behandle metanol eller etylenglykolforgiftning . I disse tilfellene konkurrerer etanol med andre alkoholer som skal metaboliseres av enzymet alkoholdehydrogenase , og reduserer dermed de toksiske derivatene som følge av metaboliseringen til aldehyder og karboksylsyrer , og reduserer de toksiske effektene på grunn av krystallisering av kalsiumoksalat (fra etylenglykol ) i nyrene .
Historiske bruksområder
Før utviklingen av moderne medisiner ble etanol brukt til forskjellige medisinske formål, inkludert behandling av depresjon og som et bedøvelsesmiddel . Det er også kjent for å kunne tjene som et sannhetsserum .
Som drivstoff ble det brukt i rakettmotorer kombinert med flytende oksygen . Under andre verdenskrig brukte det tyske " V2 " -missilet etanol blandet med 25 vol% vann for å senke temperaturen i forbrenningskammeret . Den amerikanske " PGM-11 Redstone " ballistiske raketten , inspirert av designet av den tyske V2, brukte også etanol blandet med flytende oksygen . Alkoholbaserte drivstoff til raketter og raketter ble deretter i bruk etter hvert som nye drivstoff ble utviklet.
Farmakologi
De to hovedveiene for metabolisme av etanol i leveren er alkoholdehydrogenase og oksidasjonssystem mikrosomal etanol (in) . Ved lave konsentrasjoner av etanol oksyderer alkoholdehydrogenase etanol til acetaldehyd , men ved høyere konsentrasjoner, eller med gjentatte doser etanol, dominerer det mikrosomale etanoloksidasjonssystemet.
I den europeiske farmakopeen betegner "etanol" vannfri etanol, det vil si 100% ren, i motsetning til 95 % vol eller 70 % vol etanol som finnes i apotek . Lagt til dette er kvaliteten “alkohol Ph. Eur. "(For European Pharmacopoeia ), som betegner en kvalitet på etanol som mange spor og urenheter er blitt kvantifisert for.
Fysiologiske egenskaper
Det er forskjellige effekter av alkoholholdige drikkevarer , med alkoholisme som overdreven inntak av drikkevarer som inneholder etanol, noe som fører til avhengighet, som klassifiserer etanol som et medikament. Dette ville være det mest skadelige stoffet for samfunn.
| Alkoholnivå i blodet ( g · l –1 ) |
Alkoholnivå ( % vol ) |
Symptomer |
|---|---|---|
| 0,5 | 0,05 | Eufori, avslapning |
| 1.0 | 0,1 | Depresjon, kvalme, oppkast, nedsatt sensoriske og motoriske ferdigheter, redusert kognisjon |
| > 1.4 | > 0,14 | Redusert blodstrøm til hjernen |
| 3.0 | 0,3 | Tap av bevissthet |
| 4.0 | 0,4 | Mulig død |
| 5.5 | 0,55 | Død |
Alkohol i blodet
Den BAC er mengden av etanol i blodet; det uttrykkes vanligvis i gram per liter blod. Alkoholnivåer i blodet over 4,0 g L −1 kan være dødelige, og nivået blir dødelig over 5,5 g L −1 . Lave doser etanol, under 0,5 g L −1 , forårsaker en følelse av eufori , med folk som blir mer snakkesalige, mindre hemmede og viser reduserte analytiske ferdigheter. Ved høyere doser over 1,0 g L -1 virker etanol som et depressivt middel på sentralnervesystemet , symptomer som involverer langsommere kognisjon , reduserte sensoriske evner og motorisk funksjon, bevissthetstap , til døden.
Sentralnervesystemeffekter
Etanol er et depressivt middel i sentralnervesystemet og betraktes som et medikament psykotropisk middel . Det virker på sentralnervesystemet ved å samhandle hovedsakelig med GABA A- reseptorer , og øke den hemmende effekten av nevrotransmitteren γ-aminosmørsyre (eller GABA). GABA bremser aktiviteten til nevroner (i motsetning til glutamat som er en informasjonsakselerator); ved å binde seg til GABA-reseptorer overdriver etanol således bremsing av hjernen . Det fungerer derfor som en positiv allosterisk modulator . Etanol virker også på reseptorene for serotonin , glutamat , acetylkolin og dopamin . Dens negative effekter kan forverres av bly som forbedrer oksidativt stress . Bly potenserer effekten av alkohol på sentralnervesystemet (CNS).
Langvarig inntak av etanol kan derfor forårsake permanent skade på hjernen og andre organer. Den tilbaketrekning alkohol kan føre til ulike symptomer som lidelse oppmerksomhet underskudd , økt svetting, takykardi , skjelvinger av (tremor av ekstremiteter), noen ganger kvalme eller oppkast, dehydrering, sykdomsfølelse , av hypertensjon . Noen ganger ledsages det av et anfall av epilepsi , visuelle, taktile eller auditive hallusinasjoner, det er delirium tremens i sin alvorligste form. Til slutt, og i sjeldne tilfeller, kan det oppstå smerter fra kjeven til hodeskallen. Etanol har også vist seg å forårsake endringer i størrelsen på grå materie som er synlig for det blotte øye .
Effekter på stoffskiftet
Som sådan er etanol et næringsstoff . I menneskekroppen metaboliseres det til acetaldehyd av enzymet alkohol dehydrogenase . Acetaldehyd omdannes deretter av acetaldehyddehydrogenase til acetyl-koenzym A , som er sluttproduktet av karbohydrat- og lipidmetabolisme . Imidlertid er acetaldehyd i seg selv mye mer giftig enn etanol, og er delvis ansvarlig for de fleste kliniske effekter av alkohol, som bakrus . Spesielt har det vist seg å øke risikoen for cirrhose i leveren og er knyttet til mange former for kreft .
Langtidseffekt
Etanol er klassifisert som et teratogent middel , og kan indusere føtal alkoholsyndrom , som er alkoholforgiftning av embryoet eller fosteret på grunn av mors alkoholforbruk under graviditet , og som forstyrrer utviklingsorganene.
Regelmessig inntak av alkohol er også en faktor som bidrar til økningen i triglyseridene i blodet som favoriserer utseendet til hjerte- og karsykdommer .
Etanol i alkoholholdige drikker regnes som et bestemt kreftfremkallende middel og er derfor en av kreftfremkallende stoffer fra IARC gruppe 1 .
Narkotikainteraksjoner
Etanol kan øke fenomenet sedasjon forårsaket av medikamentdempende midler som virker på sentralnervesystemet , slik som barbiturater , benzodiazepiner , opioider , fenotiaziner og antidepressiva .
Merknader og referanser
- (fr) Denne artikkelen er helt eller delvis hentet fra Wikipedia-artikkelen på engelsk med tittelen " Ethanol " ( se listen over forfattere ) .
- ETHANOL (ANHYDRO) , sikkerhetsark (er) til det internasjonale programmet for kjemisk sikkerhet , konsultert 9. mai 2009
- (in) Y. Marcus , The Properties of Solvents , Chichester, England, John Wiley & Sons , al. "Solution Chemistry" ( n o 4),1998, 254 s. ( ISBN 978-0-471-98369-9 og 0471983691 , LCCN 98018212 , online presentasjon ) , s. 95
- Marcus, 1998 , s. 88.
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 s. ( ISBN 978-0-387-69002-5 og 0-387-69002-6 , leses online ) , s. 294
- (in) Serban Moldoveanu, Forberedelse av prøve i kromatografi , Amsterdam / Boston, Elsevier ,2002, 930 s. ( ISBN 0-444-50394-3 ) , s. 258
- " Toksikologisk ark FT 48 - Etanol " , på nettstedet til National Research and Safety Institute for forebygging av arbeidsulykker og yrkessykdommer ,2011(åpnet 14. mai 2012 ) .
- (in) RH Perry og DW Green , Perrys Chemical Engineers 'Handbook , McGraw-Hill ,1997, 7 th ed. , 2640 s. ( ISBN 978-0-07-049841-9 , LCCN 96051648 ) , s. 2-50.
- (i) CA Faúndez og OJ Valderrama , " Activity Coefficient Models to Desprribe Damp-Liquid Equilibrium in Ternary Hydro-Alcoholic Solutions " , Chin. J. Chem. Eng. , vol. 17, n o toapril 2009, s. 259-267 ( ISSN 1004-9541 , DOI 10.1016 / S1004-9541 (08) 60203-7 )
- (in) William M. Haynes , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor og Francis,1 st juli 2010, 91 th ed. , 2610 s. ( ISBN 9781439820773 , online presentasjon ) , s. 14-40
- (in) O. Haida , H. Suga et al. , “ Kalorimetrisk studie av glassaktig tilstand XII. Flertall glassovergangsfenomener av etanol ” , J. Chem. Termodynamikk. , vol. 9, n o 12Desember 1977, s. 1133–1148 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (77) 90115-X ).
- (in) J. Chao og FD Rossini , " Heats of Combustion, Training, and Isomerization of alkanols Nineteen " , J. Chem. Eng. Data , vol. 10, n o 4,1965, s. 374–379 ( ISSN 0021-9568 , DOI 10.1021 / je60027a022 ).
- (i) Carl L. yaws, Handbook of Thermodynamic diagrammer: Organic Compounds C8 til C28 , vol. 1, Huston, Texas, Gulf Pub. Co.,1996, 396 s. ( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. juni 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online presentasjon ) , s. 5-89
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor og Francis,17. juni 2008, 89 th ed. , 2736 s. ( ISBN 9781420066791 , online presentasjon ) , s. 10-205
- " Etanol " , på reciprocalnet.org (åpnet 12. desember 2009 )
- [1]
- IARC arbeidsgruppe for evaluering av kreftfremkallende risikoer for mennesker, “ Globale evalueringer av kreftfremkallende egenskaper for mennesker, gruppe 1: kreftfremkallende for mennesker ” , på http://monographs.iarc.fr , IARC,16. januar 2009(åpnet 22. august 2009 )
- Sikkerhetsdatablad levert av Sigma-Aldrich, konsultert 28.9.2019
- " Etylalkohol " , på hazmap.nlm.nih.gov (åpnet 14. november 2009 )
- " ESIS " (tilgjengelig 06.12.2008 )
- (in) GP Moss ( red. ), " Basic terminology of stereochemistry " , Pure Appl. Chem. , IUPAC , vol. 68, n o 121996, s. 2193-2222 ( ISSN 0033-4545 og 1365-3075 , DOI 10.1351 / pac199668122193 ).
- (en) PE McGovern , J. Zhang et al. , “ Fermenterte drikker fra det før og førhistoriske Kina ” , Proc. Natl. Acad. Sci. USA , vol. 101, n o 51,21. desember 2004, s. 17593-17598 ( ISSN 0027-8424 , PMID 15590771 , PMCID PMC539767 , DOI 10.1073 / pnas.0407921102 , les online ).
- (no) RJ Forbes , A Short History of the Art of Destillation: From the Beginnings Up to the Death of Cellier Blumenthal , Leiden, Netherlands, Brill ,1970, 2 nd ed. ( 1 st ed. 1948), 405 s. ( ISBN 978-90-04-00617-1 , online presentasjon , les online ) , s. 89.
- " Mohammad Ibn Zakariâ Râzi (865-925), Den mest fremtredende legen i den islamske sivilisasjonen - La Revue de Téhéran | Iran ” , på www.teheran.ir (åpnet 9. juli 2016 )
- (i) " Alkohol " , på nettstedet til Encyclopaedia Britannica ,1911(åpnet 12. mai 2012 ) .
- (in) AS Cut , " was New Chemical Theory " , Philos. Mag. , 4 th serie, vol. 16,1858, s. 104-116 ( ISSN 1478-6435 , les online ).
- (i) H. Hennell , " Om den gjensidige virkningen av svovelsyre og alkohol, med bemerkninger om sammensetningen og egenskapene til den resulterende forbindelse " , Philos. Trans. R. Soc. , vol. 116,9. mars 1826, s. 240-249 ( DOI 10.1098 / rstl.1826.0021 , les online ).
- (i) Joseph DiPardo, " Utsikter for Biomasse Etanol produksjon og etterspørsel " , på Energy Information Administration (åpnes 14 mai 2012 )
- (in) VD Hunt , The Gasohol Handbook , New York Industrial Press,nitten åtti en, 580 s. ( ISBN 978-0-8311-1137-3 , online presentasjon ).
- (in) R. Dudley , " Ethanol Fruit Ripening, and the Historical Origins of Human Primate Alcoholism in Frugivory " , Integr. Komp. Biol. , vol. 44, n o 4,2004, s. 315-323 ( ISSN 1540-7063 , DOI 10.1093 / icb / 44.4.315 ).
- Kreuzwieser J, Papadopoulou E & Rennenberg H (2004) Interaksjon av fl ooding med karbonmetabolisme av skogstrær , Plant Biol., 6, 299–306, 2004
- Kimmerer TW & MacDonald RC (1987) Acetaldehyd og etanol biosyntese i blader av planter , Plant Physiol., 84, 1204–1209
- (in) S. Leblová E. Sineckáet et al. , “ Pyruvat metabolisme i spirende frø under naturlig anaerobiose ” , Biol. Plantarum , vol. 16, n o 6,1974, s. 406-411 ( ISSN 0006-3134 , DOI 10.1007 / BF02922229 ).
- Kirstine WV & Galbally IE (2011) Det globale atmosfæriske budsjettetanolet er revidert ; Atmosfærisk kjemi og fysikk 11 (1): 25909-25936 | September | DOI: 10.5194 / acpd-11-25909-2011
- (in) A. Schriver , L. Schriver-Mazzuoli et al. , “ Et mulig opphav til etanol i interstellært medium: Fotokjemi av blandede CO 2 –C 2 H 6- filmer ved 11 K. En FTIR-studie ” , Chem. Phys. , vol. 334, n bein 1-3,2007, s. 128–137 ( DOI 10.1016 / j.chemphys.2007.02.018 ).
- (en) M. Windholz ( red. ), The Merck Index: An Encyclopedia of Chemicals and Drugs , vol. 9, Merck ,1976, 9 th ed. , 1835 s. ( ISBN 978-0-911910-26-1 ).
- (no) U. Dahlmann og GM Schneider , " (flytende + væske) fase-likevekt og kritiske kurver for (etanol + dodekan eller tetradekan eller heksadekan eller 2,2,4,4,6,8,8-heptametylnonan) fra 0 , 1 MPa til 120,0 MPa ” , J. Chem. Termodynamikk. , vol. 21, n o 9,September 1989, s. 997–1004 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (89) 90160-2 ).
- (in) C. Reichardt og T. Welton , løsningsmidler og løsningsmiddeleffekter i organisk kjemi , Weinheim, Wiley-VCH ,2010, 4 th ed. , 692 s. ( ISBN 978-3-527-32473-6 , DOI 10.1002 / 9783527632220 , online presentasjon ) , “Vedlegg” , s. 568.
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , les online ) , "Etanol".
- (en) MJ Costigan , LJ Hodges et al. , “ Det isotermiske forskyvningskalorimeteret: Designmodifikasjoner for måling av eksoterme enthalpier av blanding ” , Aust. J. Chem. , vol. 33, n o 101980, s. 2103-2119 ( ISSN 0004-9425 , DOI 10.1071 / CH9802103 ).
- (in) RW Rousseau , Handbook of Separation Process Technology , John Wiley & Sons ,1987, 1010 s. ( ISBN 978-0-471-89558-9 , leses online ) , s. 261–262.
- J. Vidal , termodynamikk: anvendelse på kjemiteknikk og petroleumsindustri , Paris, Éditions Technip ,1997, 500 s. ( ISBN 978-2-7108-0715-5 , LCCN 97194455 , les online ) , s. 181.
- (i) J. Thomson , " er noen nysgjerrige bevegelser som kan observeres på overflatene av vin og andre alkoholholdige brennevin " , Philos. Mag. , vol. 10,1855, s. 330-333 ( les online ).
- (en) GA Mills og EE Ecklund , " Alkoholer som komponenter i transportbrensel " , Annu. Rev. Energi Ca. , vol. 12,November 1987, s. 47-80 ( DOI 10.1146 / annurev.eg.12.110187.000403 ).
- (en) PB Morais , CA Rosa et al. , “ Produksjon av drivstoffalkohol ved Saccharomyces-stammer fra tropiske habitater ” , Biotechnol. Lett , vol. 18, n o 111996, s. 1351-1356 ( ISSN 0141-5492 , DOI 10.1007 / BF00129969 ).
- (in) PC Badger , J. Janick ( red. ) And A. Whipkey ( red. ), Trender innen nye avlinger og nye bruksområder , Alexandria, VA, ASHS Press,2002, 599 s. ( ISBN 978-0-09-707565-5 , leses online ) , “Etanol fra cellulose: En generell gjennomgang” , s. 17–21.
- (in) MJ Taherzadeh og K. Karimi , " Syrebaserte hydrolyseprosesser for etanol fra lignocellulosematerialer: En gjennomgang " , BioRes. , vol. 2 n o 3,2007, s. 472-499 ( ISSN 1930-2126 , les online ).
- (in) MJ Taherzadeh og K. Karimi , " Enzymbaserte hydrolyseprosesser for etanol fra lignocellulosematerialer: En gjennomgang " , BioRes. , vol. 2, n o 4,2007, s. 707-738 ( ISSN 1930-2126 , les online ).
- (in) SK Ritter , " Biomasse gull burst: Teknologi for å bruke planteavledet sukker til å produsere kjemiske råvarer er klar og venter ... " , Chem. Eng. Nyheter , vol. 82, nr . 22,Mai 2004, s. 31-34 ( ISSN 0009-2347 , les online ).
- (in) " Brew Better Ethanol " på Popular Science Online ,2006(åpnet 18. mai 2012 ) .
- (in) DR Lide ( red. ), CRC Handbook of Chemistry and Physics , Boca Raton, FL, CRC Press ,2007, 88 th ed. , 2640 s. ( ISBN 978-0-8493-0488-0 ) , kap. 8 ("Analytisk kjemi") , s. 42.
- (in) HD Hinton og JA Nieuwland , " Organiske reaksjoner med borfluorid. I. The Preparation of Esters ” , J. Am. Chem. Soc. , vol. 54, n o 5,1932, s. 2017–2018 ( ISSN 0002-7863 , DOI 10.1021 / ja01344a046 ).
- (in) " Rulemaking History for OTC Sweet Spirits of Nitre Drug Products " om Food and Drug Administration (åpnet 22. mai 2012 ) .
- (in) K. Schumann og K. Siekmann , Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH Verlag ,2000( ISBN 978-3-527-30673-2 , online presentasjon ) , "Såper".
- Lide, 2007 , kap. 5 ("Termokjemi, elektrokjemi og kinetikk"), s. 70.
- Lide, 2007 , kap. 15 (“Praktiske laboratoriedata”), s. 17 .
- (i) R. Swift og D. Davidson , " Alkohol Hangover: Mechanisms and Mediators ' , Alcohol Health Res. W. , vol. 22, n o 1,1998, s. 54-60 ( les online ).
- (in) L. Hipolito , J. Sanchez et al. , “ Brain Metabolism of Ethanol and Alcoholism: An Update ” , Curr. Drug Metab , vol. 8, n o 7,oktober 2007, s. 716-727 ( ISSN 1389-2002 , PMID 17979660 , DOI 10.2174 / 138920007782109797 ).
- (pdf) Toksikologisk ark N ° 120 fra INRS, konsultert 24.6.2017
- Juan I. Garaycoechea & al. (2018) Alkohol og endogene aldehyder skader kromosomer og muterer stamceller | Nature | doi: 10.1038 / nature25154 | publisert online 3. januar 2018 | abstrakt
- (i) L. Kurti og B. Czako , Strategiske Anvendelser av navngitte reaksjoner i organisk syntese , Academic Press ,2005, 864 s. ( ISBN 978-0-12-369483-6 , online presentasjon ) , s. 264-265.
- GS Serullas , “ Karbonhydriodid . Spesielle omstendigheter der denne trippelkombinasjonen fant sted; måte å produsere det med en gang ”, Annal. Chim. Phys. , vol. 20,Mai 1822, s. 17-37 ( les online ).
- " Den siste endringen av superetanol E85..N645843 " , på usinenouvelle.com .
- (i) G. McDonnell og AD Russell , " Antiseptika og desinfeksjonsmidler: Aktivitet, handling og motstand " , Clin. Microbiol. Rev. , vol. 12, n o 1,1999, s. 147–179 ( ISSN 0893-8512 , PMCID PMC88911 , les online [PDF] ).
- (en) DG Barceloux , GR Bond et al. , " American Academy of Clinical Toxicology Practice Guidelines on the Treatment of Methanol Poisoning " , Clin. Toxicol. , vol. 40, n o 4,2002, s. 415-446 ( DOI 10.1081 / CLT-120006745 ).
- (i) YB Shvets , Washington stasjon: My Life som en KGB spion i Amerika , New York, Simon & Schuster ,1995, 298 s. ( ISBN 978-0-671-88397-3 ).
- (in) " V2 " på Rocket and Space Technology (åpnet 27. mai 2012 ) .
- (in) " Rocket Propellants " , på The Internet Encyclopedia of Science (åpnet 27. mai 2012 ) .
- (in) " A Brief History of Rocketry " på Kennedy Space Center (åpnet 27. mai 2012 ) .
- (i) LA Pohorecky og J. Brick , " Pharmacology of Ethanol " , Pharmacol. Ther. , vol. 36, n bein 2-3,1988, s. 335–427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
- (in) " Ethanolum anhydricum " på European Directorate for the Quality of Medicines (åpnet 28. mai 2012 ) .
- (in) DJ Nutt , THE King et al. , “ Drug skader i Storbritannia: en multikriteria beslutningsanalyse ” , Lancet , vol. 376, n o 9752,6. november 2010, s. 1558-1565 ( ISSN 0140-6736 , DOI 10.1016 / S0140-6736 (10) 61462-6 ).
- (en) DA Yost , “ Akutt omsorg for alkoholforgiftning. Vær forberedt på å vurdere kliniske dilemmaer ” , Postgrad Med. , vol. 112, n o 6,2002, s. 14-26 ( ISSN 0032-5481 , PMID 12510444 , DOI 10.3810 / pgm.2002.12.1361 ).
- (in) V. Santhakumar , Mr. Wallner et al. , “ Etanol virker direkte på ekstrasynaptiske undertyper av GABA A- reseptorer for å øke tonisk hemming ” , Alkohol , vol. 41, n o 3,Mai 2007, s. 211–221 ( ISSN 0741-8329 , PMID 17591544 , PMCID PMC2040048 , DOI 10.1016 / j.alkohol.2007.04.011 , les online ).
- Virgolini, MB, Mattalloni, MS, Deza-Ponzio, R., Albrecht, PA, og Cancela, LM (2019). Blyeksponering og etanolinntak: Oksidativt stress som en konvergerende virkningsmekanisme . I Neuroscience of Alcohol (s. 515-525). Academic Press ( abstrakt ).
- (en) Fein G, D Greenstein, Cardenas VA, Cuzen NL, Stein DJ et al. , " Kortikale og subkortikale volumer hos ungdommer med alkoholavhengighet, men uten substans eller psykiatriske comorbiditeter " , Psychiatry Res , vol. 214, n o 1,2013, s. 1-8. ( PMID 23916536 , PMCID PMC4203651 , DOI 10.1016 / j.pscychresns.2013.06.001 , les online [html] )
- (in) Little G, P Maurage, Kornreich C Verbanck P, S Campanella, " Binge drinking in adolescent: a review of neurophysiological and neuroimaging research " , Alcohol Alcohol , vol. 49, n o to2014, s. 198-206. ( PMID 24302160 , DOI 10.1093 / alcalc / agt172 , les online [html] )
- (en) K. Nakamura , K. Iwahashi et al. , “ Acetaldehyd addukter i hjernen til alkoholikere ” , Arch. Toxicol. , vol. 77, n o 102003, s. 591-593 ( ISSN 0340-5761 , DOI 10.1007 / s00204-003-0465-8 ).
Se også
Bibliografi
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , les online ) , "Etanol".
- (en) LA Pohorecky og J. Brick , " Pharmacology of etanol " , Pharmacol. Ther. , vol. 36, n bein 2-3,1988, s. 335–427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
Relaterte artikler
- Andre alkoholer: Alkohol , Primæralkohol , Metanol , Propanol og Butanol
- Egenskaper: Absolutt alkohol , metylert brennevin , denaturert alkohol og rektifisert alkohol
- Produksjon: Alkoholholdig gjæring , Celluloseetanol
- Bruk: Alkohol , Bioetanol , Alkoholholdige drikkevarer , Spirit drikke , alkohol industrien
- Historie: Historie om øl , Historie om vinstokker og vin
- Fysiologiske egenskaper: Alkohol dehydrogenase , Alcoholemia , alkoholisme , bakrus , alkoholforgiftning , føtalt alkoholsyndrom
- Diverse: Beregning av alkoholtitler og volumer , Alkoholnivå , Tårer av vin , Alkoholholdig maserasjon










