Acylklorid
I organisk kjemi er et acylklorid en organisk forbindelse som omfatter en funksjonell gruppe - CO - Cl , hvor deres generelle formel vanligvis betegnes RCOCl, R er en sidekjede . De anses generelt å være reaktive derivater av karboksylsyrer . De er en av de viktigste undergruppene av acylhalogenidene .
Nomenklatur
Når acylkloridfunksjonen er den prioriterte gruppen, blir acylkloridene oppkalt etter sin mors karboksylsyre ved å erstatte ordet "syre" med "klorid", suffikset "ic" med "yle" og sette inn et "de" (eller " d '") mellom de to ordene:
- den eddiksyre / etan blir acetylklorid / etanoyl , CH 3 COCl;
- at benzosyre er den benzoylklorid C 6 H 5 COCl.
Når en annen gruppe har prioritet, krever tilstedeværelsen av en acylkloridgruppe tilsetning av et "klorkarbonyl-" prefiks til navnet på molekylet: eks. : (klorkarbonyl) eddiksyre, ClOCCH 2 COOH. Prefikset "kloroformyl-" forekommer også noen ganger, f.eks. : etyl-6- (kloroformyl) heksanoat.
Eiendommer
Uten å ha muligheten til å danne hydrogenbindinger , har acylklorider lavere smelte- og kokepunkter enn deres tilsvarende karboksylsyre. For eksempel koker eddiksyre ved 118 ° C mens acetylklorid koker ved 51 ° C . Som de fleste karbonylforbindelser har de et absorpsjonsbånd på 1750 cm -1 i infrarød spektroskopi .
Syntese
I industrien
Metoden for industriell syntese av acetylklorid involverer reaksjonen av eddiksyreanhydrid med hydrogenklorid . For benzoylklorid brukes delvis hydrolyse av (triklormetyl) benzen :C 6 H 5 CCl 3 + H 2 O → C 6 H 5 C (O) CI + 2HCl
I laboratoriet
I laboratoriet fremstilles acylklorider generelt på samme måte som alkylklorider, og erstatter -OH-gruppen i en karboksyl med et klorid. Karboksylsyrene blir således behandlet med tionylklorid (SOCh 2 ), fosfortriklorid (PCl 3 ) eller fosforpentaklorid (PCL 5 ):
- R-COOH + SOCh 2 → RCOCl + SO 2 + HCl
- 3 RCOOH + PCl 3 → 3 RCOCl + H 3 PO 3
- RCOOH + PCl 5 → RCOCl + POCl 3 + HCl
Reaksjonen med tionylklorid kan katalyseres av dimetylformamid . I denne reaksjonen blir svoveldioksid (SO 2 ) og hydrogenklorid (HCl) som genereres er i gassform, og kan derfor unnslippe fra reaksjonsmediet, forskyvning av reaksjon i retning av syntesen. Et overskudd av tionylklorid (kokepunkt 74,6 ° C ) kan også lett fordampes. Reaksjonsmekanismene for reaksjoner med tionylklorid eller fosforpentaklorid er like, som med tionylklorid er vist nedenfor:
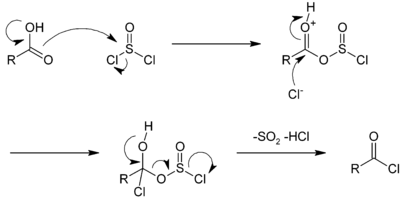
Det første trinnet består av en nukleofil substitusjon av karboksylet på tionylkloridet som frigjør et kloridion. Dette ionet tilsettes deretter karbonet i karboksylgruppen, deretter omorganiseres forbindelsen til acylklorid, hvorved H + ionet i hydroksylgruppen frigjøres fra svoveldioksid til et kloridion.
En annen metode er å bruke oksalylklorid :RCOOH + ClCOCOCl → RCOCl + CO + CO 2 + HCl
Denne reaksjonen katalyseres av dimetylformamid (DMF), som reagerer med oksalylklorid i det første trinnet for å gi et iminium- mellomprodukt :
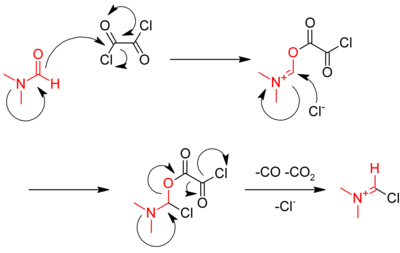
Imimium reagerer deretter med karboksylsyren, fjerner oksygen fra det og overfører kloridet til det, regenererer katalysatoren:

Vi bruker også metoder som ikke frigjør HCl, for eksempel Call-reaksjonen :R-COOH + Ph 3 P + CCl 4 → RCOCl + Ph 3 PO + HCCl 3
eller anvendelse av cyanurklorid (C- 3- N- 3- Cl 3 ):

Reaksjoner
Nukleofile reaksjoner
Acylklorider er veldig reaktive, spesielt sammenlignet med deres karboksylsyreanaloger, hvor kloridionet er en utmerket forlatende gruppe, mens -OH-gruppen i karboksylen forlater med vanskeligheter under normale forhold. Selv en svak nukleofil kan angripe karbonylen. En vanlig reaksjon - vanligvis parasittisk - er reaksjonen med vann som danner en karboksylsyre:
RCOCl + H 2 O → RCO 2 H + HClAcylklorider kan brukes til å syntetisere acylderivater, så som syreanhydrider , estere eller amider ved å reagere dem med henholdsvis et karboksylsyresalt, en alkohol eller et amin , reaksjoner kalt nukleofile substitusjoner. Acyl . Bruken av en natriumhydroksyd- eller pyridinbase , for eksempel, eller et overskudd av amin (når man fremstiller amider) er ønskelig for å eliminere det dannede hydrogenklorid og for å katalysere reaksjonen. Selv om det generelt er mulig å danne estere eller amider fra karboksylsyrer og alkoholer / aminer, er disse reaksjonene reversible og forårsaker lavt utbytte. Tvert imot er reaksjonene av syntese av estere eller amider via acylklorider (selv syntetisert fra karboksylsyrer) raske og irreversible, så det er ofte å foretrekke å velge totrinnsveien (å danne acylklorid for å reagere det med alkoholen eller aminen) som ett-trinns rute.
Med nukleofile karboner som Grignard-reagenser reagerer acylklorider først en første gang for å gi et keton , og reagerer deretter en gang til for å gi den tilsvarende tertiære alkoholen. Et bemerkelsesverdig unntak er reaksjonen med noen organocadmians der reaksjonen stopper på ketonstadiet . Den nukleofile reaksjonen med Gilmans reagens (litiert diorganokuprat) gjør det også mulig å produsere ketoner på grunn av den reduserte reaktiviteten. Acylklorider av aromatiske syrer er generelt mindre reaktive enn de av alkylsyrer og krever derfor hardere betingelser for å reagere.
Acylklorider reduseres til primære alkoholer av sterke hydridgivere, slik som litiumtetrahydruroaluminat og diisobutylaluminiumhydrid (DIBAL). Litium tri-tert-butoxyaluminumhydrid, en hindret hydriddonor, reduserer acylklorider til aldehyder, det samme gjør Rosenmund-reduksjon som bruker dihydrogen over en forgiftet palladiumkatalysator.
Elektrofile reaksjoner
Med Lewis- syrekatalyse slik som jernklorid eller aluminiumklorid , kan acylklorider brukes i Friedel-Crafts-acylering for å gi en fenon :
I det første trinnet får Lewis-syre kloridet til å dissosiere:

Dette trinnet følges av et nukleofilt angrep på arenaen mot acylgruppen:

Til slutt til kloridet rekombinerer med hydrogenioner som frigjøres av arenaen danne HCl og AlCl 3 katalysatoren regenereres:

Risiko
På grunn av reaktiviteten bør det utvises forsiktighet når du håndterer acylklorider. De er tåregass fordi de reagerer med vann på øyets overflate for å produsere saltsyre og organiske syrer som irriterer øyet. Lignende problemer kan oppstå som et resultat av innånding av acylkloriddamp.
Merknader og referanser
- Nomenklatur for organisk kjemi , R-5.7.6 Syrehalogenider
- Takao Maki, Kazuo Takeda “Benzoic Acid and Derivatives” Ullmanns Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a03_555
- (in) Boyd, Robert W. Morrison, Robert, organisk kjemi , Englewood Cliffs, NJ, Prentice Hall,1992, 1278 s. ( ISBN 0-13-643669-2 ) , s. 666–762
- (en) Clayden, Jonathan, Organisk kjemi , Oxford, Oxford University Press,2001, 1508 s. ( ISBN 0-19-850346-6 ) , s. 276–296
- " Trifenylfosfin-karbon tetraklorid Taschner, Michael J. e-EROS: Encyclopedia of Reagents for Organic Synthesis , 2001
- (in) K. Venkataraman og DR Wagle, " Cyanuric chloride: a Useful reagens for converting carboxylic syres to chlorides, esters, amides and peptides " , Tet. Lett. , vol. 20, nr . 32,1979, s. 3037–3040 ( DOI 10.1016 / S0040-4039 (00) 71006-9 )
- (in) William Reusch, " Carboxylic Acid Derivatives " , VirtualText of Organic Chemistry , Michigan State University
- (fr) Denne artikkelen er delvis eller helt hentet fra Wikipedia-artikkelen på engelsk med tittelen " Acylklorid " ( se forfatterlisten ) .