Glykolyse
Den glykolyse ( γλῠκὖς Glykys "søt" og λύσις Lysis 'frigjøring') eller Embden-Meyerhof-Lotte er en metabolsk vei av glukoseopptak og energiproduksjon. Det foregår i hyaloplasma (eller cytosol) i cellen . Som navnet antyder, krever det glukose og tillater produksjon av pyruvat . Sistnevnte kan enten komme inn i Krebs-syklusen , som finner sted i mitokondriene av eukaryoter eller cytoplasmaet til bakterier i aerobiose, eller metaboliseres ved gjæring i anaerobiose, for eksempel for å produsere laktat eller etanol .
Generelt prinsipp
Glykolyse er en ATP- regenereringsmekanisme som ikke krever oksygen . I løpet av denne prosessen er vi vitne til:
- av redoksreaksjonene der en akseptor av elektroner ( koenzym NAD + ) reduseres:
- syntese av ATP ved fosforylering av ADP (dannelse av fire ATP- molekyler , men forbruk av to ATP- molekyler , eller en total netto-dannelse av to ATP- molekyler ):
Symbolet P jeg representerer her den uorganisk fosfat HPO 4 2-eller hydrogenfosfat.
Ettersom glykolyse resulterer i reduksjon av koenzymer, ledsages den derfor av oksidasjon av organiske molekyler. Vi kan si at det tilsvarer oksidasjonen av glukose til pyruvat :
glukose + 2 NAD + → 2- CH 3 -CO-COO -+ 2 ( NADH + H + ),kombinert med:
2 ADP + 2 P i + 2 H + → 2 ATP + 2 H 2 O,totalt
glukose + 2 ADP + 2 P i + 2 NAD + → 2 pyruvat * + 2 ATP + 2 ( NADH + H + ) + 2 H 2 O.* Den pyruvate CH 3 CO-COO -strengt tatt betegner korresponderende base av pyrodruesyre CH 3 CO-COOH.
| D - glukose | Pyruvat | ||||
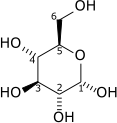
|
+ 2 ADP + 2 P i + 2 NAD + |
|
2 |
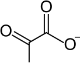
|
+ 2 ATP + 2 (NADH + H + ) + 2 H 2 O |
Glykolyse er av avgjørende betydning for kroppen, da det er hovedveien for glukosemetabolisme. Det er den eneste metabolske energikilden for hjernen , som raskt trekker sammen skjelettmuskler eller erytrocytter , bortsett fra i perioder med langvarig faste eller langvarig fysisk aktivitet. Så snart leverglykogenreservene er ferdige, vil kroppen nedbryte lipidene for å frigjøre frie fettsyrer og glyserol i blodet , som vil bli transformert av beta-oksidasjon til ketonlegemer . Det vil da være disse ketonlegemene som vil mate hjernen og resten av kroppen. Når det er produsert, kan pyruvat følge flere metabolske veier avhengig av miljøforholdene.
- I de fleste vev, når oksygen er rikelig, oksyderer pyruvat og mister karboksylgruppen i form av CO 2 , og den gjenværende to-karbon-enheten går inn i sitronsyresyklusen og gjennomgår deretter oksidativ fosforylering, i en prosess som kalles cellulær respirasjon .
- Ellers, i fravær av oksygen, kan pyruvat reduseres til laktat gjennom koblet oksidasjon av NADH + H + til NAD + . Denne prosessen, kalt melkefermentering , finnes også i visse mikroorganismer, for eksempel melkesyrebakterier som brukes til fremstilling av yoghurt.
- Til slutt, i mikroorganismer som gjær og i vev av visse planter , kan pyruvat reduseres til etylalkohol ( etanol ), igjen med koblet oksidasjon av NADH til NAD + . Det er alkoholholdig gjæring .
Stadier av glykolyse
Serien med 10 reaksjoner av glykolyse kan deles inn i tre faser:
- Fase 1: Glukose, en art med 6 C-C-atomer, blir først fosforylert ved C- 6 og C- 1 posisjoner (reaksjonene 1, 2 og 3);
- Fase 2: den spaltes deretter i to tre-karbonmolekyler i form av glyseraldehyd-3-fosfat (reaksjon 4 og 5)
- Fase 3: energien som investeres i fosforyleringene gjenvinnes endelig i form av ATP (reaksjonene 6 til 10).
Fase 1: Aktivering av heksoser ved påfølgende fosforyleringer
Fosforylering av glukose til glukose-6-fosfatDenne reaksjonen krever en Mg 2+ kation som en kofaktor og forbruker ett ATP- molekyl for å fosforylere hvert glukosemolekyl . Det hjelper å holde glukosekonsentrasjonen relativt lav i cytoplasmaet for å lette innføringen av ytterligere glukosemolekyler. I tillegg kan glukose-6-fosfat ikke lenger forlate cellen, fordi plasmamembranen ikke har en transportør for dette molekylet.

|
+ ATP → ADP + H + + |
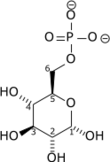
|
| Glukose | Glukose-6-fosfat | |
| Hexokinase - EC | ||
Denne reaksjonen er irreversibel. Den katalyseres av en kinase , enten en heksokinase , ikke-spesifikk for glukose, som hos pattedyr ofte finnes i muskler , eller en glukokinase , spesifikk for glukose . Disse to enzymer har forskjellige Michaelis konstanter ( K- M ) med tilsvarende verdier 0,1 mM og 10 mM vite at K M er omvendt proporsjonal med enzymets affinitet til dets substrat. Disse to enzymene er Mg 2+ avhengige. Hos mennesker er glukokinase lokalisert i leveren og i bukspyttkjertelcellene . Faktisk er sistnevnte perfekt egnet til lagringsfunksjonen i leveren (den fungerer hovedsakelig under en stor tilstrømning av glukose, for eksempel etter et måltid, og bidrar dermed til regulering av blodsukker ). En dysfunksjon av dette enzymet er derfor ansvarlig for visse typer diabetes (MODY-diabetes som i 50% av tilfellene skyldes en mutasjon i glukokinase ).
Glukosefosforylering er ikke spesifikk for glykolyse. Dette trinnet fungerer også som et utgangspunkt i pentosefosfatveien eller for glykogenogenese.
Merk: alle reaksjoner som har en høy fri entalpi- variasjon er irreversible, og da denne fosforyleringen er energisk meget favorisert, er reaksjonen irreversibel. Dette er grunnen til at disse enzymene er høyt regulerte for å forhindre at systemet løper, som de to andre irreversible trinnene for glykolyse. ( Phosphofructokinase-1 , Pyruvat kinase ). Heksokinase hemmes spesielt av sitt eget produkt, glukose-6-fosfat ( negativ tilbakemelding ), og dets genuttrykk er indusert av insulin . Glukokinase hemmes ikke av glukose-6-fosfat, men dets genuttrykk er indusert av insulin.
Fruktose-6-fosfatisomeriseringDen α- D -glukose-6-fosfat frembringes under glykolyse er isomerisert til β- D -fructose-6-fosfat av glukose-6-fosfat-isomerase (GPI) eller phosphohexose isomerase. Denne reaksjonen er reversibel, og forblir orientert mot høyre på grunn av konsentrasjonen av Fru-6-P, som holdes ganske lav på grunn av dets umiddelbare forbruk ved det følgende trinn av glykolyse.
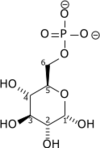
|

|
|
| Glukose-6-fosfat | Fruktose-6-fosfat | |
| Glukose-6-fosfatisomerase - EC | ||
Den β- D -fructose-6-fosfat (Fru-6-P) dannet under den foregående reaksjon er fosforylert til β- D -fructose-1,6-bisfosfat (Fru-1,6-BP) ved fosfofruktokinase -1 ( PFK-1) fra et ATP- molekyl , konvertert til ADP . Dette energiforbruket gjør dette trinnet irreversibelt, og utgjør et viktig punkt for regulering av hastigheten på glykolyse. En Mg 2+ kation fungerer som en kofaktor .

|
+ ATP → ADP + H + + |

|
| Fruktose-6-fosfat | Fruktose-1,6-bisfosfat | |
| Fosfofruktokinase-1 - EC | ||
Det er, hovedsakelig i andre organismer enn dyr , forskjellige enzymer som er i stand til å fosforylere fruktose-6-fosfat fra uorganisk pyrofosfat i stedet for ATP. Dette er tilfellet med difosfat fruktose-6-fosfat 1-fosfotransferase (PFP), som finnes i mange planter , visse bakterier , arkeaer og protister . Sjeldne arkeaer har en variant av fosfofruktokinase ved bruk av denne gangen ADP og ikke ATP.
Denne reaksjonen, katalysert av en fosfofruktokinase (PFK), er irreversibel og Mg 2+ avhengig. Dette enzymet katalyserer det første trinnet som er spesifikt for glykolyse. Det er sterkt kontrollert allosterisk ATP- fri (ATP- fri er formen av ikke-kompleksert magnesium ATP), som er sluttproduktet "nyttig" for glykolyse. Jo høyere konsentrasjon av fri ATP , jo langsommere er denne reaksjonen, og omvendt, jo lavere konsentrasjon av fri ATP , desto mer aktivt er enzymet. Dette er et selvkontrollsystem for glykolyse. Flere matematiske modeller av glykolyse er utviklet og viser at dette trinnet er det viktigste av dem som styrer glykolysestrømmen.
Hemming av ATP er reversibel av AMP , noe som gjør det mulig å holde et ATP / AMP-forhold konstant.
Men det er fremfor alt regulert av fruktose-2,6-bisfosfat : faktisk har produksjonen av fruktose-2,6-bisfosfat fra fruktose-6-fosfat den eneste funksjonen å demonstrere metning av banen i fruktose-6-fosfat ("for full") fordi fruktose-2,6-bisfosfat ikke trenger å bli metabolsk. Ved allostery aktiverer fruktose-2,6-bisfosfat derfor fosfofruktokinase-1 for å stimulere forbruket av fruktose-6-fosfat og dermed forhindre dets egen dannelse.
Fase 2: spaltning av fruktose-1,6-bisfosfat i to molekyler glyceraldehyd-3-fosfat
Spalting i glyseraldehyd-3-fosfat og dihydroksyacetonfosfatDen β- D -fructose-1,6-bisfosfat spaltes ved en lyase , den fructose-aldolase , i D -glyceraldehyde-3-fosfat (g3p) og dihydroksyaceton fosfat (DHAP).

|

|
+ |

|
|
| Fruktose-1,6-bisfosfat | G3P | DHAP | ||
| Fruktose bisfosfat aldolase - EC | ||||
Det er to klasser av aldolaser som er i stand til å spalte fruktose-1,6-bisfosfat: klasse I hos dyr og planter , og klasse II i sopp og bakterier ; disse to enzymklassene bruker forskjellige mekanismer for å spalte denne ketosen .
Isomerisering av dihydroksyacetonfosfat til glyseraldehyd-3-fosfatDen fosfat dihydroksyaceton er isomeriseres i D -glyceraldehyde-3-fosfat ved triosefosfatisomerase . Denne reaksjonen er ikke særlig favorisert, den finner sted med en hastighet på 5% i "dihydroxyacetonephosphate → glyceraldehyde-3-phosphate" -retningen og 95% i den andre retningen.

|

|
|
| DHAP | G3P | |
| Triose-phosphate isomerase - EC | ||
Selv om ketoseformen (DHAP) i likevekt er mye rikere enn aldoseformen (G3P), er transformasjonen DHAP → G3P rask fordi G3P-forbindelsen elimineres permanent ved følgende reaksjoner av glykolyse.
Dermed resulterer hvert molekyl av β- D- fruktose-1,6-bisfosfat til slutt i to molekyler D- glyceraldehyd-3-fosfat (G3P).
Fase 3: Gjenoppretting av energi investert i fosforyleringer
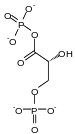
Fosforylering til 1,3-bisfosfoglyserinsyreDen D -glyceraldehyde-3-fosfat er fosforylert i 1,3-bisphospho- D -glycérate (1,3-BPG) av glyseraldehyd 3-fosfat dehydrogenase med ledsagende reduksjon av et molekyl av NAD + til NADH + H + ; det er det eneste trinnet i glykolyse hvor reduserende kraft dannes, i form av NADH + H + . Denne reaksjonen balanseres fra synspunktet til den elektriske ladningen og antallet hydrogenatomer ved at det uorganiske fosfatet (Pi) eksisterer, i det cytoplasmatiske mediet , i form av hydrogenfosfationen HPO 4 2-.

|
+ NAD + + Pi NADH + H + + |
|
| G3P | 1,3-BPG | |
| Glyseraldehyd-3-fosfatdehydrogenase - EC | ||
Denne redoksreaksjonen, reversibel og katalysert av en oksidasoreduktase , fører til dannelsen av en acyltioesterbinding med høyt overføringspotensial. Dette trinnet utgjør starten på den andre delen av glykolyse. Energien i bindingene med høyt overføringspotensial vil bli brukt til syntesen av ATP. Koenzymer er redusert (forsterkning av elektroner).
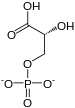
Konvertering til 3-fosfoglyserat med ATP-utvinningDen høye overføringspotensiale fosfatgruppen av 1,3-bisfosfo- D- glycerat (1,3-BPG) tillater at et ADP- molekyl fosforyleres til ATP for å danne 3- fosfo - D- glycerat ( 3PG ) under påvirkning av fosfoglyseratkinase ; det er det første trinnet i glykolyse der energi gjenvinnes i gjenbrukbar form, lagret i ATP.

|
+ ADP ATP + |
|
| 1,3-BPG | 3PG | |
| Fosfoglyseratkinase - EC | ||
Den 3-fosfo- D -glycérate er isomeriseres til 2-fosfo- D -glycérate (2PG) ved fosfoglyseratmutase .

|
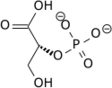
|
|
| 3PG | 2PG | |
| Fosfoglyseratmutase - EC | ||
Den 2-fosfo- D -glycérate (2PG) er dehydrert ved en lyase , den enolase til (eller phosphopyruvate hydratase) danner fosfoenolpyruvat (PEP). En Mg 2+ kation er nødvendig som en katalysator for dehydreringsreaksjonen , mens en annen Mg 2+ griper inn med en "konformasjonell" rolle i samordning med karboksyl -gruppen av 2-fosfo- D -glycerate.

|
H 2 O + |

|
| 2PG | PEP | |
| Enolase (fosfopyruvathydratase) - EC | ||
Den gruppe fosfat ved høy overføringspotensial ( Ag ° ' = -61,9 kJ mol -1 ) av fosfoenolpyruvat tillater fosforylering av et molekyl av ADP til ATP av pyruvat kinase . En Mg 2+ kation er nødvendig for denne reaksjonen som en kofaktor .

|
+ ADP + H + → ATP + |

|
| PEP | Pyruvat | |
| Pyruvatkinase - EC | ||
Under denne reaksjonen omdannes fosfoenolpyruvat faktisk irreversibelt til enolpyruvat ved hjelp av pyruvatkinase, og enolpyruvat gir deretter reversibelt pyruvat ved tautomerisme .
Glykolysevurdering

Er brukt:
Å produsere :
Slik at 2 mol ATP produseres ved å behandle 1 mol glukose.
Regulering av glykolyse
Glykolyse er hovedsakelig regulert på nivået med tre viktige enzymer: PFK-1 , pyruvatkinase og heksokinase .
Regulering av PFK-1
Den PFK-1 reguleres slik allosterisk :
- Den ATP og sitrat virker som inhibitorer
- Den AMP og fruktose 2,6-bisfosfat virker som aktivatorer.
Konsentrasjonen av fruktose-2,6-bisfosfat er derfor viktig for glykolyse. Det reguleres av fosfofruktokinase-2, hvis aktivitet er forskjellig avhengig av fosforyleringstilstanden:
- under effekten av insulin ( hypoglykemisk hormon ) defosforyleres det og katalyserer reaksjonen fruktose-6-fosfat + ATP → fruktose-2,6-bisfosfat + ADP ; konsentrasjonen av fruktose-2,6-bisfosfat øker og glykolyse akselereres.
- under virkningen av glukagon (hyperglykemiske hormon), er det fosforyleres og katalyserer reaksjonen: fruktose-2,6-bisfosfat + H 2 O→ fruktose-6-fosfat + Pi ; konsentrasjonen av fruktose-2,6-bisfosfat avtar og glykolyse reduseres.
Regulering av pyruvatkinase
Den pyruvat kinase er regulert allosterisk og dette ubikvitært:
- Den AMP og fruktose 1,6-bisfosfat er aktivatorer
- Den ATP , den acetyl-CoA og alanin er inhibitorer.
I leveren er det også regulert kovalent (av hormoner )
- den glukagon virker ved fosforylering av dette enzym , som har den effekt at det forhindrer
- de insulin utfører den motsatte handling, som har effekten av aktiverende pyruvat kinase.
Regulering av heksokinase
Aktiviteten til dette enzymet inhiberes av reaksjonsproduktet glukose-6-fosfat . Hvis det akkumuleres, reduseres produksjonen raskt for å balansere med forbruket. Denne prosessen forhindrer opphopning av metabolitter .
Reoksidering av koenzymer
Glykolyse opphører når de reduserte koenzymer ikke blir oksidert, spesielt når NADH ikke regenereres i NAD + -formen . For eksempel kan trinnet katalysert av glyseraldehyd-3-fosfatdehydrogenase ikke forekomme uten NAD + :

|
|
Oksidasjon kombinert med fosforylering av glyseraldehyd-3-fosfat (G3P) til 1,3-bisfosfoglyserat (1,3-BPG) |
.
Det er to hovedmetabolske veier for dette, avhengig av redoks- tilstanden til mediet:
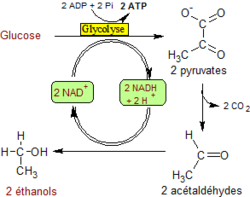
1) en, i et anaerobt miljø , kalt gjæring , skjer ved fosforylering på nivået av substratet og aksept av elektroner av en organisk substans. Det er flere typer: melkesyregjæring (som forekommer i muskelen uten oksygen) gjæring smørsyre , alkoholholdig gjæring . Ved melkegjæring reduseres pyruvat direkte av NADH til laktat . Ved alkoholgjæring forårsaket av gjær forlenges glykolyse med to ytterligere reaksjoner: dekarboksylering av pyruvat til acetaldehyd og deretter reduksjon av sistnevnte til etanol . Det er derfor i det første tilfellet pyruvatet som fungerer som den siste elektronakseptoren og acetaldehydet i det andre tilfellet.

|
|
|
|
Melkesyre gjæring : regenereringen av NAD + er sikret ved den direkte reduksjon av pyruvat til laktat pyruvat + 2 H + + 2 e - → laktat |
Alkoholgjæringen : regenereringen av NAD + sikres ved reduksjon av acetaldehyd til etanol acetaldehyd + 2 H + + 2 e - → etanol |

|
| → glykolyse Krebs syklus → respirasjonskjeden Den endelige akseptor for protoner og elektroner er oksygen til luften |
Energibalansen ved glykolyse etterfulgt av respirasjon (32 ATP) er omtrent 20 ganger høyere enn glykolyse etterfulgt av gjæring (2 ATP for melkesjæring).
Merknader og referanser
- Molecular biology of the cell av Harvey Lodish, Arnold Berk, Paul Matsudaira, James Darnell , Chris A. Kaiser, Pierre L. Masson - side 301.
- Stephen D. Anton , Keelin Moehl , William T. Donahoo og Krisztina Marosi , " Flipping the Metabolic Switch: Understanding and Applying Health Benefits of Fasting ", Fedme (Silver Spring, Md.) , Vol. 26, n o tofebruar 2018, s. 254–268 ( ISSN 1930-7381 , PMID 29086496 , PMCID 5783752 , DOI 10.1002 / oby.22065 , lest online , åpnet 19. september 2019 )
- (in) Reginald H. Garrett og Charles M. Grisham , Biochemistry , Wadsworth Publishing Co Inc,2012, 5 th ed. , 1280 s. ( ISBN 978-1-133-10629-6 og 1-133-10629-3 , les online )
- Pascal Ribéreau-Gayon , Denis Dubourdieu , Bernard Donèche og Aline Lonvaud , Ønologi-traktaten , t. 1: Vinbiologi. Vinproduksjon , DUNOD,3. oktober 2012, 6 th ed. ( ISBN 978-2-10-058234-1 og 2-10-058234-8 )
- (in) HS Seeholzer, A. Jaworowski, IA Rose , " enolpyruvat: kjemisk bestemmelse som pyruvatkinase-mellomprodukt " , Biochemistry , vol. 30, n o 3, 22. januar 1991, s. 727-732 ( les online )
- George B. Johnson , Jonathan B. Losos , Peter H. Raven og Susan S. Singer ( trans. , Fra engelsk) Biologi: luksus versjon , Brussel / Paris, Superior De Boeck 15. november 2009, 1406 s. ( ISBN 978-2-8041-6638-0 )
- Joseph-Pierre Guiraud , Food mikrobiologi , DUNOD, 18. september 2012, 2 nd ed. ( ISBN 978-2-10-057008-9 og 2-10-057008-0 )
Se også
Relaterte artikler
Andre ruter for glukose nedbrytning:
