4-klorfenol
| 4-klorfenol | |||
|
|||
| Identifikasjon | |||
|---|---|---|---|
| Systematisk navn | 4-klorfenol | ||
| Synonymer |
para klorfenol, p- klorfenol , 4-CP |
||
| N o CAS | |||
| N o ECHA | 100,003,094 | ||
| N o RTECS | SK2800000 | ||
| DrugBank | DB13154 | ||
| PubChem | 4684 | ||
| SMIL |
C1 = CC (= CC = C1O) Cl , |
||
| InChI |
InChI: InChI = 1S / C6H5ClO / c7-5-1-3-6 (8) 4-2-5 / h1-4,8H InChIKey: WXNZTHHGJRFXKQ-UHFFFAOYSA-N |
||
| Utseende | fargeløse til grå fenollignende luktnåler |
||
| Kjemiske egenskaper | |||
| Brute formel |
C 6 H 5 Cl O [isomerer] |
||
| Molarmasse | 128,556 ± 0,007 g / mol C 56,06%, H 3,92%, Cl 27,58%, O 12,45%, |
||
| pKa | 9.38 | ||
| Fysiske egenskaper | |||
| T ° fusjon | 43 ° C | ||
| T ° kokende | 220 ° C | ||
| Løselighet | 27 g · l -1 (vann, 20 ° C ) | ||
| Volumisk masse | 1,31 g · cm -3 ( 20 ° C ) | ||
| Flammepunkt | 121 ° C | ||
| Mettende damptrykk | 13- 15 hPa ( 20 ° C ) 1,42 hPa ( 50 ° C ) |
||
| Dynamisk viskositet | 5 cP ( 25 ° C ) | ||
| Termokjemi | |||
| Δ fus H ° | 13.600 kJ · mol -1 | ||
| Δ vap H ° | 47,04 kJ · mol -1 | ||
| Optiske egenskaper | |||
| Brytningsindeks |
1,5419 1,5579 |
||
| Forholdsregler | |||
| SGH | |||
   Fare H290, H302, H312, H314, H332, H411, H290 : Kan være etsende for metaller H302 : Farlig ved svelging H312 : Farlig ved hudkontakt H314 : Gir alvorlige etseskader på hud og øyne H332 : Farlig ved innånding H411 : Giftig for vannlevende organismer, med langtidsvirkninger |
|||
| Transportere | |||
60 : stofftoksisk eller med en mindre grad av toksisitet FN-nummer : 2020 : KLOROFENOLSTØRRELSER Klasse: 6.1 Klassifiseringskode: T2 : Giftige stoffer uten subsidiær risiko: Organisk, fast stoff; Etiketter: 6.1 : Giftige stoffer 9.1 Emballasje Emballasje gruppe III : substanser med liten fare.   |
|||
| Økotoksikologi | |||
| DL 50 |
670 mg · kg -1 (rotte, oral ) 15 000 mg · kg -1 (rotte, dermal) |
||
| LogP | 2.39 | ||
| Beslektede forbindelser | |||
| Isomer (er) |
2-klorfenol 3-klorfenol |
||
| Enheter av SI og STP med mindre annet er oppgitt. | |||
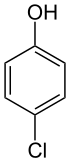
Den 4-klorfenol er en aromatisk forbindelse med formelen C 6 H 5 ClO(ClC 6 H 4- OH). Bestående av en av en benzenring substituert med en hydroksylgruppe ( fenol ) og et kloratom i posisjon 1,4-, er det en av de tre isomerene av monoklorfenol , para- forbindelsen .
Eiendommer
4-klorfenol kommer i form av fargeløse til grå nåler med en ubehagelig og gjennomtrengende fenollignende lukt
Det er lite løselig i vann ( 27,7 g · l -1 ) og også mer tett (1,31). På den annen side er den veldig løselig i etanol , eter , kloroform og benzen , og løselig i alkalisk medium.
De nåler som smelter ved 43 ° C , og etter å ha flytende form til 224 ° C . 4-klorfenol brytes ned ved oppvarming og produserer hydrogenklorid , fosgen og polyklorerte dibenzodioksiner .
Forbindelsen er brennbar ( flammepunkt på 120 ° C , lukket kopp) men ikke veldig brannfarlig.
Med en pK A på 9,31 er den veldig litt surere enn fenol (9,99); dette forklares med -I-effekten av klor som stabiliserer den anioniske formen fenolat , men på grunn av sin posisjon overfor hydroksylgruppen på ringen er denne effekten svakere enn for meta (9.08) og orto- isomerer (8.48).
4-klorfenol utgjør en eksplosjonsfare ved kontakt med sterke oksidanter , og reagerer farlig med reduksjonsmidler , sterke baser (dannelse av hydrogen ) og hydrider .
Det gir akutt (alvorlig irritasjon og etsende effekter på slimhinner og hud, risiko for alvorlig skade på øyne og luftveier, forstyrrelser i sentralnervesystemet) eller kronisk (irritasjon i øynene, luftveiene og huden). De viktigste eksponeringskildene er luftveiene og ved hudkontakt. Klorfenoler absorberes spesielt lett når de er tilstede i en ikke-ionisert form, men profesjonell håndteringserfaring indikerer at hudkontakt, selv med klorfenolsalter, kan være en viktig absorpsjonsvei.
Syntese
Klorering av fenol
På grunn av den orto-para-orienterende effekten av hydroksylgruppen , kan 4-klorfenol oppnås direkte ved klorering av fenol . Klorering av smeltet fenol med klor gir en blanding av orto- og para- forbindelser i et forhold på ca. 35/65, som neppe er avhengig av temperaturen. Forholdet mellom de to isomerer avhenger fremfor alt av kloreringsreagenset og reaksjonsmediet. Et polært løsningsmiddel slik som acetonitril eller nitrobenzen vil fremme produksjonen av 4-klorfenol, og det samme vil bruken av sulfurylklorid som kloreringsmiddel.
Annen
4-klorfenol kan produseres ved diazotisering av 4-kloranilin i dens saltdiazonium , deretter reaksjon med kobber (I) oksid ( Sandmeyer-reaksjon ) eller en variant av denne reaksjonen fra p - nitrosofenol . Til slutt kan den produseres ved selektiv reduksjon av klorbromfenoler.
bruk
Organiske synteser
4-klorfenol er fremfor alt et mellomprodukt i produksjonen av andre forbindelser, som fargestoffer , medisiner eller fytosanitære produkter.
Blant produktene som det deltar i syntesen, kan vi nevne 2,4-diklorfenol (et annet syntetisk mellomprodukt, biocid), 4-klorfenol-o-kresol ( bakteriedrepende middel ), klorfenizon ( akaricid ), fosacetin ( rodenticid ), diklorofen ( plantevernmiddel ), triadimefon (en) ( soppdrepende middel ), climbazol (en) (topisk antisvamp), difenokonazol (soppdrepende middel), profoksydim (ugressmiddel), 2-benzyl-4-klorfenol ( biocid ) og klofibrat (lipidsenkende medisin).
Det ble tidligere produsert i store mengder som en forløper for hydrokinon . Det brukes også i produksjonen av antrakinonfargestoffer , som kinizarin . Det er en klassisk forløper for sistnevnte, ved reaksjon med ftalsyreanhydrid , etterfulgt av hydrolyse av kloridet.
Andre bruksområder
4-klorfenol er et selektivt løsemiddel i raffinering av mineraloljer. Det brukes også som et biocid i visse husholdnings-, sykehus- eller landbruksdesinfiserende produkter og til og med som jordsterilisator. Det brukes også som et topisk antibakterielt middel i rotkanalterapi og som et topisk antiseptisk middel i noen salver, spesielt innen veterinærmedisin (for katter). Til slutt fungerer det som et denatureringsmiddel for alkohol .
Rest
4-klorfenol er kjent som en rest fra bruk av triadimenol (de) .
Merknader og referanser
- Oppføring "4-Chlorophenol" i den kjemiske databasen GESTIS fra IFA (tysk organ med ansvar for sikkerhet og helse på jobben) ( tysk , engelsk ) , tilgang 17. desember 2020 (JavaScript kreves)
- CRC Handbook of Tables for Organic Compound Identification , Third Edition, 1984, ( ISBN 0-8493-0303-6 ) .
- beregnede molekylmasse fra " atomvekter av elementene 2007 " på www.chem.qmul.ac.uk .
- Muller F et al; Ullmann's Encyclopedia of Industrial Chemistry. 7. utg. (2005). NY, NY: John Wiley & Sons; Klorfenoler. Online utlegningsdato: 15. juni 2000.
- yaws, CL, kjemiske egenskaper Handbook: Fysisk, Termodynamiske, Miljø, Transport, sikkerhet og helse relaterte egenskaper for organiske og uorganiske kjemikalier. McGraw-Hill, New York, NY 1999., s. 142
- yaws, CL, kjemiske egenskaper Handbook: Fysisk, Termodynamiske, Miljø, Transport, sikkerhet og helse relaterte egenskaper for organiske og uorganiske kjemikalier. McGraw-Hill, New York, NY 1999., s. 118
- O'Neil, MJ (red.). Merck-indeksen - En leksikon om kjemikalier, medisiner og biologiske stoffer. Whitehouse Station, NJ: Merck and Co., Inc., 2006., s. 356
- Federation Proceedings, Federation of American Societies for Experimental Biology. Flygning. 2, s. 76, 1943
- HYSAAV. Flygning. 29 (10), s. 37, 1964
- Lewis, RJ Sr. Hawley's Condensed Chemical Dictionary 14. utgave. John Wiley & Sons, Inc. New York, NY 2001., s. 257
- Lide, DR CRC Handbook of Chemistry and Physics 86TH Edition 2005-2006. CRC Press, Taylor & Francis, Boca Raton, FL 2005, s. 3-110
- Lewis, RJ Sax's Dangerous Properties of Industrial Materials. 9. utg. Volum 1-3. New York, NY: Van Nostrand Reinhold, 1996, s. 803
- Ullmann's Encyclopedia of Industrial Chemistry. 6. utg. Vol 1: Forbundsrepublikken Tyskland: Wiley-VCH Verlag GmbH & Co. 2003 til nå, s. V8 387 (2003)
- Ashford, RD Ashfords ordbok for industrielle kjemikalier. London, England: Wavelength Publications Ltd., 1994., s. 208
- Lewis, RJ, Sr (red.). Hawleys kondenserte kjemiske ordbok. 12. utg. New York, NY: Van Nostrand Rheinhold Co., 1993, s. 270
- The Merck Index. 10. utg. Rahway, New Jersey: Merck Co., Inc., 1983., s. 302
- Lewis, RJ Sr.; Hawley's Condensed Chemical Dictionary 14. utgave. John Wiley & Sons, Inc. New York, NY 2001., s. 270
- USEPA; Omgivelseskriterier for vannkvalitet Dok: klorerte fenoler pA-5 (1980) EPA 440 / 5-80-032
- Data Bank for farlige stoffer (HSDB)
- (en) Schollee, Jennifer; Schymanski, Emma; Stravs, Michael; Gulde, Rebekka; Thomaidis, Nikolaos; Hollender, Juliane, foreldre-transformasjonsproduktpar fra Eawag ( DOI 10.1007 / s13361-017-1797-6 )
- Desmurs JR et al; Kirk-Othmer Encyclopedia of Chemical Technology. (2005). NY, NY: John Wiley & Sons; Klorfenoler. Online utlegningsdato: 4. desember 2000.
- Ullmann's Encyclopedia of Industrial Chemistry , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a07_001.pub2 )
- LA Bigelow og HH Reynolds , " Quinizarin ", Org. Synth. , vol. 6,1926, s. 78 ( DOI 10.15227 / orgsyn.006.0078 )
- Ullmann's Encyclopedia of Industrial Chemistry , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a02_355 )
- Rossoff, IS Handbook of Veterinary Drugs. New York: Springer Publishing Company, 1974., s. 106
- (in) "klorfenol" på DrugBank
- Budavari, S. (red.). Merck-indeksen - En leksikon om kjemikalier, medisiner og biologiske stoffer. Whitehouse Station, NJ: Merck and Co., Inc., 1996., s. 359
- Sveitsiske plantevernmidler og metabolitter fra Kiefer et al 2019 ( DOI 10.1016 / j.watres.2019.114972 )

