Brystkreft
Brystkreft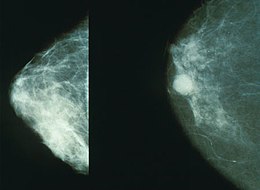 Mammogram som viser brystkreft til høyre.
Mammogram som viser brystkreft til høyre.
| Spesialitet | Onkologi |
|---|
| CISP - 2 | X76 |
|---|---|
| ICD - 10 | C50 |
| CIM - 9 | 174 - 175 , V10.3 |
| OMIM | 114480 |
| Sykdommer DB | 1598 |
| MedlinePlus | 000913 |
| medisin | 1947145, 345979 og 1276001 |
| medisin |
med / 2808 med / 3287 radio / 115 plast / 521 |
| MeSH | D001943 |
| Legemiddel | Etinyløstradiol , fluoksymesteron ( i ) , vinblastin , capecitabin , dexrazoksan , idarubicin , metotreksat , carboplatin , paclitaxel , mitoksantron , vinorelbin , trastuzumab , anastrozol , toremifen ( i ) , letrozol , eksemestan , epirubicin , docetaxel , tamoxifen , dietylstilbestrol , irinotecan , cisplatin , østradiol , cyklofosfamid , klorambucil , metyltestosteron ( i ) , melfalan , sargramostim ( i ) , leuprorelin , fulvestrant ( i ) , doksorubicin , ifosfamid , testolakton ( i ) , fluorouracil , aminoglutetimid ( i ) , megestrol- ( i ) , goserelinacetat ( en ) , nandrolon , neratinib , tamoxifen , vinorelbine og eribulin |
| UK pasient | Brystkreftproff |
Den brystkreft er en ondartet svulst i melkekjertelen . Med andre ord, det er en kreft som starter i de mobile enhetene som har til å skille ut melk, de duktolobulære enhetene i brystet , hovedsakelig hos kvinner . 8 av 10 brystkreft forekommer etter fylte 50 år.
Den første kreften i verden, i 2016 rammer den 1,8 millioner kvinner per år over hele verden, inkludert 50 000 kvinner i Frankrike. En av åtte kvinner forventes å få diagnosen brystkreft i løpet av livet. Behandling av brystkreft har forbedret seg dramatisk gjennom årene, noe som har ført til flere tilfeller av remisjon.
5 til 10% av disse kreftene har arvelig genetisk opprinnelse ; 85 til 90% av tilfellene (såkalt sporadisk eller ikke-arvelig form ) har miljømessig eller ukjent opprinnelse. En betydelig andel av sporadisk brystkreft induseres ved å ta hormoner, østrogen og progesteron som finnes i prevensjonsmidler eller behandlinger mot overgangsalderen. Risikofaktorene er også inntak av alkohol , sukker, meieriprodukter, hydrogenert fett , fedme , mangel på fysisk aktivitet. En sen første graviditet og fravær av amming vil også fremme denne kreften.
Behandlingen vil i følge protokollene kalle til kirurgi, strålebehandling, cellegift, kombinasjonen av disse behandlingene kan suppleres med hormonbehandling.
Epidemiologi
Risikoen øker betydelig med alderen mellom 30 og 60 år; den er da homogen mellom 60 og 80 år; gjennomsnittsalderen for diagnose er 61 år.
Det er visse predisponerende genetiske faktorer, så vel som hormonelle faktorer.
Det skal bemerkes at forekomsten har falt betydelig (med i underkant av 9%) i USA siden 2003 og også i Frankrike, noe som tilsvarer en lavere bruk av hormonerstatningsterapi i overgangsalderen .
I 2002 ble nesten 1,1 millioner nye tilfeller vurdert, med over 400 000 dødsfall fra brystkreft. Forekomsten ser ut til å øke jevnt og trutt med over 1,6 millioner nye tilfeller i 2010 og 425 000 dødsfall. Nesten fire millioner kvinner utvikler brystkreft . Hyppigheten av histologiske undersøkelser somavsluttes i brystkreft, avhenger fremfor alt av intensiteten av screening (se overdiagnose ). Dødeligheten har redusert betydelig siden 1990-tallet i utviklede land. Den fortsetter å vokse i andre land.
Brystkreft i Frankrike
Den Frankrike er blant de landene hvor forekomsten av brystkreft er svært høyt på verdensbasis, og hvor forekomsten av brystkreft har økt raskere (2,4 per 100 000 kvinner per år) i perioden 1980 til 2005, med en dråpe i denne hastigheten mellom 2000 og 2005 (+ 2,1 per 100 000 kvinner per år).
- Brystkreft forårsaket ca 11.000 dødsfall hvert år på 2000-tallet, dødeligheten er stabil (11201 dødsfall i 2005).
- En av åtte kvinner er rammet av brystkreft i Frankrike.
- Det representerer mer enn en av tre nye krefttilfeller (36,7% i 2008) av alle nye kreftformer, hos kvinner.
- På 2000-tallet ble rundt 50 000 nye brystkreft diagnostisert hvert år.
- I 2005 var dette tallet 49 814, noe som tilsvarer en av de høyeste forekomstene i Europa. Denne satsen økte i Frankrike med 2,4% i gjennomsnitt per år i 25 år (fra 1980 til 2005).
- Mindre enn 10% av brystkreft forekommer før fylte 40 år, 25 prosent forekommer før fylte 50 år, nesten halvparten før fylte 65 år.
- Nesten 10% av kvinnene utvikler brystkreft. 75% av nye tilfeller som ble oppdaget, gjelder kvinner over 50 år, og dette tallet øker stadig: 35 000 i 1995 , 42 000 i 2001 .
Denne kreften er en del av en av de tre kreftformene som overlevelsen har økt for siden overlevelsesraten steg fra 80% til 87% på begynnelsen av 2000-tallet, ifølge en felles rapport fra Institute for Public Health Surveillance, Francim-nettverket. det nasjonale kreftinstituttet og sykehusene i Lyon.
Brystkreft i Øst-Asia
Brystkreft i KinaBlant kvinner i Kina er brystkreft den vanligste og den viktigste årsaken til kreftdød. Brystkreftdødeligheten har økt de siste årene. Data fra det andre og tredje Kina nasjonale retrospektive dødsårsaksundersøkelser anslår at brystkreftdødeligheten økte mellom 1990-1992 og 2004-2005 fra 3,84 per 100 000 til 5,09 per 100 000 innbyggere. I 2008 ble rundt 169 000 nye tilfeller av brystkreft diagnostisert, og det var den vanligste diagnosen kreft hos kinesiske kvinner. Samme år var brystkreftdødeligheten 5,7 per 100 000 innbyggere, noe som resulterte i omtrent 44 900 dødsfall.
Brystkreft i JapanI følge en studie publisert i 2009 er forekomsten av brystkreft historisk mye lavere i Japan enn i vestlige land; mellom 1998-2002 i Osaka er det en hastighet på 32,0 per 100 000 kvinner, som kan sammenlignes med en hastighet på 105,6 per 100 000 kaukasiske kvinner på Hawaii og 107,5 per 100 000 japanske kvinner på Hawaii. Forfatteren bemerker det høyere forbruket av soyamat i Japan enn i vestlige land og dets effekter på brystkreftfrekvensen i landet.
Risikofaktorer
Sporadisk (ikke-familiær) kreft
5 til 10% av diagnosen brystkreft er genetisk disponert brystkreft. Ikke-familiær kreft utgjør de resterende 90 til 95%. En tredjedel av disse, i vestlige land, kunne forhindres av en livsstilsendring.
Mulige mekanismerMange molekyler eller cocktailer av molekyler ser ut til å være i stand til å utløse eller fremme brystkreft; angående mekanismene som er involvert:
- En inhibering av DNA- skade respons systemet kan være involvert i halvparten av brystkreft, spesielt de som er initiert eller tilrettelagt av hormoner som brukes til hormonell behandling av overgangsalderen.
- Et protein ( Akt1 ) er overuttrykt i 50% av sporadiske brystkreft. Det kan derfor disponere for brystkreft og / eller være involvert av andre prosesser (miljømessige og ikke-genetiske). Aktivering av AKT1 resulterer effektivt i inhibering ved sekvestrering av BRCA1- proteinet i cytoplasmaet ; imidlertid, hvis dette proteinet ikke lenger kan trenge gjennom og sirkulere i kjernen, blir ikke DNA reparert lenger (som i fravær av BRCA1-genet i tilfelle mange arvelige kreftformer). AKT1 aktiveres også av hormoner som mistenkes å forårsake brystkreft (kronisk hos kvinner på lang østrogenbasert hormonbehandling). I dette tilfellet kan det ikke-muterte BRCA1-genet forstyrres, noe som resulterer i økt risiko for brystkreft.
- Likeledes et annet protein; “ CK2 proteinkinase ” (et enzym som er viktig for epitelcellens plastisitet ) ser ut til å være involvert i utviklingen av disse kreftformene; endringen av aktiviteten til dette proteinet er ledsaget av en transformasjon av epitelceller til kreftceller (mer mobil og en kilde til metastaser). Dette proteinet ser normalt ut til å forhindre den cellulære mekanismen kalt " Epitel-til-mesenkym overgang " (EMT; evolusjonsprosess av epitelceller til mesenkym tilstand og mobilitet, ledsaget av motstand mot visse kreftmedisiner ). Dette enzymet kombinerer to elementer; en “katalytisk underenhet” (CK2α) og en “regulatorisk underenhet” (CK2β). En dysfunksjon av CK2β-underenheten, slik at EMT ser ut til å være involvert i produksjonen av metastaser for denne typen kreft.
Brystkreft er ofte en hormonavhengig kreft: faktorer som øker østrogennivået er derfor i fare. I utgangspunktet øker risikoen for brystkreft med antall menstruasjonssykluser, enten kunstige ( østrogen-gestagen pille ) eller naturlige.
Hormonerstatningsterapi for overgangsalderen øker risikoen for å utvikle brystkreft betydelig.
Sen overgangsalder og tidlig pubertet virker ved å øke antall menstruasjonssykluser og dermed østrogennivåer. Faktorene for tidlig pubertet er: fedme hos barn , økt forbruk av animalske proteiner (kjøtt, melk ), forbruk av sukkerholdige drikker, eksponering for hormonforstyrrende stoffer .
Ikke-fertilitet eller sen fruktbarhetKvinner som ikke har fått barn, eller som hadde sin første graviditet sent (etter 30 år), har en betydelig økt risiko for å utvikle brystkreft, sammenlignet med de som hadde minst ett barn før 30 år. Det er faktisk syklusene som gikk før den første graviditeten som ble utført til termin, som virker de farligste for brystet. Graviditet beskytter brystet ved å endre brystceller i retning av større differensiering. De differensierte cellene er mindre følsomme for kreftfremkallende stoffer, spesielt hormonelle celler. Graviditet fungerer derfor som en vaksine mot østrogen. Jo tidligere denne første graviditeten oppstår, jo bedre fungerer den.
Forurensende stoffer og andre hormonforstyrrende stofferThe Endocrine Society , i en uttalelse skrevet av internasjonale eksperter, understreker parallellitet mellom økningen i forekomsten av brystkreft i løpet av de siste 50 årene og spredning av hormonforstyrrende , syntetiske kjemikalier med østrogen eller østrogen handling. Kreftfremkallende. Disse utallige produktene (de mest kjente er DES , DDT , bisfenol A og dioksiner ), fra forskjellige kilder ( plantevernmidler , industrielle kjemikalier, plast og myknere , drivstoff og andre kjemikalier som er allestedsnærværende i miljøet), er en stor kilde til bekymring for endokrinologer. . Dermed har jenter som var høyt utsatt i livmoren på 1960-tallet for DDT en firedoblet risiko for brystkreft, ifølge en studie publisert i midten av 2015. Mat spiller en stor rolle.
Endocrine Society utsteder en rekke anbefalinger rettet mot
- øke forståelsen av effekten av hormonforstyrrende stoffer (inkludert gjennom grunnleggende forskning og kliniske studier);
- påkalle forsiktighetsprinsippet ;
- forespråke individuell involvering og lærde samfunn for å gjøre problemet kjent;
- gjøre lovendringer.
Av årsaker som er lite forstått, øker fedme risikoen for brystkreft, og spesielt for rask spredning av denne kreften. Dette har blitt demonstrert in vivo så vel som in vitro ; således, når tumorceller ( murine eller humane) samdyrkes med modne adipocytter, øker sistnevnte den invasive kapasiteten til kreften. Generelt vil fedme doble risikoen for brystkreft.
Fedme, ved å øke mengden fettvev, øker nivået av østrogen i blodet ved å aktivere et enzym som kalles aromatase . Dette omdanner faktisk hormoner av androgen- typen til østrogen . Dette fortsetter etter overgangsalderen ; En studie viste økt risiko for brystkreft hos kvinner etter menopausen basert på vektøkning.
Adipocytter dyrket med kreftceller viser en modifisert fenotype når det gjelder avfetting, og en reduksjon i markører for adipocytter assosiert med unormal aktivering preget av overekspresjon av proteaser , spesielt metalloproteinase -11, og proinflammatoriske cytokiner ( interleukin-6 (IL-6 ) eller IL-1β.
Omvendt modifiserer brystkreft tumorceller brystets fettceller ( adipocytter ). Sistnevnte utskiller spesielt pro- inflammatoriske faktorer, inkludert interleukin 6 (som in vitro er tilstrekkelig til at det alene får kreftceller til å metastasere ). Dette kan forklare hvorfor fedme øker risikoen for metastase og rask spredning av denne kreften. Det gjenstår å forstå determinantene for dialogene mellom kreftceller og adipocytter, og større svulster og / eller involverende medvirkende lymfeknuter viser høyere nivåer av IL-6. i omkringliggende svulst t adipocytter.
Peritumoral adipocytter utviser en modifisert fenotype og biologiske karakteristika spesifikk nok til å bli kalt kreft -associated adipocytter (eller CAA for cancerassosierte adipocytter ).
Forbruket av animalsk fett så vel som det av transfettsyrer (som inngår i sammensetningen av mange preparater i næringsmiddelindustrien) har vist seg å være risikofaktorer. Dette forholdet mellom nivået av inntatt animalsk fett og brystkreft har lenge vært kjent. Påvirkningen av flerumettede lipider er mindre åpenbar
En studie (Inserm-Gustave-Roussy, 1995-1998) har vist at risikoen for brystkreft øker med nesten 50% hos kvinner med høyt blodnivå av transfettsyrer , produkter som kan være tilstede i bearbeidede matvarer som industrielle brød og kaker, bakverk, kaker, chips, pizzadeig.
MeieriprodukterFlere vitenskapelige studier beholder melk som en risikofaktor for hormonavhengige kreftformer som prostata, eggstokkene og brystene. Den økte risikoen vil være knyttet til økningen i nivået av IGF-1 i blodet, i seg selv sterkt korrelert med forbruket av melk. Koblingen ser dermed ut til å være etablert i pre-menopausefasen og virker også i samsvar med fraværet av kreft observert i befolkningen som er rammet av Laron syndrom , som ikke produserer IGF-1 . IGF-1- konsentrasjonen varierer sterkt avhengig av type melk (ku, geit, sau, etc.), hvis den er lett, eller avlsmetoden for drøvtyggere ( bovint somatotropin ). Imidlertid etablerer andre studier heller en beskyttende rolle knyttet til innholdet av melk i vitamin D og / eller kalsium.
Alkohol- og tobakkforbrukDen økte risikoen og hyppigheten av brystkreft er i det minste delvis knyttet til økningen i kvinnelig alkoholforbruk ;
- Tallrike studier har vist at inntak av alkohol (uansett hva det er; vin , øl eller brennevin ) øker risikoen for brystkreft. Denne risikoen økes i gjennomsnitt med 30% for tre glass alkohol per dag. Metaanalyser har bekreftet alkoholens rolle i oppstarten eller tilrettelegging av brystkreft. En studie fant at denne risikoen var overvurdert, men den ble tilbakevist ved en metaanalyse basert på 98 saksstyring og potensielle studier.
- Risikoen øker med rundt 10% per 10 g ekstra alkohol som forbrukes i gjennomsnitt per dag med forskjellige genetiske følsomheter, avhengig av individet. Noen underpopulasjoner som er utsatt for andre kreftfremkallende risikofaktorer, kan også være mer følsomme for det. Denne risikoen forverres av andre faktorer: å være over 50, være i postmenopausal fase, bli påvirket av en godartet brystsykdom, en svulst som involverer østrogenreseptorer og / eller avanserte / invasive svulster.
- Denne risikoen dobles med kronisk alkoholforbruk (hos kvinner med normal kroppsmasseindeks (BMI <25), mens fedme er en annen faktor som ofte blir sitert).
- Konsekvensene av alkohol som kreftfremkallende faktor eller kofaktor på brystet kan være ganske raske, fordi statistikk viser at virkningen av nylig forbruk er mer signifikant enn for gammelt forbruk.
Det er en sammenheng mellom røyking og forekomsten av denne kreften.
Mangel på vitamin DDen vitamin D og dets farmasøytisk analoger har anti-proliferative og pro-differensieringseffekter. Det er derfor viktig for forebygging og behandling av kreft generelt. Spesielt kan det begrense en overdreven produksjon av østrogen ved å virke på aromatase .
Brystkreft er ofte assosiert med lave nivåer av vitamin D (mangel eller mangel i 78% av tilfellene ifølge en studie på 145 pasienter). En overdreven dødelighet fra kreft (inkludert brystkreft) hos afroamerikanere tilskrives hudpigmenteringen, som blokkerer mer ultrafiolette stråler enn nødvendig på disse breddegradene og hindrer vitamin D-produksjonen betydelig. En fransk studie av utviklingen over nesten 10 000 kvinner over 10 år bekreftet viktigheten av sammenhengen mellom vitamin D-mangel og utbruddet av brystkreft. Analyse av UV- eksponeringsindeksen hos disse kvinnene viste at bare de som var mest eksponert for UV oppnådde tilstrekkelig beskyttelse mot brystkreft for at matinntak kunne ha en målbar innvirkning; For alle de andre konkluderer INSERM-teamet med at jo lenger nord du bor, jo vanskeligere er det å nå denne vitamin D-terskelen, som beskytter mot brystkreft.
Det er et vagt begrep for enhver sykdom i brystet. Det er vanligvis reservert for godartede abnormiteter som kan føre til forvirring med en svulst, og for dette rettferdiggjør en prøve ( biopsi ) for å identifisere dem nøyaktig. Noen kan fremme påfølgende kreft og garantere regelmessig overvåking.
Et tett utseende på mammografiet, spesielt hvis det er omfattende, vil øke risikoen for å utvikle brystkreft betydelig.
AnnenHistorisk hadde det blitt funnet hos kvinner som hadde gjennomgått mange fluoroskopier da lungetuberkulose var veldig vanlig. Denne risikoen hadde også blitt oppdaget hos japanske kvinner som var blitt bestrålt ved ikke-dødelige doser under atomeksplosjoner i Hiroshima eller Nagasaki . Dette er i hovedsak begynnelsen av XXI th århundre tilfeller av strålebehandling av brystkassen ved behandling av visse kreftformer - Hodgkins sykdom i særdeleshet - hos unge kvinner som risikoen for brystkreft øker betydelig. Visse nye modaliteter for radiologiske undersøkelser, som koronar CT-skanning , kan føre til nok bestråling til å øke risikoen for brystkreft flere tiår etter at undersøkelsen er utført.
Den nattarbeid kan øke risikoen for brystkreft. Denne risikoen er lovlig anerkjent i Danmark og er gjenstand for økonomisk kompensasjon.
Amming fungerer som en beskytter mot brystkreft, spesielt ved å sovne eggstokkene og redusere antall sykluser.
Avslutning av graviditet øker ikke risikoen for brystkreft
I rike land (det har ikke vært studier på dette punktet andre steder), er en høyde over gjennomsnittet ved fødselen korrelert med en fremtidig risiko for å utvikle brystkreft. Fostereksponering for visse hormoner involvert i vekst kan være involvert (bekreftes). 5% av brystkreft hos kvinner født i utviklede land er direkte berørt.
Hos menn1% av brystkreft er utviklet av en mann. På samme stadium er prognosen identisk. Likevel er brystkjertelen hos menn veldig liten, diagnosen er ofte sen, så det er mange flere kreftformer oppdaget på et avansert stadium, ledsaget av hudinvolvering eller dype plan (T4). Risikoen for å få brystkreft øker hos menn med familiehistorie av brystkreft, spesielt når det er en mutasjon i BRCA1- og BRCA2-genene.
Familiekreft
5 til 10% av diagnosen brystkreft er brystkreft med genetisk disposisjon, dvs. mellom 2000 og 4000 mennesker som rammes hvert år, 550 til 1000 dødsfall, i Frankrike. I 2008 var ti gener assosiert med økt risiko for brystkreft. Ni er knyttet til DNA-skadesresponssystemet. Den tiende koder for et protein som hemmer virkningen av AKT1-enzymet (et enzym hvis hemming også spiller en rolle i ikke-genetisk kreft). To av disse ti genene (kalt BRCA1 og BRCA2) er alene ansvarlige for halvparten av disse genetisk disponerte kreftformene, eller 2,5 til 5% av alle brystkreftene.
KjennetegnOfte vises denne typen brystkreft hos en kvinne uten noe særlig helseproblem. Svært sjelden er kvinnen bærer av en kjent genetisk sykdom.
Flere tegn kan tyde på brystkreft med genetisk disposisjon :
- Ung alder (gjennomsnitt på 43 år i stedet for 60 år i ikke-overførbare former);
- Familiehistorie av brystkreft;
- Kreft som forekommer i begge brystene suksessivt eller samtidig;
- Utseende av en ny kreft i eggstokken ;
- Medullær histologisk type kreft.
Det er av den autosomal dominerende typen . Hos en kvinne utsetter tilstedeværelsen av en enkelt mutasjon av genet en 80% risiko for å utvikle brystkreft (i stedet for 10% i fravær av en mutasjon).
Risikoen som kvinner kjører fra en familie der det er unormalt gen, avhenger av om de har arvet det eller ikke. Hvis det arvelige genet ikke er unormalt, er risikoen den samme som for andre kvinner; hvis genet er mutert, vil de ha 70% til 80% sjanse for å få brystkreft. Problemet er likt for risikoen for eggstokkreft eller tykktarmskreft . I noen familier kan disse kreftformene observeres i direkte linje (bestemor, mor, datter) eller i nære slektninger (tante, søster, søskenbarn). Disse kreftformene oppstår vanligvis i den første delen av livet.
En genetisk test kan markere denne risikoen, men en test for et mutert gen er bare sikker på om den er positiv (i dette tilfellet bør alle pårørende følges opp). Denne veldig spesialiserte handlingen bør bare etterspørres for familier hvis hustruer sannsynligvis vil utgjøre en arvelig risiko, demonstrert av en onkogenetisk konsultasjon som vil etablere slektsgren for denne familien.
Gener involvertflere gener er identifisert, men de to viktigste er:
- BRCA1 på kromosom 17 . Mer enn 500 mutasjoner eller sekvensvariasjoner er allerede beskrevet.
- BRCA2 på kromosom 13 . Mer enn 100 forskjellige mutasjoner er telt.
Bare en del av alle disse mutasjonene øker risikofaktoren for kreft. De mutasjoner i BRCA2 (1 i 1460) er funnet oftere enn mutasjoner i BRCA1 (1 i 1960). Disse mutasjonene forårsaker, i tillegg til overflødig risiko for brystkreft, et overskudd av risiko for eggstokkreft.
Sannsynligheten for å utvikle brystkreft i en bærer av en BRCA1- mutasjon er omtrent 65% før fylte 70 år (45% for bærere av en BRCA2-mutasjon ).
Utviklingen av kreft som bærer BRCA1- mutasjoner er fortsatt dårlig forstått: forverring ifølge noen, for andre, lignende alvorlighetsgrad for bærere av BRCA2-mutasjoner eller ikke-bærere av mutasjoner.
Forekomsten av disse mutasjonene er fortsatt lav hos pasienter med brystkreft (mindre enn 4% for BRCA1 , selv om det er dobbelt så høyt i Ashkenazi-jøder).
De andre berørte genene er PALB2 som er involvert i stabiliseringen av BRCA2 , ATM , CHEK2 , RAD51C , BARD1 eller TP53 .
Genetisk rådgivningI noen land kan enhver kvinne som ønsker det, dra nytte av genetisk rådgivning for å bestemme risikoen for arvelig kreft. Hvis sannsynligheten for genetisk predisposisjon er større enn 25%, blir disse pasientene tilbudt en molekylær diagnose. Denne molekylære forskningen er spesielt prediktiv hvis vi kjenner mutasjonen hos en forelder som allerede lider av brystkreft med genetisk disposisjon.
Overvåking av høyrisikokvinnerKvinner med risiko for genetisk predisposisjon eller bærer en mutasjon overvåkes av kliniske overvåkingsteam hver sjette måned fra fylte 20 år og årlig mammografi fra fylte 30 år . Blant de risikoøkende faktorene er eksistensen av duktalt karsinom in situ , ansett som en pre-kreftform, og lobulært karsinom in situ , som er mildere, men kan utvikle seg til kreft i 20 til 30% av identifiserte tilfeller.
Screening
Det er mulig å oppdage og behandle svulster når de er veldig små (mindre enn en centimeter i diameter) takket være mammografi og regelmessig overvåking. Dette reduserer risikoen for dødelighet , og tillater behandlinger som er mindre tunge og mindre traumatiske enn cellegift , "lemlestende" kirurgi (ablasjon). Det er mellom 50 og 74 år at kvinner er mest utsatt for denne typen kreft. Et mammogram hvert annet år tillater effektiv screening, men som utsetter en risiko for overdiagnose som tilsvarer en falsk positiv : kvinnen anses å ha brystkreft når hun ikke er, og utsetter den dermed for en uberettiget behandling med alle bivirkningene og risikoen som følger. Fordelen med denne screeningen må derfor dokumenteres nøye. I følge en metaanalyse fra 2003 kan det i noen tilfeller påvises en signifikant reduksjon i screening mortalitet; den samme metaanalysen rapporterer imidlertid to andre konkurrerende studier som ikke viser noen signifikant reduksjon. Denne eksistensen av risikoreduksjon blir imidlertid kritisert.
I Frankrike sender en avdelings- eller interdepartemental ledelsesstruktur alle kvinner i alderen 50 til 75 år en invitasjon til gratis mammografi (100% økonomisk støtte fra sosialforsikringen) hvert annet år. Invitasjonen kan sendes på forespørsel fra allmennlegen , gynekologen eller kvinnen selv. Besøket må gjøres til en akkreditert radiolog, medlem av nettverket som spesialiserer seg på screening satt opp på avdelingsnivå. Denne strategien er spesielt basert på en ekspertrapport utarbeidet i 2001-2 av Technology Assessment Department of the National Agency for Healthcare Assessment and Accreditation. Det uttalte målet for denne rapporten inkluderte en påminnelse om de franske gjeldende anbefalingene. Rapporten konkluderte med at siden ineffektiviteten av screening mammografi ikke var bevist, skulle anbefalingene som ble brukt for screening av brystkreft opprettholdes.
En ultralyd assosiert med mammografi kan oppdage et større antall kreft, men er assosiert med et større antall falske positive (biopsi som gjør diagnosen kreft ugyldig). Plassen til denne undersøkelsen i screeningstrategien gjenstår derfor å bli evaluert.
Den magnetisk resonansavbildning (MRI) ville også være en lovende test med høyere sensitivitet enn mammografi.
Selv - undersøkelse var en veldig populær screening teknikk i 1980 og 1990, som fortsatt ble anbefalt, men har ikke vist seg å være effektive.
Bruken av infrarød termografi , for påvisning, er en undersøkelse med mindre bivirkning (ingen stråling), med bedre følsomhet , færre falske positive og tidligere påvisning enn mammografi. Kostnadene for termografi vil også være betydelig lavere enn for screening ved mammografi, hvis årlige budsjett er 250 millioner euro. Imidlertid ble termografi knapt brukt i Frankrike i 2017. Teknikken viste sin enkelhet gjennom en nyhetssak.
Utover 75 år har ikke fordelen med systematisk screening blitt demonstrert. Han ser ut til å være svak mellom 70 og 75 år. Før 50 år er interessen tvilsom, uten påvist reduksjon i dødeligheten.
Overdiagnose
Før overgangsalderen har systematisk screening ikke vist seg å være effektiv fordi minimale mistenkelige abnormiteter er vanlige. Ulempene i dette tilfellet ser ut til å oppveie fordelene, bortsett fra kvinner i fare.
Risikoen for systematisk screening er å stille en feil diagnose og føre til uberettiget behandling, med en kostnad og en risiko som et resultat. Dette kalles overdiagnose . Ved brystkreft kan mammografi føre til en betydelig overdiagnose. Denne andelen kan variere fra en av ti til en av fire, eller til og med en av to. Forholdet mellom antall reddet liv og antall kvinner med overdiagnose (delvis gjenspeiler det som kalles nytte / risiko-forholdet ved en undersøkelse) kan variere fra 1 til 2 til 1 av 10.
Forklaringen på disse overdiagnostikkene er ikke entydig: feiltolkning av dokumenter, kreftformer med veldig langsom utvikling eller til og med spontan regresjon av visse ondartede svulster.
I henhold til avdelingen for kroniske sykdommer ved det franske instituttet for folkehelseovervåking , bør disse analysene i fremtiden gjøre det mulig å gjøre screening enda mer effektiv med sikte på å identifisere kreft som vil utvikle seg fra de som vil forbli latente, uten å stille spørsmål. fordelen med selve screeningen.
Tette bryster
For tette eller ekstremt tette bryster kan et mammogram være ineffektivt i å kunne oppdage kreft. Studier har målt at mammografi ikke finner kreft i nesten en tredjedel til halvparten av kvinnene med tette bryster .
Tett brystvev forstyrrer evnen til å finne kreft med et mammogram. Fungerer som en sky, det tette brystvevet er hvitt og kan maskere kreft som også ser ut som hvit.
Brysttetthet kan måles med BI-RADS ved hjelp av et 1-4 poengsystem. Dette systemet lar radiologer måle og beskrive tettheten til brystene
BI-RADS 1: Tett brystvev <25% BI-RADS 2: Tett brystvev mellom 26 og 50% BI-RADS 3: Tett brystvev mellom 51 og 75% BI-RADS 4: Tett brystvev> 75%
Nesten halvparten av kvinnene i USA har tette bryster. I noen stater har radiologer en lovlig forpliktelse til å gi kvinner brysttettheten slik at de kan ha en informert samtale med helseteamet om hvilke tilleggstester de måtte trenge.
Fem fakta om tett vev i brystet:
. 40% av kvinnene har tette bryster. . brysttetthet er en av de mest pålitelige prediktorer for mammografi ineffektivitet ved å oppdage eksisterende kreft. . mammografi oppdager ikke en eksisterende kreft i en tredjedel til halvparten av tilfellene ifølge studiene, for tette bryster. . Brysttetthet er en veletablert prediktor for brystkreftrisiko. . høy brysttetthet er en høyere risikofaktor enn å ha to førstegrads slektninger med brystkreft.
En ultralyd kombinert med et mammogram kan oppdage et større antall kreftformer for tette og hypertette bryster. Ved ultralyd ser noen brystkreft ut som svarte og kan derfor oppdages. En bryst ultralyd er ikke tilstrekkelig alene for screening for brystkreft.
En annen type skanning er MR.
En annen type analyse har utviklet seg i USA for å overvinne ineffektiviteten av mammogrammer for kreftscreening for tette bryster. Breast Molecular Imaging (MBI) er et svært effektivt sekundært diagnostisk verktøy .
Selv med et negativt mammografiresultat for kvinner med tette bryster (eller som anses å ha høy risiko for brystkreft), bør ytterligere MBI-testing vurderes.
Et MBI-bilde representerer en aktiv molekylær funksjonell analyse av vevet på grunn av å ta et radiospor injisert i venene. I disse bildene vises sunt vev, tett eller ikke, i svart og sykt vev vises i hvitt på grunn av raskere absorpsjon av gammastråler som finnes i kontakten til radiosporeren.
Diagnostisk
Klinisk
Palpering av brystet er den første undersøkelsen som utføres. På grunn av deres anatomiske beliggenhet er brystene lette å føle, spesielt når de er av middels eller liten størrelse. Det anbefales at pasienter utfører denne testen selv rutinemessig ved slutten av menstruasjonen.
Under palpasjon mistenkes det fra oppdagelsen av en knute , som kan oppdages ved palpering fra ca. 1 cm i diameter. Uregelmessigheten er kanskje ikke smertefull, men eventuelle nylige avvik bør særlig tiltrekke seg pasienten og legen hennes.
Blant uregelmessigheter pasienten kan se på alene:
- en grop eller en rynke som uthuler overflaten av brystet med et ”appelsinskall” utseende;
- en deformasjon av brystvorten , som trekker den innover;
- et eksemisk utseende av brystvorten som blir rød, crusty eller erodert;
- brystvorteutslipp, spesielt hvis det er blodig eller svartaktig.
Observasjon av et av disse tegnene bør føre til medisinsk konsultasjon veldig raskt. Imidlertid er det bare legen som vil kunne bedømme hvilke ytterligere undersøkelser som er nødvendige, fordi alle disse tegnene ikke bare finnes i tilfelle kreft. En knute kan være godartet:
- når den er solid i konsistens, kan det være et adenofibrom som har utviklet seg i brystkjertelen. Dette kan utvikle seg på grunn av et bestemt bakteriemiljø, som kanskje eller ikke senere blir til adenokarsinom .
- når det er flytende i naturen, kan det være en cyste .
Mammografi
Legen kan bestemme seg for å få sin første diagnose bekreftet med et mammogram . Den ultralyd er en utfyllende eksamen som kan bidra til å lokalisere feilen å lette fjerning eller gjenkjenne om det er en væskefylt cyste, men det kan aldri erstatte mammografi. Mammografi, utført regelmessig og som en del av screeningprogrammer , kan diagnostisere sykdommen på et tilstrekkelig tidlig stadium for at behandlingen skal være så konservativ som mulig og samtidig effektiv. Faktisk, så lenge svulstens størrelse er mindre enn 1-2 cm, er sjansen for utvinning nær 100%.
Bekreftelse av diagnosen
Hvis alle undersøkelsene fremdeles ikke gjør det mulig å sikre en god diagnose, og hvis det er tvil, er det nødvendig å vurdere en prøve som oftest tas av en stor nål (trocar) under lokalbedøvelse uten innleggelse på sykehus. Prøven, eller biopsi , blir ofte utført under en ultralyd- eller røntgenveiledning; vi snakker da om ultralydveiledet biopsi og stereotaksisk biopsi av brystet. Den diagnose av sikkerhet vil bli gjort av den anatomo-patologisk undersøkelse av prøven er tatt.
Vurdering av utvidelse
Søket etter metastaser er grunnleggende i strategien for behandling av brystkreft. Men til tross for de mange studiene som er utført eller den inngående kunnskapen om visse utforskninger, er det foreløpig ingen validert strategi for det systematiske søket etter metastase ved brystkreft.
De fleste av anbefalingene foreslår foreløpig en utvidelse av utvidelsen, inkludert røntgen av brystet, ultralyd i leveren og bein scintigrafi. For svært små svulster kan denne vurderingen være valgfri. På den annen side, for avanserte svulster (inflammatoriske, multifokale svulster, signifikant lymfeknuteinvasjon), er den innledende metastatiske risikoen høy og kan rettferdiggjøre en mer inngående vurdering inkludert en helkropps- tomografi (CT) -skanning og bryst-MR .
Tumorens størrelse, eksistensen av metastatisk lymfadenopati, tilstedeværelsen av en involvering av huden eller brystveggen eller av fjerne metastaser gjør det mulig å etablere en klinisk klassifisering av brystkreft.
| TNM-klassifisering | Beskrivelse |
|---|---|
| Tx | Svulst som ikke kan vurderes på grunn av mangel på informasjon |
| T0 | Ingen bevis for primær svulst |
| Tis | Ductal carcinoma in situ eller lobular carcinoma in situ eller Pagets sykdom i brystvorten uten underliggende svulst |
|
T1 T1a T1b T1c |
Tumor mindre enn 2 cm i største dimensjon - T <0,5 cm - T mellom 0,5 og 1 cm - T mellom 1 og 2 cm |
| T2 | Svulst større enn 2 cm og mindre enn 5 cm i sin største dimensjon |
| T3 | Svulst på mer enn 5 cm i sin største dimensjon |
|
T4 T4a T4b T4c T4d |
Svulst i alle størrelser med utvidelse: - til brystveggen - hudødem eller sårdannelse eller gjennomtrengingsknute - til hud og brystvegg Inflammatorisk kreft |
Ulike typer brystkreft og karsinom
WHO-klassifisering
Den anatomopatologiske studien viser eksistensen av forskjellige typer brystkreft. I følge Verdens helseorganisasjon viser tabellen nedenfor den histologiske klassifiseringen av brystkreft som brukes i alle kreftsentre.
Som med en hvilken som helst epitelial tumor, der er kreft in situ . Det vanligste utvalget av brystkreft er duktaltypen .
| Ikke-infiltrerende epitel-svulster |
| Ductal carcinoma in situ (intracanal) (DCIS) |
| Lobulært karsinom in situ (LCIS) |
| Infiltrerende epitelsvulster |
| Invasivt duktalt karsinom NOS (ingen annen indikasjon) |
| Invasivt duktalt karsinom med dominerende intrakanalkomponent |
| Invasivt lobulært karsinom |
| Slimhinne (kolloid) karsinom |
| Medullært karsinom |
| Papillær karsinom |
| Tubulært karsinom |
| Adenoid cystisk karsinom |
| Ungdomsutskillende karsinom |
| Apokrin karsinom |
| Metaplastisk karsinom av plateepitel |
| Spindelcelletype metaplastisk karsinom |
| Kondroider og metaplastisk karsinom i bein |
| Blandet metaplastisk karsinom |
| Pagets sykdom i brystvorten |
Betennelseskreft
Inflammatorisk brystkreft er en svært sjelden form for brystkreft (1-4%) som utvikler seg raskt over noen få dager eller uker. Den sprer seg raskt gjennom lymfesveien uten å ha tid til å danne en svulst. Blokkering av lymfekar av kreftceller er årsaken til lokal betennelse i brystet av varierende betydning. Diagnosen brystabscess nevnes ofte innledningsvis, spesielt siden bildebehandling (mammografi og ultralyd) ofte er negativ. Enhver utholdenhet av en mer eller mindre smertefull rødhet i brystet krever biopsier, som alene vil bekrefte sykdommen. Behandlingen er først og fremst basert på cellegift, som i den senere tid har gjort det mulig å kurere i mange tilfeller.
Histologisk og molekylær klassifisering
I forbindelse med brystkreftforskning skilles hovedsakelig fire typer brystkreft i henhold til deres morfologi og tilstedeværelsen av tre molekylære markører: den for østrogenreseptoren (ER) og overekspresjonen av reseptoren. Progesteron (PR) og HER2- markør , den siste er en EGFR-reseptor. De resulterende fire klassene er:
- Basal eller trippel negativ: ER- / PR- / HER2-
- HER2-overuttrykk: ER- / PR- / HER2 +
- Luminal A: ER + / PR + / HER2-
- Luminal B: ER + / PR + / HER2 +
Navnet på basale og luminale typer kommer fra likheten mellom svulstene og det tilsvarende normale brystepitelvevet. Generelt har basal og HER2 overuttrykkende kreft dårlig klinisk prognose.
Studier basert på bruk av DNA-sjetonger systematisk i kohorter av pasienter, var også i stand til å isolere forskjellige genuttrykkssignaturer og brystkreft i luminal-typen har en tendens til å uttrykke gener og proteiner GATA3 , KRT19, så de av basaltypen derimot ikke uttrykke disse, men blant annet ETS1 og CD44 .
Behandlinger
Som med alle kreftformer, er det ideelt (fra et medisinsk synspunkt) på kirurgisk fjerning av svulsten, noe som samtidig gjør det mulig å stille diagnosen med sikkerhet. Det neste problemet er å gjøre utvidelsesvurderingen : tilstedeværelse eller ikke av berørte lymfeknuter , tilstedeværelse eller fravær av metastase.
Imidlertid tilsvarer brystlemlestelse generelt psykologisk og sosial lemlestelse for kvinner, og brystene er et av de sterkeste symbolene på kvinnelighet. Noen kvinner kan oppleve denne lemlestelsen som en negasjon av deres kvinnelighet og derfor av deres personlighet.
Det finnes også andre behandlinger som cellegift , strålebehandling og hormonbehandling , som i noen tilfeller kan brukes til å redusere svulsten før operasjonen. Effektiviteten og risikoen ved hver type behandling avhenger av krefttypen, omfanget og stedet.
Terapeutisk strategi
Det finnes mange behandlinger for brystkreft, men de må alltid tilpasses for optimal behandling. Dermed vil genomisk analyse av brystkreft avsløre omtrent femti forskjellige typer brystkreft, hvor hver type eller gruppe vil være utsatt for en bestemt målrettet terapi.
For lokalisert brystkreft har behandling nesten alltid et kurativt mål. Den er basert på de fire terapeutiske våpnene som er kirurgi, cellegift, strålebehandling og hormonbehandling. Kirurgi er et viktig skritt i kur mot brystkreft, med andre behandlinger som vanligvis bare er rettet mot å redusere risikoen for tilbakefall. De vil derfor bli indikert hvis denne risikoen er betydelig, og hvis den antatte fordelen med behandlingen er tilstrekkelig, fordi alle disse behandlingene har bivirkninger. Den forventede fordelen må derfor veies opp mot risikoen for komplikasjoner.
For metastatisk brystkreft: på dette utviklingsstadiet er det svært sjelden å kunne tilby en kurativ behandling. Men moderne behandlinger gjør det ofte mulig å utvide overlevelsen med flere år. Det er umulig å detaljere her de forskjellige mulige terapeutiske strategiene, fordi de avhenger av et veldig stort antall faktorer. Behandling av metastatisk brystkreft begynner med cellegift og hormonbehandling. Kirurgisk eller strålebehandling av de metastatiske stedene kan vurderes enten for et kurativt formål når alle stedene er tilgjengelige for behandling (f.eks: enkelt lever- eller vertebrale metastaser) eller for palliative formål ( f.eks: bestråling av smertefullt metastase).
Det er en rekke genetiske markører som korrelerer med prognosen for brystkreft og kan derfor potensielt lede behandlingen.
Det finnes også molekylære markører for alvorlighetsgrad og prognose for brystkreft. Den metallothionein (MT) er en. De binder seg lett til visse metaller og blir kodet av minst 10 funksjonelle MT-gener som er assosiert med spredning av brystkreftceller, spesielt invasive duktale brystkreftformer. Dette gjør TM til en prognostisk biomarkør for brystkreft som kan påvises ved immunhistokjemi . Jo flere TM er uttrykt i brystkreft, jo mer alvorlig kreft.
Enkelte behandlinger (alkyleringsmidler eller tamoxifen ) kan inhiberes ved overekspresjon av metallotionin (for eksempel hos en pasient som har hatt tungmetallforgiftning)
Kirurgi
SvulstfjerningDet er tre typer brystkirurgi: lumpektomi (fjerning av svulsten), segmentektomi (fjerning av en del av brystet) og mastektomi (fjerning av hele brystet).
I tilfeller der svulsten blir tatt hånd om tidlig nok, er minimal kirurgi (konservativ kirurgi) mulig. Noen ganger må du fjerne hele brystet. Rekonstruktiv kirurgi kan gjøres samtidig eller sekundært.
- Illustrasjon av rekonstruktiv brystkirurgi: gjenoppretting av en del av underlivets muskler ( restus abdominus ) for å rekonstruere brystet, National Cancer Institute .
Denne teknikken består i fjerning av lymfeknuter plassert i armhulen (på nivået av armhulen). Denne operasjonen har mange bivirkninger fordi denne ablasjonen destabiliserer lymfatisk nettverk , noe som kan føre til utseende av lymfødem (stor arm). Det er med sikte på å redusere disse bivirkningene at sentinel node teknikken ble implementert.
Sentinel node teknikkI en svulst er sentinelnoden den første som får lymfatisk drenering.
Den Sentinel node er identifisert ved injeksjon av et fargestoff, hvorvidt eller ikke ledsaget av en radioaktiv kolloid. Det trekkes deretter tilbake for å tillate en anatomopatologisk studie. Hvis den studerte lymfeknuten er sunn, unngår denne teknikken å måtte ty til aksillær disseksjon (fjerning av nesten alle lymfeknuter i regionen), noe som vil føre til betydelige følgevirkninger. Det kan brukes på pasienter med en svulst på mindre enn 3 centimeter, og påvirker opptil 70% av dem.
Denne teknikken er validert, med en feilrate på mindre enn 10%.
Forebygging av postoperativ smerteEn reduksjon i risikoen for kronisk postoperativ smerte kan oppnås ved å utføre lokoregional anestesi på tidspunktet for operasjonen. Tre til tolv måneder etter brystkreftoperasjon kan kronisk postoperativ smerte forhindres hos en av syv personer ( antall personer som skal behandles ). Mens oppmuntrende, er disse resultatene basert på bevis på lavt nivå.
Etter operasjon overvåkingEtter den første behandlingen er det viktig at pasienten overvåkes regelmessig.
Flere undersøkelser er ikke nødvendig, men årlig bilateral mammografi er viktig, spesielt i tilfelle konservativ kirurgi. Avhengig av tilfelle kan det kombineres med andre tilleggsundersøkelser definert i hvert tilfelle.
Selv optimalt behandlet brystkreft kan gjenta seg lokalt eller på avstand ( metastase ). Gjentakelse kan forekomme år etter første behandling, derav viktigheten av å opprettholde overvåking.
Strålebehandling
Det reduserer dødeligheten av denne kreften, men krever en irreproachable teknikk for å redusere bestråling av sunt vev som kan føre til overdreven dødelighet fra kardiovaskulær patologi. Det skilles mellom strålebehandling på brystet og de på lymfeknuteområdene. Ved konservativ kirurgi bør strålebehandling alltid utføres fordi det reduserer risikoen for lokal tilbakefall betydelig. Strålebehandling vil være desto viktigere jo yngre kvinnen er. I tilfelle total brystfjerning er strålebehandling indisert, i visse tilfeller for å redusere risikoen for lokal tilbakefall. Bestrålingen av ganglionkjedene avhenger av plasseringen av svulsten og resultatet av den anatompatologiske undersøkelsen av ganglier.
Langsiktige bivirkningerRisikoen for dødelighet sekundær til strålebehandling sammenlignet med kardiovaskulær dødelighet ser ikke ut til å øke før det tredje tiåret etter behandling, ifølge en studie som overvåker mer enn 500 000 kvinner.
En europeisk studie om risikoen for fosteret i forbindelse med strålebehandling eller cellegiftbehandling for kreftbehandling har vist at fostre hvis mor ble behandlet under graviditet ikke ville ha mer hjertefeil enn ett ueksponert barn.
For å identifisere risikoen for brystfibrose indusert av strålebehandling er det utviklet en test av Inserm for å måle "frekvensen av radioindusert lymfocytisk apoptose (TALRI)". Jo høyere TALRI-nivå, jo lavere er risikoen for brystfibrose.
Cellegift
Den består av administrering av kreftmedisiner med faste intervaller, vanligvis hver 3. uke. Antall adjuverende cellegiftkurs (cellegift utført etter kirurgi) for brystkreft er mellom 4 og 6. Fordelene med adjuvant cellegift fremfor kirurgisk behandling uten cellegift er en betydelig reduksjon i dødelighet og en lavere tilbakefall. I tilfelle aksillær lymfeknute involvering, er ordningen som kombinerer 3 sykluser med cellegift med antracyklin (Farmorubicin °) og cyklofosfamid (Endoxan °) og deretter 3 sykluser med docetaxel (Taxotere °) for tiden referansen. For kreft uten aksillær lymfeknuteinvasjon, gjør søket etter faktorer med dårlig prognose som kan forklare et ugunstig utfall (høy histologisk grad, ingen hormonreseptorer, tumorstørrelse større enn 15 eller til og med 10 mm for noen osv.) Det også mulig for å indikere indikasjonen av 'adjuverende cellegift.
Ved en avansert eller inflammatorisk svulst er det noen ganger nødvendig å starte behandling med cellegift ( neoadjuvant cellegift ) for å redusere tumorstørrelsen og muligens tillate konservativ kirurgi.
Neo-adjuverende cellegift praktiseres også for å begrense størrelsen på eksisjonen: en lumpektomi er noen ganger tilstrekkelig når en mastektomi med adjuverende cellegift først ble planlagt.
I denne sistnevnte indikasjonen, mens den totale dødeligheten, tiden til sykdomsforverring og frekvensen av fjern tilbakefall ikke er forskjellig fra adjuverende cellegift, er lokalregionale tilbakefall hyppigere. Det er for tiden ingen standard neo-adjuverende cellegiftprotokoll.
Ulemper: generell tretthet, kvalme og oppkast, midlertidig hårtap. De varierer i henhold til produktene som brukes, og kontrolleres bedre og bedre.
En rekke produkter har vist seg å være effektive i adjuverende behandling av brystkreft og har en referanseprotokoll, men andre produkter kommer inn på markedet og / eller blir undersøkt.
Målrettede terapier
Den Trastuzumab revolusjonert behandlingen av mange pasienter. Andre legemidler blir evaluert. Disse molekylene er ofte preget av god toleranse, men de er spesielt dyre produkter.
TrastuzumabNoen brystkreftformer overuttrykker Her2- genet betydelig (dette gjelder rundt 25% av brystkreft, ofte med dårlig prognose, siden Her2 - eller CerbB2 - er membranreseptoren som gjør det mulig å aktivere en av banene for økt celleproliferasjon). Kreftceller viser deretter en onkogen avhengighet , og er avhengig av sin overlevelse av funksjonen til signalveien indusert av Her2 . Dette hemmes av trastuzumab (Herceptin °), et monoklonalt antistoff som blokkerer denne reseptoren. Herceptin ble først brukt i en palliativ situasjon. I denne sammenheng gjorde Herceptin det i gjennomsnitt mulig å doble overlevelsestiden til disse pasientene. I tillegg til adjuverende cellegift reduserer Herceptin ° hver 21. dag i 12 måneder risikoen for tilbakefall hos HER2 + pasienter med halvparten og dødelighet med omtrent en tredjedel.
Siden november 2017 har Ontruzant, et biosimilært stoff av trastuzumab , hatt den første markedsføringstillatelsen utstedt av EU-kommisjonen , som tillater distribusjon i EU, så vel som i Norge , Island og Liechtenstein .
BevacizumabI 2007 ble bevacizumab ( Avastin ) brukt ved metastatisk brystkreft (markedsføringstillatelse i Frankrike i 2007, førstelinjemetastatisk). Det er et anti- VEGF monoklonalt antistoff , levert ved infusjon. Den binder selektivt til denne vekstfaktoren og blokkerer dermed neo- angiogenese . Kombinert med paklitaxel , dobler denne behandlingen responstiden (tid til sykdomsprogresjon). På den annen side er det ingen økning i overlevelsestiden.
I Frankrike, i mai 2011 , konkluderte imidlertid Haute Autorité de Santé : "Gitt den lave gevinsten i overlevelse uten gjentakelse og mangelen på forbedring i total overlevelse med kombinasjonen bevacizumab / taxane versus taxane, er fordelen ved å legge bevacizumab til paklitaxel er mindre veletablert i dag. Denne interessen er begrenset til pasienter som er negative for HER2- reseptorer , østrogen og progesteron . " .
LapatinibDen lapatinib ( Tyverb ) som er gitt oral behandling er en intracellulær tyrosinhemmer av kinaseaktiviteten til reseptoren HER2 og HER1 (EGFR). Hos pasienter som overuttrykker HER2, i svulstprogresjon under herceptin og som allerede har fått antracykliner og taxaner, dobler lapatinib- capecitabin- kombinasjonen responstiden sammenlignet med capecitabin alene, uten fordel ved totaloverlevelse. Markedsføringstillatelse ble innhentet i 2008.
Hormonbehandling
I omtrent to tredjedeler av brystkreft har kreftceller overflødig hormonreseptorer. Svulsten sies da å være hormonfølsom fordi østrogen stimulerer kreftproliferasjon gjennom disse reseptorene. Ved brystkreft vil hormonelle behandlinger virke enten ved å redusere nivået av østrogen i blodet og derfor ved å stimulere hormonreseptorer (kastrering, anti-aromataser), eller ved å blokkere hormonreseptorer ( anti-østrogen ).
Ovarial undertrykkelse- kirurgisk, ved laparotomi eller laparoskopi
- stråling, ved å lage 12 til 16 grå i 4 til 8 fraksjoner på et lite bekken, etter å ha identifisert eggstokkens posisjon ved ultralyd;
- Medisinsk, vanligvis ved bruk av agonister LHRH
- Leuprorelin , Enantone LP 3,75 mg / 4 uker
- Goserelin , Zoladex 3,6 mg / 4 uker
- Merk: Decapeptyl har ikke markedsføringstillatelse for brystkreft.
-
Tamoxifen 20 mg d −1
- Mekanisme: delvis østradiolreseptorantagonist
- Forholdsregler: Gjør endometrieundersøkelse 1 / år, sjekk leverfunksjon og triglyserider, må østradiol i plasma og tilsett LHRH hvis økt, effektiv prevensjon (teratogen).
-
Fulvestrant 250 mg IM hver 28. dag
- Mekanisme: østrogenreseptorantagonist uten delvis agonistisk virkning.
Bruk av tamoxifen er gunstig hvis det er østrogenreseptorer i svulsten uavhengig av pasientens alder. Den optimale varigheten av påføring av adjuverende hormonbehandling med tamoxifen er 5 år i en dose på 20 mg d -1 . Bruk av tamoxifen reduserer risikoen for gjentakelse med 8% og risikoen for død med 5%.
Anti-aromataserSiden 2004 kan nye molekyler tilbys kvinner etter menopausen. Dette er aromatasehemmere . De to mest vurderte molekylene er anastrozol og letrozol . Deres toksisitetsprofil er forskjellig fra tamoxifen. Administrasjonen av disse to molekylene gjør det mulig å redusere tilbakefall etter brystkreftoperasjon, uten fordeler når det gjelder total overlevelse ( versus tamoxifen).
-
Letrozole , Femara 2,5 mg d −1
- Mekanisme: ikke-steroide aromatasehemmere
- Forholdsregler: bentetthet, dyslipidemi
-
Anastrozol , Arimidex 1 mg
- Mekanisme: Ikke-steroide aromatasehemmere
- Forholdsregler: bentetthet, dyslipidemi
-
Exemestane , Aromasin 25 mg
- Mekanisme: steroidaromatasehemmer
- Forholdsregler: bentetthet, dyslipidemi
Forebygging: hvordan du kan redusere risikoen
Å vite at brystkreft er en hormonell sykdom, er enhver handling eller behandling som tar sikte på å redusere varigheten og intensiteten av eksponering for østrogen eller for hormonforstyrrende stoffer som etterligner dette østrogenet teoretisk sett antatt å være effektiv.
Handlinger eller hendelser som reduserer risikoen
Flere typer tiltak kan tas for å redusere risikoen for å utvikle brystkreft.
Gynekologiske valgRisikofaktorene har en fellesnevner: økningen i hormonell impregnering av kvinner: direkte, for hormonbehandlinger i overgangsalderen, østrogen-gestagen-pillen, økning i antall menstruasjonssykluser (lavt antall graviditeter eller korte ammingstider), eller indirekte via økningen i aktiviteten til aromataseenzymet i fett, for alkohol, overvekt, mangel på fysisk aktivitet. Dermed kan en primær forebygging av brystkreft foreslås, med en modifisering av livsstilen
Valget av p-pillerDette er for å favorisere piller som ikke inneholder østrogen blokkerende ovarian aktivitet.
En første graviditet i tidlig alderÅ redusere alderen på første graviditet reduserer risikoen for brystkreft fordi syklusene mellom puberteten og den første graviditeten til termin ser ut som de farligste fra dette synspunktet. Den første graviditeten som ble gjennomført til termin, ville fungere som en vaksine mot kreft ved å differensiere vevet og gjøre dem mindre sårbare for hormoner. Graviditet fungerer derfor som en vaksine mot østrogen. Jo tidligere denne første graviditeten oppstår, jo bedre fungerer den.
Langvarig ammingLangvarig amming (fordi å sette eggstokkene i søvn ) reduserer risikoen. I følge WCRF- rapporten gir amming fordeler uavhengig av når kreften utvikler seg (før eller etter overgangsalderen ).
Unngå overgangsalder hormonbehandling (HRT)"Hormonell behandling for overgangsalderen anses nå som en risikofaktor for brystkreft, spesielt når den tas i mer enn 5 år", rapporterte Le Figaro i 2008.
Livsstilsvalg VekttapFedme og overvekt øker risikoen for brystkreft. Professor Pierre Kerbrat (Eugène-Marquis-senteret, Rennes) estimerte i 2008 at kampen mot kvinnelig fedme ville forhindre 13 000 nye tilfeller av brystkreft per år i EU.
Fysisk treningIfølge professor Kerbrat, ville det å praktisere 30 minutters fysisk aktivitet, fem dager i uken, redusere antall nye tilfeller med 30% til 40%. Den beskyttende effekten kommer fra både kampen mot fedme og virkningen av trening på hormonelle sekreter. Amerikanske studier har også vist sin forebyggende effekt mot gjentakelse av sykdommen.
Redusere alkoholforbruketRisikoen for brystkreft øker med alkoholinntak. Moderat alkoholforbruk øker risikoen med 20% til 30%. Mer presist øker risikoen med 10% når det daglige alkoholforbruket øker med 10 g alkohol (dvs. ett glass).
MatvalgDe ville redusere risikoen.
- Gjennomført ved hjelp av spørreskjema fra 334850 kvinner i alderen 35 til 70 år og inkludert i EPIC (European Prospective Investigation in Cancer and Nutrition) kohort (oppfølgingsvarighet: 11,5 år), en studie datertapril 2013viser at det ikke er noen sammenheng mellom inntak av flavonoider og lignan ( fytoøstrogener ) og risikoen for brystkreft uansett om man tar hensyn til menopausal status eller hormonreseptorens status .
Transfettsyrer i blodet øker kvinnens risiko for brystkreft med nesten 50%. De transfettsyrer anvendes i bearbeidede matvarer som brød og industrielle kjeks, kaker, kaker, brød, pizzaer, industriell pasta.
- Den grønn te og / eller soya kan (er) har beskyttende egenskaper (som ville forklare det faktum at i Europa en i 12 kvinner utvikler denne kreftformen, mot en for 80 i Japan hvor disse matvarene er konsumert) .
- Etter begynnelsen av brystkreft ser det ikke ut til å redusere risikoen for gjentakelse ved å doble forbruket av frukt og grønnsaker.
- Omega 3- tilskudd ble testet i 2008 for å se om det forbedret cellegift.
- Ikke å ta hormonelle behandlinger vil redusere risikoen for brystkreft.
- SERM-type behandlinger ( tamoxifen , raloxifene ) vil redusere risikoen. Imidlertid har disse medikamentene signifikante bivirkninger (økning i antall tromboemboliske sykdommer for de to molekylene, endometriecancer for tamoxifen) og deres plass gjenstår å bli bestemt.
"Forebyggende" kirurgiske behandlinger
Forebyggende kirurgiske behandlinger har blitt foreslått hos kvinner med familiehistorie av brystkreft med mutasjon i BRCA1- eller BRCA2-gener. Hos disse kvinnene varierer risikoen for brystkreft mellom 40 og 85% før fylte 80 år. De kirurgiske forslagene er enten fjerning av begge brystene med eller uten bilateral ooforektomi , eller bilateral ooforektomi alene.
Nåværende observasjonsstudier om forebyggende bilateral mastektomi (MBP) viser at det kan redusere forekomsten av brystkreft og / eller død, selv om disse studiene har metodiske begrensninger. Tilfredshet med å følge denne prosedyren ser ut til å være god, med redusert kreftbekymring ledsaget av nedsatt kroppsbilde og seksuelle opplevelser. Hos kvinner som har hatt kreft i det ene brystet, ser det ut til å fjerne det andre brystet å redusere forekomsten av kreft, men effekten på langtidsoverlevelse er usikker på grunn av fortsatt risiko for tilbakefall eller metastase av den opprinnelige kreften.
Psykologiske aspekter
Å finne ut at du har kreft kan være veldig vanskelig å gjøre opp med, siden denne nyheten lenge har blitt ansett som den forestående døden. I tillegg endrer sykehusinnleggelse, kirurgi og adjuverende behandlinger alvorlig liv i pasienten. Det er derfor viktig å gi pasienter passende psykologisk støtte, som vanligvis innebærer deltakelse i pasientgrupper som gjennomgår de samme prøvelsene.
Imidlertid er brystkreft diagnostisert sent ofte lemlestende. For kvinner tilsvarer denne brystlemlestelsen generelt psykologisk og sosial lemlestelse. Brystet er et av de sterkeste symbolene på femininitet , og noen kvinner kan oppleve denne lemlestelsen som en negasjon av deres femininitet og derfor av deres personlighet.
Parforholdet lider ofte av konsekvensene av sykdommen. I perioden etter behandlingen kan pasienten eller hennes partner uttrykke negative følelser, som fortalelse. Denne typen situasjoner bør tas profesjonelt, da det kan være forbundet med psykiske lidelser som depresjon. I følge Nicolas Favez, Sarah Ciro Notari, Tania Antonini og Linda Charvoz, vil denne typen situasjoner sannsynligvis dukke opp i de tidlige stadiene av sykdommen, og selv når den medisinske prognosen er optimistisk. I denne sammenheng kan rekonstruktiv kirurgi tilbys, ledsaget av psykologisk behandling.
Brystkreft er derfor ikke bare et medisinsk problem. Det påvirker livet, kroppen og selvtilliten. Når en kvinne får dommen om "brystkreft", forlater hun legekontoret med frykt i magen, med mange spørsmål om hvordan livet hennes vil bli i fremtiden. Hvordan snakke om dette til slektningene? Hvordan håndtere håravfall og tap av øyenbryn? Hvordan komme seg hjemmefra og møte andres blikk? Hvordan kan du fortsette å ta vare på barna dine? Vil hun fortsatt kunne ha noen? Mister hun jobben? Hva vil skje med forholdet hennes til mannen i livet hennes? Så mange spørsmål, få muligheter for dialog, mange tabuer. Ofte faller kvinner tilbake på sykdommen, og dette er til og med skadelig for terapiens suksess.
Mye gjenstår å gjøre for å kommunisere ordentlig med pasienter og deres familier, men også for å konkret forbedre medisinsk behandling av kvinner og deres livskvalitet generelt.
I populærkulturen
Humoristen Marie Reno støtter bevissthet om brystkreft med sin humoristiske sang Attention to your boobs! .
Merknader og referanser
- https://www.francetvinfo.fr/sante/cancer/cancer-du-sein-il-y-a-une-vraie-recrudescence_1815585.html
- André Cicolella, brystkreft. Avslutter epidemien , red. Les Petits Matins, 2016.
- (i) PM Ravdin, Cronin KA, Howlader N et al. “ Reduksjonen av forekomst av brystkreft i 2003 i USA ” , New Eng J Med , 2007; 356: 1670-1674
- "Reduksjon i forekomsten av brystkreft i 2005 og 2006 i Frankrike: et paradoksalt fenomen" Cancer Bulletin , 2008; 95: 11-5
- (in) Forouzanfar MH, KJ Foreman, Delossantos AM et al. “ Bryst- og livmorhalskreft i 187 land mellom 1980 og 2010: en systematisk analyse ” , Lancet , 2011
- Boyle og Ferley, 2004
- WCRF - Brystkreftstatistikk
- IARC - Faktaark for brystkreft
- Source Inserm 2008, konsultert 2008 10 04
- "Antoine Spire snakker med David Khayat for Le Monde de l'Education" utdrag fra en artikkel publisert i april 2006 i Le Monde de l'Education
- "Avansert brystkreft: løftene om en ny behandling" på futura-sciences.com
- Institutt for folkehelseovervåking (InVS) INSERM
- " Brystkreft: mot mindre intensive behandlinger " (vist på en st oktober 2015 )
- National Cancer Institute, Breast Cancer, oppdatering fra april 2008.
- " Kreft: overlevelse forbedres i Frankrike " , på sante.lefigaro.fr (åpnet 2. februar 2016 )
- Wang B, He M, Wang L, Engelgau MM, Zhao W, Wang L. Screening av brystkreft blant voksne kvinner i Kina, 2010. Prev Chronic Dis 2013; 10: 130136. DOI: https://dx.doi.org/10.5888/pcd10.130136
- (i) Nagata, Chisato, " Factors to consider in the Association Between Soy Isoflavone Intake and Breast Cancer Risk " , J Epidemiol , vol. 20, n o to2009, s. 83-89 ( ISSN 1349-9092 , DOI 10.2188 / jea.JE20090181 , les online )
- Wooster R, Weber BL. Bryst- og eggstokkreft . N Engl J Med 2003; 348: 2339-47
- generelle cancer Course P r JF HERON
- Loibl S, Poortmans P, Morrow M, Denkert C, Curigliano G, Brystkreft , Lancet, 2021; 397: 1750-1769
- Isabelle Plo, Corentin Laulier, Fabienne Lebrun, Laurent Gauthier, Fabien Calvo og Bernard Lopez. AKT1 hemmer homolog rekombinasjon ved å indusere cytoplasmatisk retensjon av BRCA1 og RAD51 . Kreftforskning. 15. november 2008.
- [ hormonelle behandlinger fremme brystkreft? CEA pressemelding]
- Pressemelding / Forskning fra Université Joseph-Fourier (Grenoble) ; [CK2: en viktig rolle i progresjonen av brysttumorer] ; 10. mai 2012
- Clavel-Chapelon F, kumulert antall menstruasjonssykluser og risiko for brystkreft: resultater fra E3N-kohortestudien av franske kvinner , Cancer Causes and Control, 2002; 13: 831-838
- Beral V, brystkreft og hormonerstatningsterapi i millionkvinnestudien, Lancet, 2003; 362: 419-27
- Jenter når puberteten tidligere enn noensinne
- (in) Merrill RM Fugal S Novilla LB, Raphael ™, " Kreftrisiko assosiert med tidlig og sen maternal alder ved første fødsel " , Gynecol Oncol , Vol. 96, n o 3,2005, s. 583-93. ( PMID 15721398 , DOI j.ygyno.2004.11.038 )
- (en) Faupel-Badger JM, Arcaro KF, Balkam JJ, Eliassen AH, Sherman ME et al. , “ Postpartum remodeling, lactation, and breast cancer risk: summary of a National Cancer Institute-sponsed workshop ” , J Natl Cancer Inst , vol. 105, n o 3,2013, s. 166-74. ( PMID 23264680 , PMCID PMC3611853 , DOI 10.1093 / jnci / djs505 , les online [html] )
- (en) Diamanti-Kandarakis E, Bourguignon JP, Giudice LC, et al. , “ Endokrinforstyrrende kjemikalier: en vitenskapelig uttalelse fra Endocrine Society ” , Endocr. Rev. , vol. 30, n o 4,Juni 2009, s. 293–342 ( PMID 19502515 , PMCID 2726844 , DOI 10.1210 / er.2009-0002 )
- Romain Loury (2015) Bak brystkreft, DDT , 16. juni 2015
- "Dr de Lorgeril - Årsakene til brystkreft endelig identifisert Slik beskytter du deg.?"
- Fettceller og brystkreft - en farlig kombinasjon (ifølge en CNRS pressemelding) 2011/04/05
- Brystkreft: det kreves forebyggingskampanjer i Le Figaro , 23. oktober 2008, side 11
- Økt risiko for brystkreft hos kvinner etter overgangsalderen basert på vektøkning
- Béatrice Dirat; Kreftassosierte adipocytter viser en aktivert fenotype og bidrar til brystkreftinvasjon ; Cancer Research, doi: 10.1158 / 0008-5472.CAN-10-3323 Cancer Res 1. april 2011 71; 2455 Sammendrag )
- B. Dirat et al. Kreftforskning , en st april 2011
- Studie som viser sammenhengen mellom brystkreft og inntak av animalsk fett fra 1986
- Studie av identifiserte kreftfaktorer i Spania
- kosten fett inntak og risiko for brystkreft: en case-control studie i Kina
- Konklusjoner fra Inserm og Institut Gustave-Roussy om å evaluere forskjellige fettsyrers rolle for utvikling av brystkreft, fra blodanalyser samlet fra 1995 til 1998 blant 25 000 av 100 000 kvinner fulgt som en del av -kalt E3N- studie .
- (in) Vekstfaktor øker kreftrisikoen
- (in) Melk, melkeprodukter og laktoseinntak og risiko for eggstokkreft: En metaanalyse av epidemiologiske studier , International Journal of Cancer , vol. 118, utgave 2, s. 431-441
- (in) Variasjon i plasma Insulin-lignende vekstfaktor-1 og Insulin-lignende vekstfaktor bindende protein-3: Personlige og livsstilsfaktorer (USA)
- "Andes-rapporten, s76 / 210"
- (in) "Forbruk av rå eller oppvarmet melk fra forskjellige arter: En evaluering av potensielle ernæringsmessige og helsemessige fordeler, p4 / 14
- (in) "Assosiasjon av IGF-1-innhold med helmelk og fettfattig melk i México"
- (i) Inntak av meieriprodukter, kalsium og vitamin D og risikoen for brystkreft
- (i) Meieriprodukter og risiko for brystkreft
- [PDF] Rapport Alkohol og risiko for kreft (60 sider), National Cancer Institute, and Nacre network, 2007)
- Xue F, Willett WC, Rosner BA, Hankinson SE, Michels KB, Sigarettrøyking og forekomsten av brystkreft , Arch Intern Med, 2011; 171: 125-133
- (en) Lundqvist J, M Norlin, Wikvall K, " 1α, 25-dihydroxyvitamin D (3) utøver vevsspesifikke effekter på østrogen androgen metabolisme " , Biochim Biophys Acta ,januar 2011( PMID 21262387 , DOI 10.1016 / j.bbalip.2011.01.004 )
- (en) Napoli N, Vattikuti S, Ma C, et al. , “ Høy forekomst av lavt vitamin D og muskelskjelettplager hos kvinner med brystkreft ” , Breast J , vol. 16, n o 6,2010, s. 609–16 ( PMID 21070438 , DOI 10.1111 / j.1524-4741.2010.01012.x )
- (in) Grant WB, Peiris AN, " Role of Possible serum 25-hydroxyvitamin D in black-white Health Disparities in the United States " , J Am Med Dir Assoc , Vol. 11, n o 9,november 2010, s. 617–28 ( PMID 21029996 , DOI 10.1016 / j.jamda.2010.03.013 )
- (in) Engel P Fagherazzi G, S Mesrine, Boutron-Ruault MC, Clavel-Chapelon F, " Felles effekter av diett vitamin D og soleksponering er brystkreftrisiko: resultater fra den franske E3N-kohorten " , Cancer Epidemiol. Biomarkører Forrige , vol. 20, n o 1,januar 2011, s. 187–98 ( PMID 21127286 , DOI 10.1158 / 1055-9965.EPI-10-1039 )
- (in) Mammografisk tetthet og risikoen for påvisning av brystkreft og Norman F. Boyd, Helen Guo, Lisa J. Martin, Limei Sun, Jennifer Stone, Eve Fishell, Roberta A. Jong, Greg Hislop, Anna Chiarelli, Salomon Minkin, Martin J. Yaffe, New Eng J Med , 2007; 356: 227-236
- (en) Travis LB, Hill D, Dores GM, Gospodarowicz M, van Leeuwen EF, Holowaty E et al. “ Kumulativ absolutt risiko for brystkreft for unge kvinner behandlet for Hodgkin lymfom ” J Natl Cancer Inst . 2005; 97: 1428-37
- (i) Einstein AJ, Henzlova MJ, Rajagopalan S, " Estimating risk of cancer associated with exposure exposure from 64-slice computed tomography coronary angiography " JAMA 2007; 298: 317-323
- (in) Kolstad HA, " Nattskiftarbeid og risiko for brystkreft og andre kreftformer - en kritisk gjennomgang av det epidemiologiske beviset " Scand J Work Around Health . 2008; 34: 5-22
- Kronisk vekslende lette sykluser øker risikoen for brystkreft hos mus
- (no) Wise J, " Danske nattevaktarbeidere med brystkreft etter kompensasjon " BMJ . 2009; 338: b1152
- (in) Stuebe AM, Willett WC, Fei Xue, Michels KB, " Lactation and incidence of premenopausal breast cancer ," Arch Intern Med . 2009; 169 (15): 1364-1371
- "Frivillig avslutning av svangerskapet øker ikke risikoen for brystkreft" (WHO, lagt ut online i juni 2000)
- Silva IdS, Stavola BD, McCormack V, Collaborative Group on Pre-Natal Risk Factors and Subsequent Risk of Breast Cancer (2008), " Birth Size and Breast Cancer Risk: Re-analysis of Individual Participant Data from 32 Studies " ( Arkiv • Wikiwix • Archive.is • Google • Hva skal jeg gjøre? ) (Besøkt 2. august 2017 ) . PLoS Med 5 (9): e193
- Nasjonalt institutt mot kreft, brystkreft hos menn .
- Maalej M, Hentati D, Messai T, Kochbati L, El May A, Mrad K, Romdhane KB, Ben Abdallah M, Zouari B. Brystkreft i Tunisia i 2004: en komparativ klinisk og epidemiologisk studie. Bull Cancer. 2008 feb; 95 (2): E5-9.
- Antoniou A, Pharoah PD, Narod S et als. Gjennomsnittlig risiko for bryst- og eggstokkreft assosiert med BRCA1- eller BRCA2-mutasjoner oppdaget i saksserier som ikke er valgt for familiehistorie: en kombinert analyse av 22 studier , Am J Hum Genet, 2003; 72: 1117-1130
- Robson ME, Chappuis PO, Satagopan J, et al. En kombinert analyse av utfallet etter brystkreft: forskjeller i overlevelse basert på BRCA1 / BRCA2 mutasjonsstatus og administrering av adjuverende behandling , Breast Cancer Res 2004; 6: R8-R17
- Rennert G, Bisland-Naggan S, Barnet-Griness O, et al. Kliniske utfall av brystkreft hos bærere av BRCA1- og BRCA2-mutasjoner , N Engl J Med 2007; 357: 115-123
- John EM, Miron A, Gong G og Als. [2007; 298 (24): 2869-2876 Prevalens av patogene BRCA1-mutasjonsbærere i fem amerikanske rasegrupper / etniske grupper ], JAMA, 2007; 298: 2869-2876
- Antoniou AC, Casadei S, Heikkinen T et al. Brystkreftrisiko i familier med mutasjoner i PALB2 , N Engl J Med, 2014; 371: 497-506
- Brystkreft in situ på nettsiden til foreningen for kreftundersøkelse i Meurthe et Moselle, konsultert 13. januar 2016
- "Brystkreft: illusjonene av screening", Coisne S og Lemarchand F., La Recherche , 395, mars 2006: 44-48
- Humphrey LL, Helfand M, Chan BKS, Woolf SH, screening av brystkreft: En oppsummering av bevisene for den amerikanske arbeidsgruppen for forebyggende tjenester , Ann Intern Med , 2002: 137: 347-360
- Resultatene av to-fylkesforsøket med mammografiscreening er ikke kompatible med samtidig offisiell svensk brystkreftstatistikk . Zahl PH, Peter C. Gøtzsche , Andersen JM, Maehlen J. Dan Med Bull. 2006 nov; 53 (4): 438-40.
- Berg WA, Blume JD, Cormack JB, Kombinert screening med ultralyd og mammografi vs mammografi alene hos kvinner med forhøyet risiko for brystkreft JAMA 2008; 299: 2,151 til 2,163
- Leach MO, Boggis CR, Dixon AK et al. Screening med magnetisk resonansbilder og mammografi av en britisk befolkning med høy familiær risiko for brystkreft: en potensiell multisenter-kohortstudie (MARIBS) , Lancet, 2005; 365: 1769-78
- Kösters JP, Peter C. Gøtzsche , Regelmessig egenundersøkelse eller klinisk undersøkelse for tidlig påvisning av brystkreft , Cochrane Database of Systematic Reviews 2003, utgave 2. Art. Nr.: CD003373. DOI: 10.1002 / 14651858.CD003373
- "Niramai Bruk termisk bildebehandling og AI for å revolusjonere diagnostisering av brystkreft"
- "You tube, Breast termografi"
- "You tube: Mammografi og Thermal Imaging"
- "Ncbi, 2014: En ny modell for smart brystkreftpåvisning i termogrambilder."
- "Mars 2017: Støttende ikke-invasivt verktøy for diagnostisering av brystkreft ved hjelp av et termografisk kamera som sensor"
- "10Systematic Reviews in Pharmacy, Vol 9, Issue 1, Jan-Dec, 2018, The Effect of Thermography on Breast Cancer Detection"
- "2012, Skifer: Brystkreft: en fransk skandale?"
- "Termografi for påvisning av brystkreft"
- "Infrarød avbildning av brystet - en oversikt, s18 / 22"
- [artikkel - [relatert] "France-info, 2019: Britisk turist oppdager brystkreft ... mens hun besøker et museum"]
- Warner E, screening for brystkreft , N Engl J Med, 2011; 365: 1025-1032
- Miller AB, T, Baines CJ, Wall C, The Canadian National Breast Screening Study-1: brystkreft dødelighet etter 11 til 16 års oppfølging: en randomisert screeningprøveversjon av mammografi hos kvinner alderen 40 til 49 år , Ann Intern Med, 2002; 137: 305-312
- Moss SM, Cuckle H, Evans A, Johns L, Waller M, Bobrow L, Effekt av mammografiscreening fra fylte 40 år på brystkreft dødelighet på 10 års oppfølging: en randomisert kontrollert studie , Lancet 2006; 368: 2053-2060
- Zackrisson S, Andersson I, Janzon L, Manjer J, Garne JP, Overdiagnose av brystkreft 15 år etter avslutningen av mammografisk screeningstudie i Malmö: oppfølgingsstudie , BMJ, 2006; 332: 689-92
- Welch HG, Schwartz LM, Woloshin S, Begrensninger av screening for brystkreft: 1 av 4 kreftformer oppdaget ved mammografi er pseudokreft , BMJ, 2006; 332: 727
- Jørgensen KJ, Peter C. Gøtzsche , Overdiagnostikk i offentlig organiserte mammografiscreeningprogrammer: systematisk gjennomgang av forekomst trender , BMJ 2009; 339: b2587
- Zahl PH, Mæhlen J, Welch HG, Den naturlige utviklingen av invasiv brystkreft påviselig ved sortering mammografi , Arch Intern Med 2008; 168: 2311-6
- [1] .
- "En mangel på Methylobacterium-bakterier i kreft i brystvevet"
- "EverZen: Hva er overlevelsesraten for brystkreft?"
- fra Cabarrot E. Naturhistorie av brystkreft. Medikokirurgisk leksikon . Vitenskapelige og medisinske utgaver Elsevier SAS, Paris. Gynekologi, 865-A-10, 2000.
- Inflammatorisk brystkreft: spørsmål og svar på nettstedet til National Cancer Institute .
- (in) X. Dai , " Brystkreft iboende subtypeklassifisering, klinisk bruk og fremtidige trender " , Am J Cancer Res , vol. 5, n o 1015. september 2015, s. 2929–2943 ( les online ).
- (in) E. Charaffe-Jauffret , " Gene Expression profilering av brystcellelinjer identifiserte potensielle nye basale markører " , Oncogene , vol. 25,6. april 2006, s. 2273–2284 ( les online ).
- "Genomikkrevolusjonen" , 1 min 33 s / 3 min
- "Målrettet terapi 3m39 / 5m33"
- van 't Veer LJ, Dai H, van de Vijver MJ og Als. Genuttrykksprofilering forutsier klinisk utfall av brystkreft , Nature, 2002; 415: 530-536
- Paik S, Shak S, Tang G og Als. En multigen-analyse for å forutsi tilbakefall av tamoxifen-behandlet, node-negativ brystkreft , N Engl J Med, 2004; 351: 2817-2826
- Wang Y, Klijn JG, Zhang Y og Als. Genuttrykkingsprofiler for å forutsi fjernmetastase av lymfeknute-negativ primær brystkreft , Lancet, 2005; 365: 671-679
- Betydning MA, Somji S, Lamm DL, Garrett SH, Slovinsky F, Todd JH, Betydning DA. Overuttrykk av metallotionin isoform 3 er assosiert med brystkreft som har dårlig prognose . Am J Pathol 159: 21–26, 2001.
- Nartey N, Cherian MG, Banerjee D. Immunohistokjemisk lokalisering av metallothionein i humane thyreoideatumorer . Am J Pathol 129: 177–182, 1987.
- Haerslev T, Jacobsen K, Nedergaard L, Zedeler K. Immunhistokjemisk påvisning av metallotionin i primære brystkarsinomer og deres aksillære lymfeknute-metastaser. Pathol Res Pract 190: 675–681, 1994. 64.
- Haerslev T, Jacobsen K, Zedeler K. prognostisk betydning for immunhistokjemisk detekterbar metallothionein i primær brystkarsinoma. APMIS 103: 279–285, 1995.
- Fresno M, Wu W, Rodriguez JM, Nadji M. Lokalisering av metallothionein i brystkarsinomer. En immunhistokjemisk studie. Virchows Arch A Pathol Anat Histopathol 423: 215–219, 1993.
- 5. INTERNASJONALE KONFERANSE OM METALLOTHIONEIN SYMPOSIUMPAPIRER Metallothionein som en prognostisk biomarkør i brystkreft Boon-Huat Bay, Rongxian Jin, Jingxiang Huang og Puay-Hoon Tan ( “ Sammendrag ” ( Arkiv • Wikiwix • Archive.is • Google • Hva skal jeg gjøre? ) (åpnet 2. august 2017 ) og “full PDF-artikkel (6 sider) ” ( Arkiv • Wikiwix • Archive.is • Google • Hva skal jeg gjøre? ) (åpnet 2. august 2017 ) )
- Ioachim E, Tsanou E, Briasoulis E, Batsis Ch, Karavasilis V, Charchanti A, Pavlidis N, Agnantis NJ. Klinisk patologisk studie av uttrykk for hsp27, pS2, cathepsin D og metallothionein i primær invasiv brystkreft . Bryst 12: 111–119, 2003.
- Surowiak P, Matkowski R, Materna V, Gyorffy B, Wojna A, Pudelko M, Dziegiel P, Kornafel J, Zabel M. Forhøyet metallothionein (MT) uttrykk i invasiv duktal brystkreft forutsier tamoksifenresistens . Histol Histopathol 20: 1037–1044, 2005.
- [PDF] Nettstedet av National Organization of Liberal Sykepleiere Fagforeninger
- Mansel RE, Fallowfield L, Kissin M et als. Randomisert multisenterforsøk med sentinel node biopsi versus standard aksillær behandling ved opererbar brystkreft: ALMANAC-studien , J. Natl Cancer Inst. , 2006; 98: 599-609
- Erica J Weinstein , Jacob L Levene , Marc S Cohen og Doerthe A Andreae , “ Lokalbedøvelse og regional anestesi versus konvensjonell analgesi for å forhindre vedvarende postoperativ smerte hos voksne og barn ”, Cochrane Database of Systematic Reviews ,21. juni 2018( ISSN 1465-1858 , PMID 29926477 , PMCID PMC6377212 , DOI 10.1002 / 14651858.cd007105.pub4 , lest online , åpnet 21. juli 2020 )
- (en) Clarke M, Collins R, S Darby et al. "Effekter av strålebehandling og av forskjeller i omfanget av kirurgi for tidlig brystkreft på lokal tilbakefall og 15-års overlevelse: en oversikt over randomiserte studier" Lancet 2005; 366: 2087-106
- (en) Henson KE, McGale P, Taylor C, Darby SC. “Strålingsrelatert dødelighet fra hjertesykdom og lungekreft mer enn 20 år etter strålebehandling for brystkreft” British Journal of Cancer 20. desember 2012 DOI : 10.1038 / bjc.2012.575
- " Kreft kan bli behandlet i løpet av svangerskapet " (tilgjengelig 02.10.2015 )
- " Brystkreft: en blodprøve for å forutsi virkningen av strålebehandling " , på Santé Magazine (åpnet 27. januar 2016 )
- (en) Romond EH, Perez EA, Bryant J et al. “Trastuzumab pluss adjuverende cellegift for opererbar HER2-positiv brystkreft” N Engl J Med. 2005; 353: 1673-84
- " Medscape France - Medisinsk informasjon og ressurser for leger | Medscape France ” , på francais.medscape.com (åpnet 4. september 2018 )
- (no-NO) John Wiley & Sons Ltd og The Atrium, Southern Gate , “ Ontruzant lanserer for å bli første Herceptin biosimilar tilgjengelig i Storbritannia | Pharmafile ” , på www.pharmafile.com (åpnet 4. september 2018 )
- (en) Miller K, Wang M, Gralow J et al. “Paclitaxel pluss bevacizumab versus paklitaxel alene for metastatisk brystkreft” N Engl J Med. 2007; 357: 2666-76.
- Sammendrag av uttalelsen fra Haute Autorité de Santé (Frankrike), mai 2011
- (en) Geyer et al. “Lapatinib pluss capecitabin for HER2-positiv avansert brystkreft” ( Arkiv • Wikiwix • Archive.is • Google • Hva skal jeg gjøre? ) (Tilgang 2. august 2017 ) N Engl J Med. 2006; 355: 2733-43.
- For anastrozol , mindre endometriecancer, mindre cerebrovaskulær iskemi, mindre dyp venetrombose, men flere brudd og artralgi. For Letrozole , færre venøse tromboemboliske hendelser, men mer artralgi, brudd, hjerteproblemer og høyt kolesterol
- Colditz, GA og Bohlke, K. (2014), Prioriteringer for primær forebygging av brystkreft. CA: A Cancer Journal for Clinicians, 64: 186–194. doi: 10.3322 / caac.21225
- IARC Monografiprogram klassifiserer kombinert prevensjonsmiddel og monopausal hormonbehandling som kreftfremkallende stoffer , International Agency for Research on Cancer , 29. juli 2005 pressemelding
- (en) Chavez-MacGregor M Elias SG, Onland-C Moret et al. Postmenopausal brystkreftrisiko og kumulativt antall menstruasjonssykluser , Cancer Epidemiology Biomarkers & Prevention, 2005; 14: 799-804
- "Brystkreft: forebyggingskampanjer kalles for" Le Figaro , 23. oktober 2008
- (in) E. Riboli et al ". European Prospective Investigation in Cancer and Nutrition (EPIC) study populations and data collection ' Public health nutrition , vol. 5, n o 6B2002, s. 1113-1124 ( PMID 12639222 , les online [html] , åpnet 16. april 2013 )
- (i) R. Zamora-Ros et al., " Inntak av flavonoider og lignan i diett og brystkreft risikerer selon overgangsalder og hormonreseptorstatus i European Prospective Investigation in Cancer and Nutrition (EPIC) Study ' Breast cancer research and treatment ,2013( PMID 23572295 , les online [html] , åpnet 16. april 2013 )
- Konklusjon av en Women's Healthy Eating and Living (WHEL) studie, publisert sommeren 2007 i JAMA
- Eksperiment utført av INSERM i Tours (kilde: Science et Avenir fra april 2008)
- Bevers, Therese B, Bevis for Raloxifene som et reduksjonsmiddel for brystkreftrisiko for postmenopausale kvinner , JNCCN, 2007; 5: 817-822
- Nelson HD, Smith MB, Griffin JC, Fu R, bruk av medisiner for å redusere risikoen for primær brystkreft , Ann Intern Med 2013; 158: 604-614
- (i) Nora E Carbine , Liz Lostumbo Judi Wallace og Henry Ko , " Risikoreduserende mastektomi for forebygging av primær brystkreft " , Cochrane Database of Systematic Reviews ,5. april 2018( PMID 29620792 , PMCID PMC6494635 , DOI 10.1002 / 14651858.CD002748.pub4 , les online , åpnet 13. mai 2019 )
- (i) Nicolas Favez , Sarah Cairo Notari , Tania Antonini og Linda Charvoz , " Tilknytning og dreiemomenttilfredshet som prediktorer for uttrykt følelse hos kvinner som står overfor brystkreft og deres partnere i den umiddelbare perioden etter operasjonen " , British Journal of Health Psychology , flygning. 22, n o 1,1 st februar 2017, s. 169–185 ( ISSN 2044-8287 , DOI 10.1111 / bjhp.12223 , lest online , åpnet 23. august 2017 )
- " Marie Reno - Rosa Oktober - Toppen av nyheter - 27 september 2019 - Marie Réno - Toppen av nyheter på Rire & Chansons - Rire & Chansons " , på Rire & Chansons.fr (åpnes 07.10.2019 )
Se også
Relaterte artikler
- Bryst
- Eggstokkreft
- Livmorhalskreft
- Mastektomi , protese
- Mitoxantrone
- Kognitiv forstyrrelse etter cellegift
- Atossa
- Oncotype DX
- Seintinelles
Eksterne linker
- Myndighetsregistreringer :
- Merknader i generelle ordbøker eller leksikon : Brockhaus Enzyklopädie • Encyclopædia Britannica
- Helserelaterte ressurser :
- ICD-10 versjon: 2016
- MalaCards
- Nasjonalt kreftinstitutt
- NCI synonymordbok
- Orphanet
- (en) Internasjonal klassifisering av primæromsorg
- (no) Sykdommer ontologi
- (en) Sykdommer DB
- ( fr ) Mendeliansk arv hos mennesker
- ( fr ) Mendeliansk arv hos mennesker
- (sv) Internettmedisin
- (en + es) MedlinePlus
- (no + nn + nb) Oppbevar medisinske leksikon
- Brystkreft på helseforsikringsnettstedet
- www.cancerdusein.org Nettstedet til “Brystkreftforeningen, Parlons-en! », Ved begynnelsen av oktober måned Rose for å øke bevisstheten om kampen mot brystkreft og tidlig påvisning, i Frankrike siden 1994
- Brystkreft på nettstedet til National Federation for the Fight against Cancer
- Brystkreftkategori i dmoz-katalogen
- GRCS, brystkreftforskningsgruppen til CHUM forskningssenter i Montreal
- Radio Curie En informasjonsradio dedikert til kvinner med brystkreft og deres nærmeste